Чему равна лямбда чугуна — Морской флот
Изобретению уже известного вам жидконаполненного калориметра (см. § 06-в) предшествовало создание в ХVIII веке французами П.Лапласом и А.Лавуазье ледяного калориметра. Если при пользовании первым калориметром измеряют изменение температуры жидкости, то при пользовании вторым калориметром измеряют массу растаявшего льда. В ХVIII веке только так и можно было поступить, так как не было общепринятых методов измерения температуры.
Лаплас и Лавуазье опирались на труды своих предшественников, шотландца Д.Блэка и голландца И.Вильке, которые решили ввести в физику новое понятие: скрытая теплота.
 |
Вильке, например, в 1772 году нагревал смесь воды и льда и обнаружил, что часть теплоты «исчезает». То есть пламя греет, а температура смеси не повышается (см. левую часть рисунка). В 1803 году Блэк описал постоянство температуры тающего льда, несмотря на приток теплоты. Отсюда он пришёл к понятию «скрытой теплоты плавления», как он её назвал.
Позже он установил наличие и «скрытой теплоты парообразования», поскольку вода кипит при постоянной температуре, несмотря на приток теплоты (см. правую часть рисунка). На основе своих наблюдений Блэк чётко разграничил термины «количество теплоты» и «количество температуры». Первый термин сохранился в физике до наших дней, хотя мы чаще говорим «тело получило 100 Дж теплоты» вместо «тело получило 100 Дж количества теплоты». Второй термин в наши дни употребляется исключительно как «температура».
Усилиями физиков конца XVIII–начала XIX веков установлено, что количество теплоты прямо пропорционально массе расплавившегося вещества или массе испарившейся жидкости. То есть во сколько раз больше масса вещества, которое перешло в другое состояние, во столько же раз больше нужно теплоты.
Далее показан современный вид формул для расчёта теплоты плавления и теплоты парообразования. Они, наряду с уже известной вам основной калориметрической формулой Q = cmΔt°, по сей день лежат в основе всех методов калориметрических измерений.
- В предыдущем параграфе мы познакомились с устройством .
- При проведении измерений с его помощью .
- В ХVIII веке применяли ледяной калориметр, поскольку .
- Что Вильке понимал под «исчезновением теплоты»?
- Блэк ввёл понятие «скрытой теплоты плавления», так как наблюдал .
- Проводя наблюдения за «скрытыми теплотами», Блэк .
- Он ввёл понятие «скрытой теплоты плавления», так как .
- Важнейший итог научных работ Блэка состоит в том, что он .
- Количество теплоты пропорционально массе вещества. Это значит: .
- Три формулы: Q = cmΔt°, а также Q=λm и Q=rm .
Количество теплоты, необходимое для плавления, зависит от массы плавящегося вещества и удельной теплоты плавления:
Q – количество теплоты, Дж
λ – удельная теплота плавления, Дж/кг
m – масса вещества, кг
Удельная теплота плавления – физическая величина, показывающая количество теплоты, требуемое для превращения в жидкость 1 кг вещества без изменения его температуры. Коэффициенты «λ» для различных веществ, как правило, различны. Они измерены опытным путём и занесены в специальные таблицы (см. ниже).
Точные калориметрические измерения и опыты показывают, что при кристаллизации вещества (это процесс, обратный плавлению) выделяется такое же количество теплоты, какое было затрачено на образование расплава. Это – проявление закона сохранения энергии.
Количество теплоты, необходимое для парообразования, зависит от массы испаряющегося вещества и удельной теплоты парообразования:
Q – количество теплоты, Дж
r – удельная теплота парообразования, Дж/кг
m – масса вещества, кг
Удельная теплота парообразования – физическая величина, показывающая количество теплоты, требуемое для превращения в пар 1 кг вещества без изменения его температуры. Коэффициенты «r» для различных веществ, как правило, различны. Они измерены опытным путём и занесены в специальные таблицы (см. ниже).
Точные калориметрические измерения и опыты показывают, что при конденсации вещества (это процесс, обратный парообразованию) выделяется такое же количество теплоты, какое было затрачено на образование пара. Это – проявление закона сохранения энергии.
| Удельные теплоты плавления и парообразования, кДж/кг | ||||
| Лёд | 330 | Вода | 2260 | |
| Железо | 270 | Спирт | 906 | |
| Свинец | 24 | Свинец | 860 | |
- Произведением λ·m подсчитывают .
- Название коэффициента «лямбда» – .
- Удельная теплота плавления показывает .
- При кристаллизации жидкого вещества .
- Произведением r·m подсчитывают .
- Название коэффициента «эр» – .
- Удельная теплота парообразования показывает .
- При конденсации газообразного вещества .
- В таблице наибольший коэффициент «λ» имеет .
- В таблице наибольший коэффициент «r» имеет .
Физика.ru • Клуб для учителей физики, учащихся 7-9 классов и их родителей
УДЕЛЬНАЯ ТЕПЛОТА ПЛАВЛЕНИЯ — физ. величина, показывающая, какое количество теплоты необходимо для превращения 1 кг кристаллического вещества при температуре плавления в жидкость той же температуры; в СИ выражается в Дж/ кг … Большая политехническая энциклопедия
удельная теплота плавления — — [А.С.Гольдберг. Англо русский энергетический словарь. 2006 г.] Тематики энергетика в целом EN heat of fusion … Справочник технического переводчика
удельная теплота плавления — savitoji lydymosi šiluma statusas T sritis fizika atitikmenys: angl. specific fusion heat; specific melting heat vok. spezifische Schmelzwärme, f rus. удельная теплота плавления, f pranc. chaleur massique de fusion, f; chaleur spécifique de… … Fizikos terminų žodynas
удельная теплота плавления — savitoji lydymosi šiluma statusas T sritis Energetika apibrėžtis Lydymosi šiluma, padalyta iš kristalinės medžiagos masės. atitikmenys: angl. specific heat of fusion vok. spezifische Schmelzwärme, f rus. удельная теплота плавления, f pranc.… … Aiškinamasis šiluminės ir branduolinės technikos terminų žodynas
ТЕПЛОТА ПЛАВЛЕНИЯ — – количество теплоты, которое необходимо сообщить веществу в равновесном процессе, чтобы перевести его из твердого (кристаллического) состояния, в жидкое (то же количество теплоты выделяется при кристаллизации вещества). Теплота плавления… … Металлургический словарь
теплота сгорания — [heat value] теплота горения, теплотворная способность, теплотворность, теплопроизводительность, калорийность количество теплоты, выделенное при полном cгании топлива; измеряется в Дж. Теплота сгорания единицы массы или объема топлива называют… … Энциклопедический словарь по металлургии
Энтальпия плавления — Удельная теплота плавления (также существует равнозначное понятие удельная теплота кристаллизации) количество теплоты, которое необходимо сообщить одной единице массы кристаллического вещества в равновесном изобарно изотермическом процессе,… … Википедия
Влага — Вода Общие Систематическое наименование Оксид водорода Традиционные названия вода Химическая формула Н2O … Википедия
Водная среда — Вода Общие Систематическое наименование Оксид водорода Традиционные названия вода Химическая формула Н2O … Википедия
Воды — Вода Общие Систематическое наименование Оксид водорода Традиционные названия вода Химическая формула Н2O … Википедия
Задача:
Сколько потребуется каменного угля, чтобы расплавить 100 тонн чугуна, взятого при температуре 20 гр. цельсия, если КПД печи 40%
Пояснения:
удельная теплота сгорания кам. угля 2,7 *10 в 7 степени
удельная теплоемкость чугуна 540 дж/кг граус цельсия
удельная теплота плавления чугуна 98-140 дж/кг(нужно брать 100)
morflot.su
просто и доходчиво – формула, таблица

Содержание:
Под плавлением в физике подразумевают процесс превращения тела из твердого состояния в жидкое, под действием температуры. Классическим повсеместным примером плавления из жизни является таяние льдов, их превращение в воду, или превращение твердого куска олова в жидкий припой под действием паяльника. Передача тому или иному телу определенного количества тепла может изменить его агрегатное состояние, это удивительное свойство твердых тел превращаться в жидкие под действием температуры имеет большое значение для науки и техники. Ученым (а также техникам, инженерам) важно знать при каких температурах плавятся те или иные металлы (а порой и не только металлы), и для этого в физику вошло такое понятие как «удельная теплота плавления». О том, что означает удельная теплота плавления, какая ее формула расчета, читайте далее.
Почему твердое тело становится жидким?
Но давайте для начала разберем, как происходит сам процесс плавления на атомно-молекулярном уровне. Как мы знаем, в любом твердом теле все атомы и молекулы находятся четко и упорядочено в узлах кристаллической решетки, благодаря этому твердое тело и является твердым.
Но что происходит, если мы начинает это самое гипотетическое твердо тело сильно нагревать – под действием температуры атомы и молекулы резко увеличивают свою кинетическую энергию и по достижении определенных критических значений, они начинают покидать кристаллическую решетку, вырываться из нее. А само твердое тело начинает буквально распадаться, превращаясь в некое жидкое вещество – так происходит плавление.
При этом процесс плавления происходит не резким скачком, а постепенно. Также стоит заметить, что плавление относится к эндотермическим процессам, то есть процессам, при которых происходит поглощение теплоты.
Процесс обратный к плавлению называют кристаллизацией – это когда тело из жидкого состояния наоборот превращается в твердое. Если вы оставите воду в морозилке, она через какое-то время превратится в лед – это самый типичный пример кристаллизации из реальной жизни.
Определение удельной теплоты плавления
Удельной теплотой плавления называют физическую величину равную количеству тепла (в джоулях), которое необходимо передать твердому телу массой 1 кг, чтобы полностью перевести его в жидкое состояние. Удельную теплоту плавления обозначают греческой буквой «лямбда» – λ.
Формула удельной теплоты плавление выглядит так:
λ = Q/m
Где m – масса плавящегося вещества, а Q – количество тепла, переданное веществу при плавлении.
Зная значение удельной теплоты плавления, мы можем определить, какое количество тепла необходимо передать для тела с той или иной массой, для его полного расплавления:
Q = λ * m
Для разных веществ удельная теплота плавления была определена экспериментально.
Единица удельной теплоты плавления
Многих интересует вопрос, в каких единицах измеряется удельная теплота плавления. Так вот, удельная теплота плавления измеряется в Джоулях на килограмм – Дж/кг.
Таблица удельной теплоты плавления
Значение удельной теплоты для разных веществ: золота, серебра, цинка, олова и многих других металлов можно найти в специальных таблицах и справочниках. Обычно эти значения приводятся в виде таблицы.
Вашему вниманию таблица удельной теплоты плавления разных веществ
| Вещество | 105 * Дж/кг | ккал/кг | 105 * Дж/кг | ккал/кг | |
| Алюминий | 3,8 | 92 | Ртуть | 0,1 | 3,0 |
| Железо | 2,7 | 65 | Свинец | 0,3 | 6,0 |
| Лед | 3,3 | 80 | Серебро | 0,87 | 21 |
| Медь | 1,8 | 42 | Сталь | 0,8 | 20 |
| Нафталин | 1,5 | 36 | Цинк | 1,2 | 28 |
| Олово | 0,58 | 14 | Платина | 1,01 | 24,1 |
| Парафин | 1,5 | 35 | Золото | 0,66 | 15,8 |
Интересный факт: самым тугоплавким металлом на сегодняшний день является карбид тантала – ТаС. Для его плавления необходима температура 3990 С. Покрытия из ТаС применяют для защиты металлических форм, в которых отливают детали из алюминия
Рекомендованная литература и полезные ссылки
- Енохович А. С. Краткий справочник по физике. — М.: «Высшая школа», 1976. — С. 114. — 288 с.
- Atkins, Peter & Jones, Loretta (2008), Chemical Principles: The Quest for Insight (4th ed.), W. H. Freeman and Company, с. 236, ISBN 0-7167-7355-4
- Hoffer J. K., Gardner W. R., Waterfield C. G., Phillips N. E. Thermodynamic properties of 4He. II. The bcc phase and the P-T and VT phase diagrams below 2 K (англ.) // Journal of Low Temperature Physics (англ.)русск. : journal. — 1976. — April (vol. 23, no. 1). — P. 63—102. — DOI:10.1007/BF00117245. — Bibcode: 1976JLTP…23…63H.
Удельная теплота плавления, видео
Эта статья доступна на английском языке – Enthalpy of Fusion.
www.poznavayka.org
Удельная теплота плавления ℹ️ определение, обозначение и единица измерения, формула расчета физической величины, таблица показателей для различных веществ

Общая информация
Правильное понимание удельного значения теплоты плавления невозможно без изучения ключевых особенностей самого процесса расплавки. И при плавлении, и при кристаллизации какого-либо вещества его внутренняя энергия изменяется. При первом процессе она возрастает, так как он неизменно сопровождается нагреванием — главным условием для увеличения энергии. Температура же при расплавке остается неизменной. В определенном смысле это парадоксально, ведь внутренняя энергия может характеризоваться температурой.

Однако увеличению энергии при неизменной температуре существует весьма простое и логичное объяснение. Во время процесса расплавки разрушается пространственная решетка кристаллического тела, на это уходит вся энергия. Разрушение кристаллической решетки требует расходования определенного количества энергии со стороны какого-либо внешнего источника. Как следствие, в ходе процесса расплавки происходит увеличение внутренней энергии тела.
В процессе отвердевания тела или, иначе говоря, кристаллизации, напротив, происходит уменьшение его внутренней энергии, так как оно отдает тепло телам, которые его окружают. Отвердевание (кристаллизация) — это обратный процесс по отношению к расплавке. Молекулы вещества образуют общую (единую) систему, и в ходе этого объединения отдаваемая составляющими вещества избыточная энергия поглощается внешней средой.
Основные сведения о теплоте плавления
По закону сохранения энергии тело поглощает в ходе плавления и отдает во время отвердевания (при необходимой для каждого из этих процессов температуре) равное количество тепла.

Теплотой плавления называют количество теплоты, которое необходимо для того, чтобы физическое тело при температуре плавления перешло в жидкое состояние из твердого. Это тепловое явление — частный случай фазового перехода в термодинамике.
На теплоту расплавки влияют масса плавящегося вещества, а также свойства, которыми оно обладает и которые для него характерны. Эта связь между теплотой расплавки физического тела и родом вещества, выражающаяся через зависимость первого от второго, измеряется удельной величиной.
Для плавления вещества требуется такое же количество тепла, которое выделяется при кристаллизации, поэтому определение удельного значения теплоты существует в двух равнозначных понятиях — для плавления и для кристаллизации. У этой величины есть и альтернативное наименование — энтальпия плавления.
Особенности измерения
Экспериментальным путем ученые-физики установили, что для перевода одного и того же вещества в жидкое из твердого состояния требуется разное количество теплоты. Затем исследователями-экспериментаторами было принято решение сравнить эти показатели при одинаковой массе вещества. Так появилось понятие удельной величины.
Согласно ее упрощенному определению, она показывает соотношение теплоты плавления тела из определенного вещества и его массы. Этот показатель считается главной характеристикой как для плавления, так и для кристаллизации.
Единицей измерения этой величины, согласно Международной системе единиц, считается Дж/кг (джоуль на килограмм). Обозначается удельный показатель буквой лямбда (реже встречается прочтение как ламбда) из греческого алфавита (аналог кириллической буквы «л»).

Находят удельную теплоту плавления по формуле: лямбда = Q/m, где Q — это обозначение количества теплоты, которое вещество получило при плавлении или выделило в процессе кристаллизации, а m — масса вещества (плавящегося или кристаллизующегося). Отсутствие температурного показателя в размерности обусловлено тем, что температура не меняется ни при плавлении, ни при кристаллизации.
Удельная величина при расплавке всегда положительна, а при кристаллизации — отрицательна. Исключение из этого правила существует (или, вернее, известно науке) только единственное — это химический элемент системы Менделеева под названием гелий, находящийся под высоким давлением. Он при расплавке отрицателен.
Чтобы перевести вещество в размере одного килограмма из твердого состояния в жидкое, нужно нагреть его до температуры плавления и подвести к нему теплоту в количестве, равном удельному показателю. В процессе кристаллизации одного килограмма вещества тепло выделяется ровно в том же количестве.
Для нахождения количества теплоты, необходимого для расплавки или кристаллизации вещества при соответствующих температурах, нужно удельную величину умножить на массу вещества. Для кристаллизующихся тел этот показатель будет со знаком минус, то есть отрицательным. Это связано с тем, что в процессе отвердевания все тепло теряется — выделяется не сохраняясь.
Сравнительная таблица
Таблица с удельной теплотой плавления некоторых веществ и химических элементов (вещества в таблице расположены не в алфавитном порядке, а по уменьшению их удельного показателя):
| Название вещества или элемента | Удельный показатель теплоты плавления в кДж/кг |
| Алюминий | 390 |
| Лед | 330 |
| Железо | 277 |
| Медь | 213 |
| Нафталин | 151 |
| Парафин | 150 |
| Эфир | 113 |
| Цинк | 112 |
| Серебро | 105 |
| Платина | 101 |
| Серый чугун | 100 |
| Сталь | 83 |
| Золото | 66 |
| Олово | 61 |
| Свинец | 25 |
| Белый чугун | 14 |
| Ртуть | 12 |
Удельные величины для этих веществ считаются табличными (постоянными и известными) значениями, поэтому производить расчеты для их поиска нет никакой необходимости.
Родственные величины
Так называемые удельные показатели существуют для характеристики не только плавления и кристаллизации. В физической науке помимо этих процессов удельными величинами теплоты характеризуются:
- парообразование;
- конденсация;
- теплоемкость.

Удельный показатель теплоты парообразования и конденсации отображает объем теплоты, необходимый для обращения единицы массы жидкости в пар и наоборот. Формула этой величины: Q/m. Таким образом, по сути, это то же самое, что и энтальпия расплавки и кристаллизации.
Что касается удельной теплоемкости, то это показатель соотношения теплоемкости и массы вещества. Он равен объему теплоты, передача которого единичной массе вещества необходима для изменения его температуры на один градус.
Тематические задания
Изучение тепловых явлений и их особенностей, к числу которых относится и удельная теплота, входит в школьную программу по физике для старших классов. Для проверки усвоения пройденного материала используются тематические задачи.
Задания на нахождение удельной теплоты парообразования помимо обычных текстовых условий в большинстве случаев сопровождаются графиками, отображающими температурные изменения, которые происходили с веществом по мере поглощения им теплоты.
Но графические задачи — не самые интересные. В число наиболее занимательных заданий входят такие:

- Кусок льда, размещавшийся в температуре -90 градусов Цельсия, начали нагревать посредством подведения к нему тепловой мощности постоянного типа. По прошествии 63 секунд от начала нагревания лед достиг температуры, необходимой для плавления. Требуется найти время в секундах, которое займет процесс плавления льда от момента его достижения нужного нагрева при условии, что потери теплоты нет. Ответ: 110 секунд.
- Кусок свинца, пребывавший в температуре +27,5 градуса Цельсия, путем подведения к нему постоянной тепловой мощности начали нагревать. Спустя 39 секунд после начала нагревания температура свинца достигла уровня плавления (+327,5 градуса Цельсия). Нужно определить продолжительность процесса плавления свинца в секундах от этого момента, с учетом отсутствия тепловых потерь. Ответ: 25 секунд.
Сравнение ответов этих задач позволяет оценить разницу между удельными величинами плавления льда и свинца. У первого она очень большая, а у второго, наоборот, маленькая. Это неудивительно — количество теплоты, нужное для плавления, напрямую зависит от свойств и характеристик вещества, в частности — от энергии связей, соединяющих частицы этого вещества между собой.
Роль большой удельной величины, которой обладает лед, неоценима как для природы, так и для человечества. Если бы этот показатель был меньше, то по весне все льды и снега растаяли, что обернулось бы ужасными последствиями. Потоки воды, образовавшиеся в результате такого таяния, смыли бы все на своем пути.
К счастью, ледяные и снежные массы не способны растаять за несколько мгновений. Физические свойства этих веществ лишний раз доказывают, что природа — гениальный и неподражаемый творец.
nauka.club
Теплоемкость чугуна, теплопроводность чугуна, плотность, энтальпия, состав и свойства
Удельная теплоемкость чугуна
В таблице представлены значения средней удельной теплоемкости чугуна и энтальпия (теплосодержание) серых чугунов различного состава в зависимости от температуры.
Теплоемкость чугуна выражена в кДж/(кг·град) и указана в диапазоне от 100 до 1350°С.
Из таблицы видно, что с повышением температуры значения массовой теплоемкости чугуна и его энтальпия возрастают.
То же можно сказать и про энтальпию серых чугунов. Значения удельной теплоемкости чугунов и их энтальпия имеют различие в зависимости от состава чугуна. Например, при температуре 200°С теплоемкость чугуна в зависимости от состава изменяется от 290,1 до 460,5 Дж/(кг·град). При нагревании чугуна до температуры 1300°С эта величина увеличивается и становится равной 800…900 Дж/(кг·град).
Теплопроводность чугуна
В таблице даны значения теплопроводности чугуна в зависимости от температуры и состава. Также указана теплопроводность жидкого чугуна при температуре 1400°С.
Представлены значения теплопроводности для следующих марок чугуна: обыкновенный чугун, чугун молибденохромистый, молибденовый, хромоникелевый, марганцевоникелевый, чугун никельрезист, никросилал, хромоалюминиевый, медистый, обыкновенный чистый, серый чугун, отожженый ковкий чугун, жидкий чугун.
Теплопроводность чугуна дана в зависимости от температуры в диапазоне от 0 до 400°С. По данным таблицы видно, что с ростом температуры теплопроводность чугуна уменьшается. Значения теплопроводности чугуна распространенных марок указаны также в этой таблице.
Плотность чугуна, температура плавления и коэффициент линейного расширения
В таблице представлена плотность чугуна различных сортов, а также температура плавления чугуна и его коэффициент теплового линейного расширения (КТлР).
Следует отметить что плотность чугуна в зависимости от сорта находится в диапазоне от 6600 до 7700 кг/м3. Температура плавления чугуна составляет от 1095 до 1315°С, а его КТлР от 10,5 до 18·10-6 1/град.
| Плотность чугуна, кг/м3 | |
|---|---|
| Серый чугун наименее плотный высокоуглеродистый | 6600-6950 |
| Серый чугун обычный средней плотности | 7000-7300 |
| Высококачественный чугун малоуглеродистый | 7400-7500 |
| Жаростойкий, жаропрочный | 7500-7600 |
| Чугун высоколегированный аустенитного класса | 7500-7700 |
| Температура плавления чугуна, °С | |
| Обычный серый чугун | 1095-1315 |
| Жаростойкий чугун | 1300 |
| Коэффициент линейного расширения чугуна (КТлР), 1/град | |
| Обычный серый при температуре 20…450°С | 10,5·10-6 |
| Обычный серый при температуре 20…750°С | 14·10-6 |
| Высоколегированный аустенитного класса при температуре 20…150°С | (16…18)·10-6 |
| Жаростойкий чугун при температуре 20…250°С | 16,7·10-6 |
| Жаростойкий чугун при температуре 250…750°С | 17,6·10-6 |
Источники:
- Казанцев Е. И. Промышленные печи. Справочное руководство для расчетов и проектирования.
- Чиркин В. С. Теплофизические свойства материалов ядерной техники. Справочник.
thermalinfo.ru
| Уде́льная теплота́ плавле́ния/кристаллиза́ции — количество теплоты, которое необходимо сообщить одной единице массы кристаллического вещества в равновесном изобарно-изотермическом процессе, чтобы перевести его из твёрдого (кристаллического) состояния в жидкое (то же количество теплоты выделяется при кристаллизации вещества). Теплота плавления — частный случай теплоты фазового перехода первого рода. Различают удельную теплоту плавления (Дж/кг) и молярную (Дж/моль). Удельная теплота плавления обозначается буквой λ (греческая буква лямбда).
|
|
ru.teplowiki.org
§ 8.8. Теплота плавления
При плавлении происходит разрушение пространственной решетки кристаллического тела. На этот процесс расходуется определенное количество энергии от какого-нибудь внешнего источника. В результате внутренняя энергия тела в процессе плавления увеличивается.
Количество теплоты, необходимое для перехода тела из твердого состояния в жидкое при температуре плавления, называется теплотой плавления.
В процессе отвердевания тела, наоборот, внутренняя энергия тела уменьшается. Тело отдает теплоту окружающим телам. Согласно закону сохранения энергии количество теплоты, поглощенное телом при плавлении (при температуре плавления), равно количеству теплоты, отданному этим телом при отвердевании (при температуре отвердевания).
Удельная теплота плавления
Теплота плавления зависит от массы плавящегося вещества и его свойств. Зависимость теплоты плавления от рода вещества характеризуют удельной теплотой плавления этого вещества.
Удельной теплотой плавления вещества называется отношение теплоты плавления тела из этого вещества к массе тела.
Обозначим теплоту плавления через Qпл, массу тела буквой т и удельную теплоту плавления буквой λ. Тогда
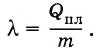 (8.8.1)
(8.8.1)
Таким образом, чтобы расплавить кристаллическое тело массой m, взятое при температуре плавления, необходимо количество теплоты, равное
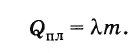 (8.8.2)
(8.8.2)
Теплота кристаллизации
Согласно закону сохранения энергии количество теплоты, выделяемое при кристаллизации тела (при температуре кристаллизации), равно
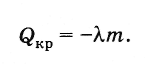 (8.8.3)
(8.8.3)
Из формулы (8.8.1) следует, что удельная теплота плавления в СИ выражается в джоулях на килограмм.
Довольно велика удельная теплота плавления льда 333,7 кДж/кг. Удельная теплота плавления свинца всего лишь 23 кДж/кг, а золота — 65,7 кДж/кг.
Формулы (8.8.2) и (8.8.3) используются при решении задач на составление уравнений теплового баланса в тех случаях, когда мы имеем дело с плавлением и отвердеванием кристаллических тел.
Роль теплоты плавления льда и кристаллизации воды в природе
Поглощение теплоты при таянии льда и выделение ее при замерзании воды оказывают значительное влияние на изменение температуры воздуха, особенно вблизи водоемов. Все вы, вероятно, замечали, что во время обильных снегопадов обычно наступает потепление.
Очень важно большое значение удельной теплоты плавления льда. Еще в конце XVIII в. шотландский ученый Д. Блэк (1728—1799), открывший существование теплоты плавления и кристаллизации, писал: «Если бы лед не обладал значительной теплотой плавления, то тогда весной вся масса льда должна была бы растаять в несколько минут или секунд, так как теплота из воздуха непрерывно передается льду. Но тогда последствия этого были бы ужасны: ведь и при существующем положении возникают большие наводнения и сильные потоки воды при таянии больших масс льда и снега».
Сопло космической ракеты
Приведем интересный технический пример практического использования теплоты плавления и парообразования. При изготовлении сопла для космической ракеты следует учитывать, что струя газов, выходящая из сопла ракеты, имеет температуру около 4000 °С. В природе практически отсутствуют материалы, которые в чистом виде могли бы выдержать такую температуру. Поэтому приходится прибегать ко всякого рода ухищрениям, чтобы охладить материал сопла во время горения топлива.
Сопло изготавливают методом порошковой металлургии. В полость формы закладывается порошок тугоплавкого металла (вольфрам). Затем его подвергают сдавливанию. Порошок спекается, получается пористая структура типа пемзы. Затем эта «пемза» пропитывается медью (ее температура плавления всего 1083 °С).
Полученный материал называется псевдосплавом. На рисунке 8.31 показана фотография микроструктуры псевдосплава. На белом фоне вольфрамового каркаса видны медные включения неправильной формы. Этот сплав может, как это ни невероятно, кратковременно работать даже при температуре газов, образующихся при сгорании топлива, т. е. выше 4000°С.


Рис. 8.31
Происходит это следующим образом. Вначале температура сплава растет, пока не достигнет температуры плавления меди t1 (рис. 8.32). После этого температура сопла не будет меняться, пока вся медь не расплавится (промежуток времени от τ1 до τ2). В дальнейшем температура опять возрастает до тех пор, пока медь не закипит. Это происходит при температуре t2 = 2595 °С, меньшей температуры плавления вольфрама (3380 °С). Пока вся медь не выкипит, температура сопла опять меняться не будет, так как испаряющаяся медь забирает теплоту от вольфрама (промежуток времени от τ3 до τ4). Конечно, сколько угодно долго сопло работать не будет. После испарения меди вольфрам опять начнет нагреваться. Однако двигатель ракеты работает всего лишь несколько минут, а за это время сопло не успеет перегреться и расплавиться.
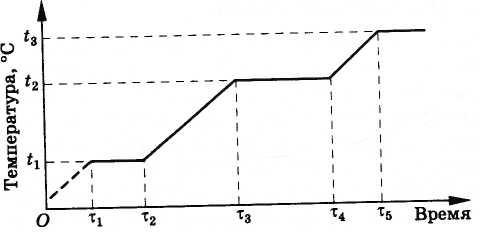
Рис. 8.32
studfile.net
06-г. Теплота плавления и парообразования
§ 06-г. Теплота плавления и парообразования
Изобретению уже известного вам жидконаполненного калориметра (см. § 06-в) предшествовало создание в ХVIII веке французами П.Лапласом и А.Лавуазье ледяного калориметра. Если при пользовании первым калориметром измеряют изменение температуры жидкости, то при пользовании вторым калориметром измеряют массу растаявшего льда. В ХVIII веке только так и можно было поступить, так как не было общепринятых методов измерения температуры.
Лаплас и Лавуазье опирались на труды своих предшественников, шотландца Д.Блэка и голландца И.Вильке, которые решили ввести в физику новое понятие: скрытая теплота.
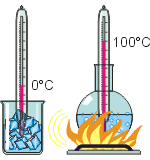
Вильке, например, в 1772 году нагревал смесь воды и льда и обнаружил, что часть теплоты «исчезает». То есть пламя греет, а температура смеси не повышается (см. левую часть рисунка). В 1803 году Блэк описал постоянство температуры тающего льда, несмотря на приток теплоты. Отсюда он пришёл к понятию «скрытой теплоты плавления», как он её назвал.
Позже он установил наличие и «скрытой теплоты парообразования», поскольку вода кипит при постоянной температуре, несмотря на приток теплоты (см. правую часть рисунка). На основе своих наблюдений Блэк чётко разграничил термины «количество теплоты» и «количество температуры». Первый термин сохранился в физике до наших дней, хотя мы чаще говорим «тело получило 100 Дж теплоты» вместо «тело получило 100 Дж количества теплоты». Второй термин в наши дни употребляется исключительно как «температура».
Усилиями физиков конца XVIII–начала XIX веков установлено, что количество теплоты прямо пропорционально массе расплавившегося вещества или массе испарившейся жидкости. То есть во сколько раз больше масса вещества, которое перешло в другое состояние, во столько же раз больше нужно теплоты.
Далее показан современный вид формул для расчёта теплоты плавления и теплоты парообразования. Они, наряду с уже известной вам основной калориметрической формулой Q = cmΔt°, по сей день лежат в основе всех методов калориметрических измерений.
Количество теплоты, необходимое для плавления, зависит от массы плавящегося вещества и удельной теплоты плавления:
Формула для подсчёта количества теплоты, поглощаемого телом при плавлении или выделяющегося при его кристаллизации. Формула читается так: «Ку равно лямбда эм».
| Q = λ·m | Q – количество теплоты, Дж |
Удельная теплота плавления – физическая величина, показывающая количество теплоты, требуемое для превращения в жидкость 1 кг вещества без изменения его температуры. Коэффициенты «λ» для различных веществ, как правило, различны. Они измерены опытным путём и занесены в специальные таблицы (см. ниже).
Точные калориметрические измерения и опыты показывают, что при кристаллизации вещества (это процесс, обратный плавлению) выделяется такое же количество теплоты, какое было затрачено на образование расплава. Это – проявление закона сохранения энергии.
Количество теплоты, необходимое для парообразования, зависит от массы испаряющегося вещества и удельной теплоты парообразования:
Формула для подсчета количества теплоты, поглощаемого телом при парообразовании или выделяющегося при его конденсации. Формула читается так: «Ку равно эр эм».
| Q = r·m | Q – количество теплоты, Дж |
Удельная теплота парообразования – физическая величина, показывающая количество теплоты, требуемое для превращения в пар 1 кг вещества без изменения его температуры. Коэффициенты «r» для различных веществ, как правило, различны. Они измерены опытным путём и занесены в специальные таблицы (см. ниже).
Точные калориметрические измерения и опыты показывают, что при конденсации вещества (это процесс, обратный парообразованию) выделяется такое же количество теплоты, какое было затрачено на образование пара. Это – проявление закона сохранения энергии.
Удельные теплоты плавления или парообразования показывают количество теплоты, которое необходимо для плавления или превращения в пар 1 кг вещества при постоянной температуре.
| Удельные теплоты плавления и парообразования, кДж/кг | ||||
| Лёд | 330 | Вода | 2260 | |
| Железо | 270 | Спирт | 906 | |
| Свинец | 24 | Свинец | 860 | |
В вашем браузере отключен Javascript.
Чтобы произвести расчеты, необходимо разрешить элементы ActiveX!
Источник
Источник информации
×Не можешь написать работу сам?
Доверь её нашим специалистам
от 100 р.стоимость заказа
2 часамин. срок
Узнать стоимость
calcsbox.com
