Титан. Описание, свойства, происхождение и применение металла
Брусок кристаллического титана
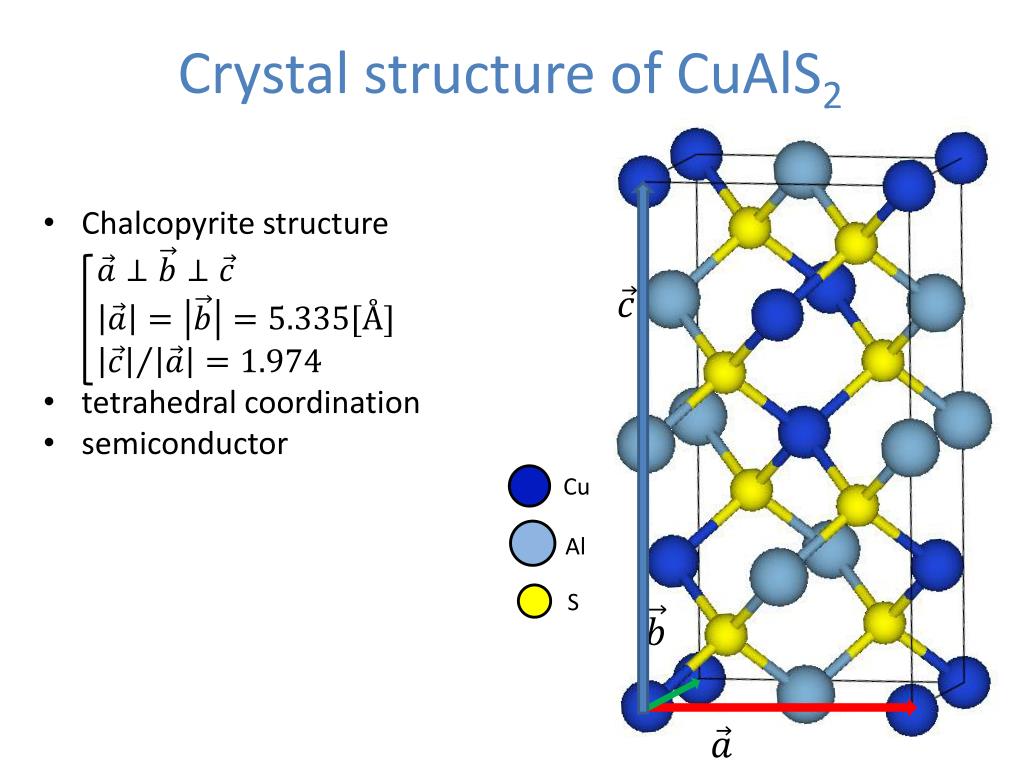
Титан — лёгкий прочный металл серебристо-белого цвета. Существует в двух кристаллических модификациях: α-Ti с гексагональной плотноупакованной решёткой, β-Ti с кубической объёмно-центрированной упаковкой, температура полиморфного превращения α↔β 883 °C.Титан и титановые сплавы сочетают легкость, прочность, высокую коррозийную стойкость, низкий коэффициент теплового расширения, возможность работы в широком диапазоне температур.
СТРУКТУРА
Кристаллическая структура кристалла
Титан имеет две аллотропические модификации. Низкотемпературная модификация, существующая до 882 °C, имеет гексагональную плотноупакованную решетку с периодами а = 0,296 нм и с = 0,472 нм. Высокотемпературная модификация имеет решетку объемноцентрированного куба с периодом а = 0,332 нм.
Полиморфное превращение (882 °C) при медленном охлаждении происходит по нормальному механизму с образованием равноосных зерен, а при быстром охлаждении — по мартенситному механизму с образованием игольчатой структуры.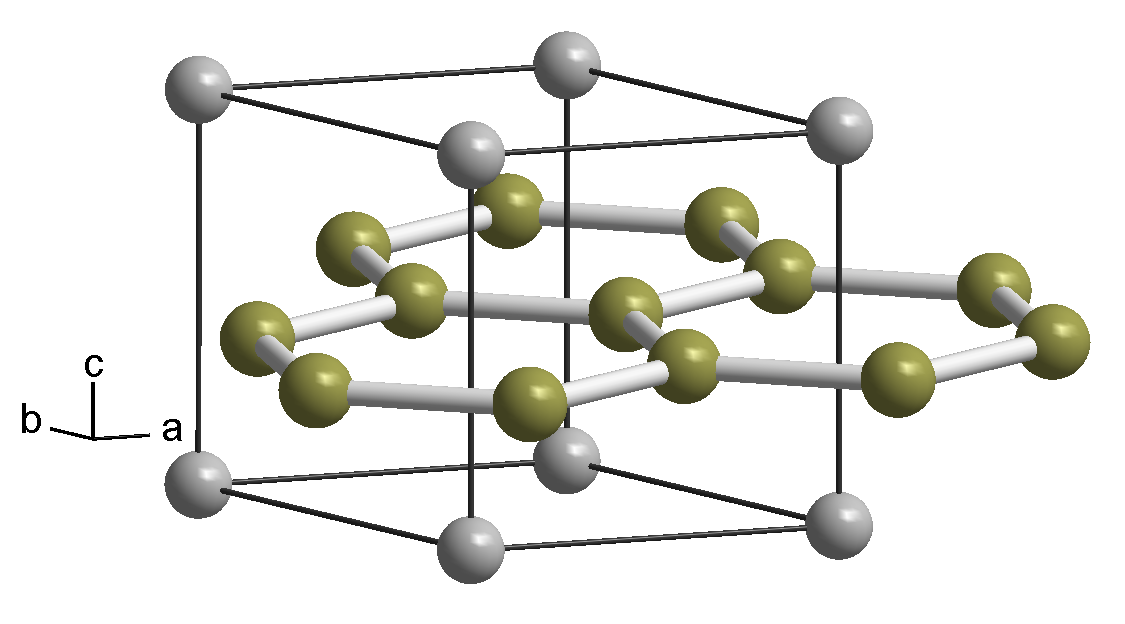
Титан обладает высокой коррозионной и химической стойкостью благодаря защитной окисной пленке на его поверхности. Он не корродирует в пресной и морской воде, минеральных кислотах, царской водке и др.
СВОЙСТВА
Кристаллы титана
Точка плавления 1671 °C, точка кипения 3260 °C, плотность α-Ti и β-Ti соответственно равна 4,505 (20 °C) и 4,32 (900 °C) г/см³, атомная плотность 5,71×1022 ат/см³. Пластичен, сваривается в инертной атмосфере.
Применяемый в промышленности технический титан содержит примеси кислорода, азота, железа, кремния и углерода, повышающие его прочность, снижающие пластичность и влияющие на температуру полиморфного превращения, которое происходит в интервале 865-920 °С. Для технического Титана марок ВТ1-00 и ВТ1-0 плотность около 4,32 г/см Конфигурация внешней электронной оболочки атома Ti 3d24s2.
Конфигурация внешней электронной оболочки атома Ti 3d24s2.
Имеет высокую вязкость, при механической обработке склонен к налипанию на режущий инструмент, и поэтому требуется нанесение специальных покрытий на инструмент, различных смазок.
При обычной температуре покрывается защитной пассивирующей пленкой оксида TiO2, благодаря этому коррозионностоек в большинстве сред (кроме щелочной). Титановая пыль имеет свойство взрываться. Температура вспышки 400 °C.
ЗАПАСЫ И ДОБЫЧА
Кристаллы титана
Основные руды: ильменит (FeTiO3), рутил (TiO2), титанит (CaTiSiO5).
На 2002 год, 90 % добываемого титана использовалось на производство диоксида титана TiO2. Мировое производство диоксида титана составляло 4,5 млн т. в год. Подтвержденные запасы диоксида титана (без России) составляют около 800 млн т. На 2006 год, по оценке Геологической службы США, в пересчёте на диоксид титана и без учёта России, запасы ильменитовых руд составляют 603—673 млн т.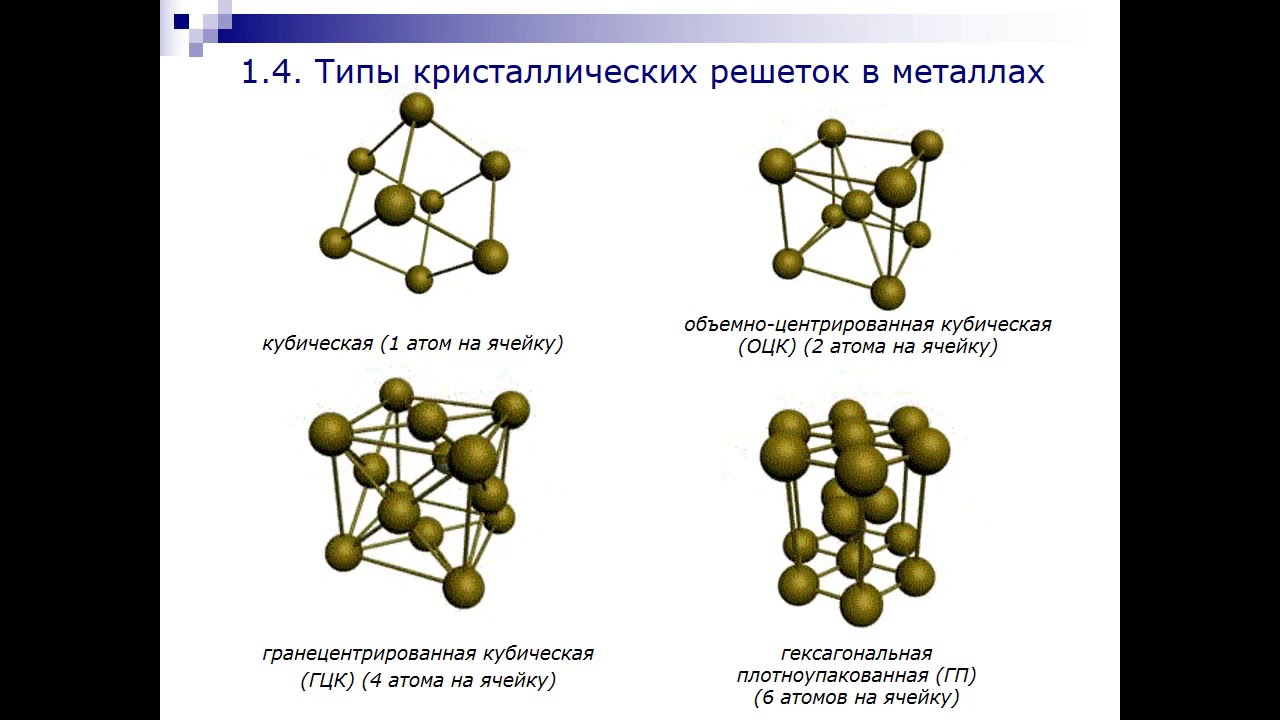
Россия обладает вторыми в мире, после Китая, запасами титана. Минерально-сырьевую базу титана России составляют 20 месторождений (из них 11 коренных и 9 россыпных), достаточно равномерно рассредоточенных по территории страны. Самое крупное из разведанных месторождений находится в 25 км от города Ухта (Республика Коми). Запасы месторождения оцениваются в 2 миллиарда тонн.
Концентрат титановых руд подвергают сернокислотной или пирометаллургической переработке. Продукт сернокислотной обработки — порошок диоксида титана TiO2. Пирометаллургическим методом руду спекают с коксом и обрабатывают хлором, получая пары тетрахлорида титана их при 850 °C восстанавливают магнием.
Полученную титановую «губку» переплавляют и очищают. Ильменитовые концентраты восстанавливают в электродуговых печах с последующим хлорированием возникающих титановых шлаков.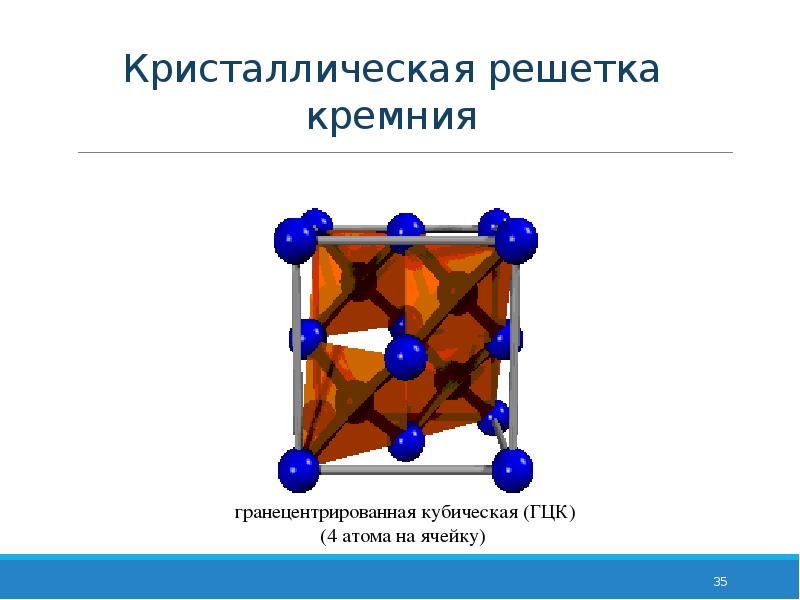
ПРОИСХОЖДЕНИЕ
Титановая руда
Титан находится на 10-м месте по распространённости в природе. Содержание в земной коре — 0,57 % по массе, в морской воде — 0,001 мг/л. В ультраосновных породах 300 г/т, в основных — 9 кг/т, в кислых 2,3 кг/т, в глинах и сланцах 4,5 кг/т. В земной коре титан почти всегда четырёхвалентен и присутствует только в кислородных соединениях. В свободном виде не встречается. Титан в условиях выветривания и осаждения имеет геохимическое сродство с Al2O3. Он концентрируется в бокситах коры выветривания и в морских глинистых осадках.
Перенос титана осуществляется в виде механических обломков минералов и в виде коллоидов. До 30 % TiO Различают коренные руды титана — ильменит-титаномагнетитовые и россыпные — рутил-ильменит-цирконовые.
Различают коренные руды титана — ильменит-титаномагнетитовые и россыпные — рутил-ильменит-цирконовые.
ПРИМЕНЕНИЕ
Изделия из титана
Титановые сплавы играют большую роль в авиационной технике, где стремятся получить наиболее легкую конструкцию в сочетании с необходимой прочностью. Титан легок по сравнению с другими металлами, но в то же время может работать при высоких температурах. Из титановых сплавов изготовляют обшивку, детали крепления, силовой набор, детали шасси, различные агрегаты. Также данные материалы применяются в конструкциях авиационных реактивных двигателей. Это позволяет уменьшить их массу на 10-25%. Из титановых сплавов производят диски и лопатки компрессора, детали воздухозаборника и направляющего аппарата, крепеж.
Также титан и его сплавы используют в ракетостроении. Ввиду кратковременной работы двигателей и быстрого прохождения плотных слоев атмосферы в ракетостроении в значительной мере снимаются проблемы усталостной прочности, статической выносливости и отчасти ползучести.
Технический титан из-за недостаточно высокой теплопрочности не пригоден для применения в авиации, но благодаря исключительно высокому сопротивлению коррозии в ряде случаев незаменим в химической промышленности и судостроении. Так его применяют при изготовлении компрессоров и насосов для перекачки таких агрессивных сред, как серная и соляная кислота и их соли, трубопроводов, запорной арматуры, автоклав, различного рода емкостей, фильтров и т.п. Только титан обладает коррозионной стойкостью в таких средах, как влажный хлор, водные и кислые растворы хлора, поэтому из данного металла изготовляют оборудование для хлорной промышленности. Из титана делают теплообменники, работающие в коррозионно активных средах, например в азотной кислоте (не дымящей).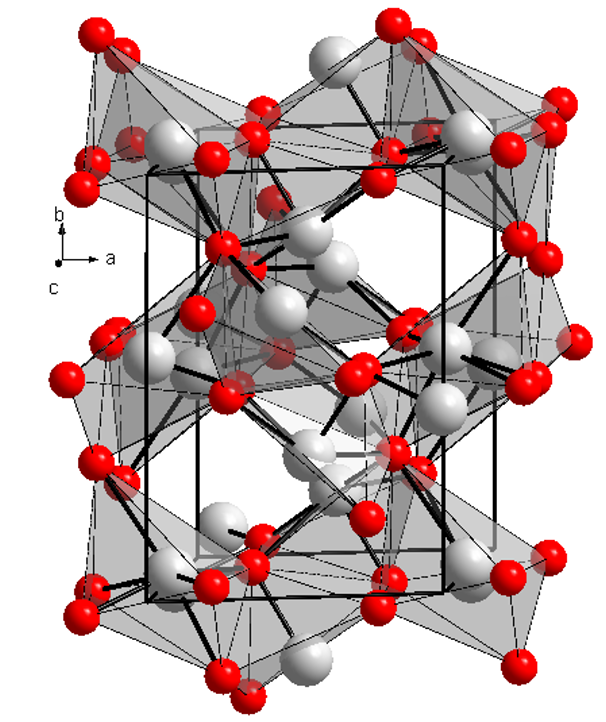
Титановые сплавы перспективны для использования во многих других применениях, но их распространение в технике сдерживается высокой стоимостью и дефицитностью титана.
Титан (англ. Titanium) — Ti
| Молекулярный вес | 47.88 г/моль |
| Происхождение названия | Минерал получил своё название в честь титанов, персонажей древнегреческой мифологии, детей Геи. |
| IMA статус | подтвержден в 2010 году |
КЛАССИФИКАЦИЯ
| Strunz (8-ое издание) | 1/A.06-05 |
| Dana (7-ое издание) | 1.1.36.1 |
| Nickel-Strunz (10-ое издание) | 1.AB.05 |
ФИЗИЧЕСКИЕ СВОЙСТВА
| Цвет минерала | Серебристо-серый |
| Цвет черты | серовато черный |
| Прозрачность | непрозрачный |
| Блеск | металлический |
| Спайность | нет |
| Твердость (шкала Мооса) | 4 |
| Излом | в зазубринах |
| Прочность | податливый |
| Плотность (измеренная) | 4. 503 г/см3 503 г/см3 |
| Радиоактивность (GRapi) | 0 |
| Магнетизм | парамагнетик |
ОПТИЧЕСКИЕ СВОЙСТВА
| Люминесценция в ультрафиолетовом излучении | не флюоресцентный |
КРИСТАЛЛОГРАФИЧЕСКИЕ СВОЙСТВА
| Точечная группа | 6/mmm (6/m 2/m 2/m) — дигексагональный дипирамидальный |
| Пространственная группа | P63/mmc |
| Сингония | гексагональная |
| Параметры ячейки | a=2,951 с=4,697 (α-Ti) |
Интересные статьи:
mineralpro.ru 13.07.2016Титан Кристаллическая структура — Энциклопедия по машиностроению XXL
Цирконии (Zr) — температура плавления 1852°С, температура кипения 3600°С, атомная масса 91,22, в Периодической системе элементов Д.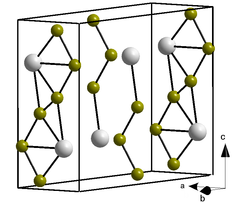 И. Менделеева расположен под номером 40, является аналогом титана. Плотность 6,49 г/см . Он имеет, как титан, две модификации а н fi. При температуре 20 — 862°С кристаллическая структура а-фазы гексагональная плотноупакованная, а = 0,323 нм, с = 0,5133 нм, атомный радиус г = 0,160 нм.
[c.83]
И. Менделеева расположен под номером 40, является аналогом титана. Плотность 6,49 г/см . Он имеет, как титан, две модификации а н fi. При температуре 20 — 862°С кристаллическая структура а-фазы гексагональная плотноупакованная, а = 0,323 нм, с = 0,5133 нм, атомный радиус г = 0,160 нм.
[c.83] Сплав Алюминий Никель Медь Кобальт Титан Ниобий Кремний Тип кристаллической структуры [c.98]
Обычно металлы с гексагональной кристаллической структурой имеют пониженную пластичность из-за ограниченного количества систем скольжения. Титан (а также цирконий) представляет исключение из этого правила. Одной из причин этого является благоприятное отношение осей da кристаллической решетки титана. Кроме того, у титана установлено по крайней мере 30 возможных систем скольжения и двойникования в связи с этим по пластичности титан не уступает другим металлам с иными типами кристаллических решеток (табл. 10). [c.43]
Как отмечено ранее, титан существует в модификациях а и р. Температура аллотропического превращения для чистого титана равна 882—885° С. а-Титан пластичнее Р-титана, что объясняется особенностями кристаллической структуры. Примеси в титане (кислород, азот, водород и др.) значительно ухудшают его пластичность. Все это следует учитывать при разработке технологии ковки, штамповки, прессования и прокатки технического титана. Его необходимо деформировать с меньшими обжатиями и более частыми отжигами, чем чистый титан (иодидный).
[c.294]
Температура аллотропического превращения для чистого титана равна 882—885° С. а-Титан пластичнее Р-титана, что объясняется особенностями кристаллической структуры. Примеси в титане (кислород, азот, водород и др.) значительно ухудшают его пластичность. Все это следует учитывать при разработке технологии ковки, штамповки, прессования и прокатки технического титана. Его необходимо деформировать с меньшими обжатиями и более частыми отжигами, чем чистый титан (иодидный).
[c.294]
Молибден принадлежит к мономорфным металлам с характерной объемноцентрированной кристаллической структурой. При сварке молибдена и его сплавов мало растворимые в металле кислород и углерод создают легкоплавкие эвтектики. Как и титан, молибден [c.392]
Титан имеет при нормальных температурах гексагональную кристаллическую структуру с плотной упаковкой атомов. При 885° эта структура переходит в структуру с объемно-центрированной кубической решеткой.
[c. 570]
570]
Для повышения жаропрочности стали необходимо обеспечить торможение дислокаций и диффузии вакансий как по границам, так и в объеме зерна. Дислокации хорошо затормаживаются мелкодисперсными карбидами и интерметаллидами. Легирование твердого раствора элементами, повышающими жаропрочность, приводит к усилению межатомных связей, уменьшает диффузионную подвижность вакансий и тем самым замедляет диффузионную ползучесть. Сильные карбидообразователи — хром, молибден, титан, ниобий — связывают углерод в прочные карбиды, затрудняют его диффузию и способствуют получению стабильной структуры. Вследствие искажений кристаллической решетки в районе дислокаций последние очень активно притягивают атомы примесей. Вокруг дислокаций особенно легко концентрируются атомы элементов, образующих растворы внедрения,— углерода, азота, бора и др. Поэтому дислокации часто оказываются местами зарождения частиц второй фазы. [c.83]
Термической обработкой можно изменить структуру только тех металлов, которые обладают полиморфизмом. Поли.морфизм появляется в существовании у металла двух или более кристаллических форм и модификаций, устойчивых в определенном интервале температур. Наряду с железом полиморфные модификации имеют олово, кобальт, титан, марганец, кальций и другие. металлы.
[c.26]
Поли.морфизм появляется в существовании у металла двух или более кристаллических форм и модификаций, устойчивых в определенном интервале температур. Наряду с железом полиморфные модификации имеют олово, кобальт, титан, марганец, кальций и другие. металлы.
[c.26]
Многочисленные опыты подтверждают зависимость диффузии по границам зерен от состава приграничных участков. В серии металлографических исследований (Архаров) показано, что ванадий, титан, ниобий, молибден и бор задерживают диффузию никеля по границам зерен железа, а сурьма ускоряет подвижность атомов серебра вдоль границ меди. Это объяснено сильным разрыхлением кристаллической решетки меди вследствие большого различия кристаллографических структур сурьмы и меди. Подобно сурьме, железо ускоряет диффузию серебра в меди. Характерно, что отмеченное влияние сурьмы наблюдается только при малом содержании примеси. При более высоком содержании она располагается не только по границам, но и во всем объеме зерен, и диффузия серебра также идет в объеме зерна.
 [c.120]
[c.120]В твердом состоянии все металлы имеют кристаллическое строение. Объемноцентрированную кубическую решетку имеют а-железо, хром, молибден, вольфрам гранецентрированную кубическую решетку имеют у-железо, алюминий, никель, медь, свинец, платина гексагональную — цинк, бериллий, магний, титан. Другие металлы, например олово, марганец, висмут, имеют более сложную кристаллографическую структуру. [c.8]
При обычных температурах толщина окисных пленок составляет от 10—20 до 80—100 А. Эти пленки не всегда имеют кристаллическое строение. Часто они близки к аморфному, чему еще способствуют внутренние напряжения, возникающие при образовании фазовых окислов на сравнительно жесткой основе, которой является металл. Для таких металлов, как железо, алюминий, титан и др., определена структура окисных пленок с помощью электронографического метода. [c.26]
Сплавы ВТ5, ВТ5-1, ВТ4, 0Т4 и ВТЮ При комнатной температуре сохраняют кристаллическую решетку, присущую модификации а-титана.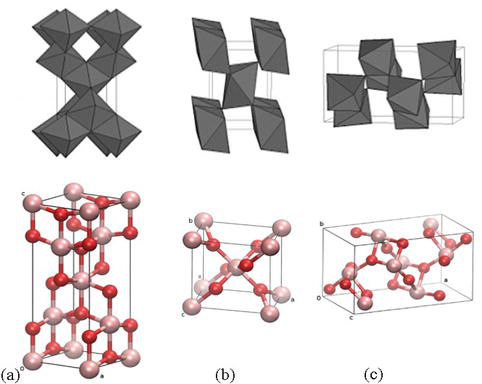 В большинстве случаев эти сплавы применяют в отожженном состоянии. Температура их отжига выше температуры отжига технического титана. В качестве сплава с а-структурой можно рассматривать и технический титан (ВТ1-00, ВТ -О, ВТЫ. ВТ1-2).
[c.388]
В большинстве случаев эти сплавы применяют в отожженном состоянии. Температура их отжига выше температуры отжига технического титана. В качестве сплава с а-структурой можно рассматривать и технический титан (ВТ1-00, ВТ -О, ВТЫ. ВТ1-2).
[c.388]
Титан, как и железо, имеет две кристаллические модификации, что создает благоприятные условия для различного рода фазовых превращений в твердом состоянии и изменений в широком диапазоне структуры и свойств. [c.31]
Многие синие керамические пигменты имеют основную структуру шпинели, представляя собой смешанные оксиды кобальта и алюминия. Коричневые керамические пигменты имеют структуру рутила с титаном, хромом и сурьмой. Хорошо известные титанаты никеля имеют рутильную структуру с никелем и сурьмой в кристаллической решетке они окрашены в желтый цвет. [c.90]
Кристаллическая структура. Титан является полиморфным металлом и существует в двух аллотропических модификациях, различающихся по структуре атомной решепш.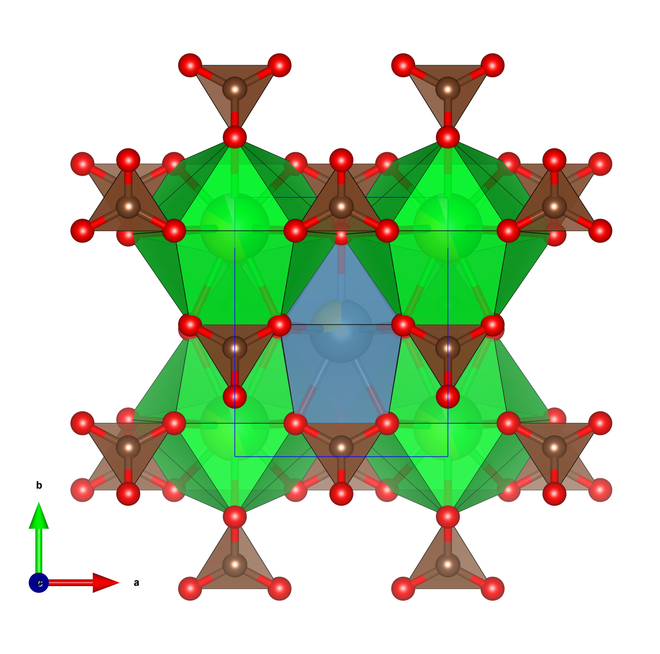 Ниже температуры полиморфного превращения 882,5° С титан существует в виде модификации а, имеющей гексагональную плотноупакован-ную решетку, а выше этой температуры — в виде модификации р с кубической объемноцентрированной решеткой.
[c.356]
Ниже температуры полиморфного превращения 882,5° С титан существует в виде модификации а, имеющей гексагональную плотноупакован-ную решетку, а выше этой температуры — в виде модификации р с кубической объемноцентрированной решеткой.
[c.356]
При питтинговой коррозии основное коррозионное разрушение локализуется на отдельных небольших участках металла (магний, алюминий, железо, никель, титан и др.) и протекает с большой скоростью, что может приводить к сквозной точечной коррозии металла. Питтинговая коррозия наблюдается, обычно, когда основной металл находится в пассивном состоянии. Ионы-активаторы (СГ, Вг , I») адсорбируются в основном на участках поверхности, где плеяка оксида несовершенна (металлические или неметаллические включения, искажающие или нарушающие кристаллическую структуру оксида) [22]. Анионы частично замещают кислород в оксиде и образуют хорошо растворимые поверхностные комплексные ионы. Пассивная пленка нарушается, и металл начинает непосредственно контактировать с раствором. Потенциал металла на этих участках имеет более отрицательное значение, чем потенциал основного металла, покрытого оксидной пленкой, что приводит к возникновению локальных токов. Если пассивная пленка не обладает большим омическим сопротивлением, то система заполяризовывается и на участках питтингооб-разования в основном протекает интенсивно анодный процесс, а катодный процесс восстановления окислителя идет на пассивной поверхности металла. При этом миграция анионов-активаторов идет в основном к участкам питтингообразования.
[c.38]
Потенциал металла на этих участках имеет более отрицательное значение, чем потенциал основного металла, покрытого оксидной пленкой, что приводит к возникновению локальных токов. Если пассивная пленка не обладает большим омическим сопротивлением, то система заполяризовывается и на участках питтингооб-разования в основном протекает интенсивно анодный процесс, а катодный процесс восстановления окислителя идет на пассивной поверхности металла. При этом миграция анионов-активаторов идет в основном к участкам питтингообразования.
[c.38]
Диаграмма состояния системы титан — осмий построена нами впервые [5] (рис. 2). В литературе было известно соединение TiOs с кристаллической структурой типа s l [18, 20]. [c.178]
Таким образом, все металлы VHI группы образуют с титаном фазы на основе эквиатомных соединений с кристаллической структурой типа s l. Эта структура в системах с железом, рутением, осмием и кобальтом устойчива вплоть до комнатной температуры во всей области гомогенности этих фаз.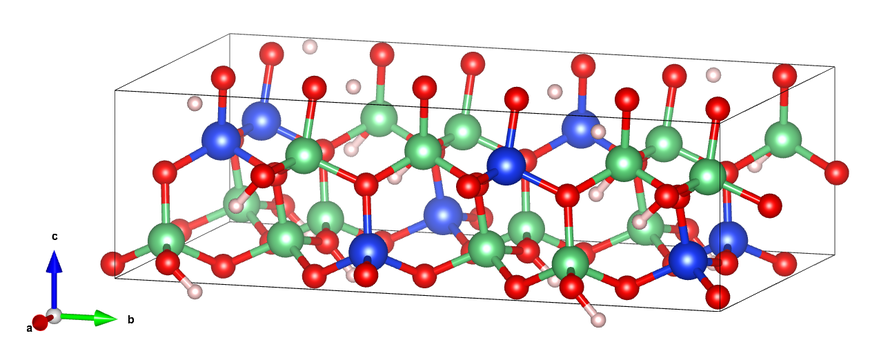 В системах с родием и иридием существует узкий интервал ее устойчивого состояния при сравнительно низких температурах за счет стабилизации избыточным, по сравнению с эквиатомным составом, содержанием титана. В сплавах близких к эквиатомному, а в системах с никелем, палладием и платиной — во всей области гомогенности — с понижением температуры
[c.187]
В системах с родием и иридием существует узкий интервал ее устойчивого состояния при сравнительно низких температурах за счет стабилизации избыточным, по сравнению с эквиатомным составом, содержанием титана. В сплавах близких к эквиатомному, а в системах с никелем, палладием и платиной — во всей области гомогенности — с понижением температуры
[c.187]
Примечания ]. В обозначениях марок сплавов буквы означают Б — ниобий, Д — медь, К — кобальт, Н — никель, С — кремний, Т — титан, Ю — алюминий, А — столбчатую кристаллическую структуру, АА монокристалли-ческую структуру. Цифры означают процентное содержание элемента. [c.27]
Марки сплавов, химический состав тип кристаллической структуры и на личие магнитной анизотропии норми рованы ГОСТ 17809—72 (табл. 22) Названия марок сплавов составлены из условных буквенных обозначений (табл. 23) химических элементов, входящих в сплав (не считая железа). Цифры определяют процентное содержание того элемента, за буквенным обозначением которого они следуют.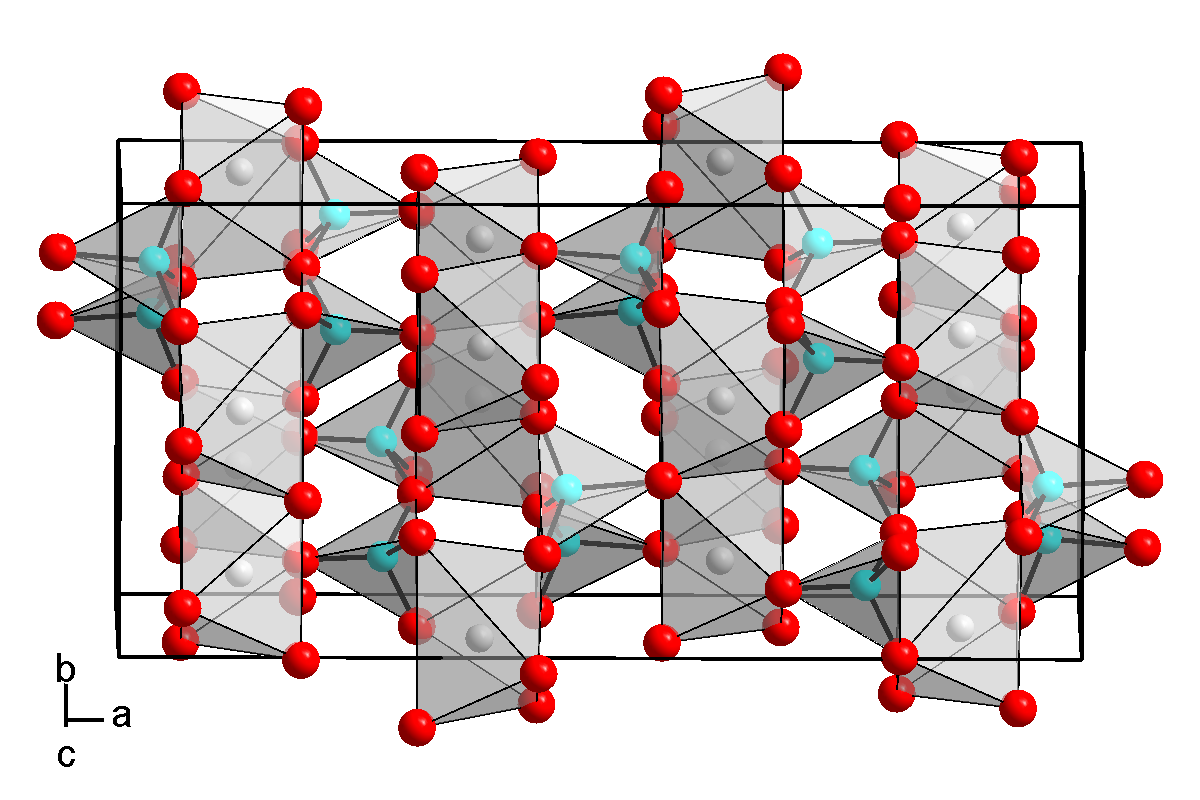 Например, марка ЮНДК35Т5Б означает сплав железа с алюминием, никелем, медью, кобальтом, титаном и ниобием. Процентное содержание кобальта и титана соответственно 35 и 5%. Марка ЮНДК35Т5БА означает сплав железа с алюминием, никелем, медью, кобальтом и ниобием со столбчатой кристаллической структурой, а марка ЮНДК35Т5АА — сплав железа с алюминием, никелем, медью, кобальтом и титаном с моно-кристаллической структурой.
[c.97]
Например, марка ЮНДК35Т5Б означает сплав железа с алюминием, никелем, медью, кобальтом, титаном и ниобием. Процентное содержание кобальта и титана соответственно 35 и 5%. Марка ЮНДК35Т5БА означает сплав железа с алюминием, никелем, медью, кобальтом и ниобием со столбчатой кристаллической структурой, а марка ЮНДК35Т5АА — сплав железа с алюминием, никелем, медью, кобальтом и титаном с моно-кристаллической структурой.
[c.97]
Основными компонентами этих материалов являются железо (до 70%), алюминий (до 14%), никель (до 25%), медь (до 4%), кобальт (до 42%), титан (до 9%). Металлы обозначаются в марках следующими буквами Ю — алюминий, Н — никель, Д — медь, К — кобальт, Т — титан, С — кремний, Б — ниобий. Цифры после букв в обозначении означают содержание металла в %. Кристаллическая структура сплава обозначается буквой А — столбчатая равноосная, АА — монокристаллическая. Например, сплав марки ЮН 14ДК25БА означает, что он содержит алюминий, никель (14%), медь, кобальт (25%), ниобий и имеет столбчатую кристаллическую структуру. [c.146]
[c.146]
Металлы с кристаллической структурой объем-ноцентрированного куба (стали на основе а-железа, вольфрам, хром, молибден и др.), а также некоторые металлы с гексагональной плотноупакованной решеткой (цинк, кадмий, магний) относятся к хладноломким материалам. Чистый титан имеет решетку ГП, но сохраняет пластичность и при низких температурах. Металлы с решеткой гране-центрированного куба (аустенитные стали на основе у-железа, медь, алюминий, никель) не склонны к хладноломкости. [c.20]
Одним из » наиболее перспективных приложений ионной имплантации металлов и сплавов является легирование титана и его сплавов. Отличаясь высокими удельными прочностными характеристиками, титановые сплавы склонны к схватыванию при контактном взаимодействии и имеют низкую износостойкость. Методом ионной имплантации удается значительно повысить фрикционные характеристики титановых сплавов. В отдельных случаях износостойкость возрастает на три порядка [193]. Априори невозможно назвать основной механизм, ответственный за повышение фрикционных характеристик, так как он зависит от состава сплава, типа ионов, параметров имплантации и условий трения. Следует отметить, что, обладая большим сродством к С, N, В, О, титан легко образует соответствующие высокопрочные соединения. Их точная идентификация в поверхностных слоях затруднена изоморфизмом кристаллических структур и возможностью образования оксииитридов, карбонитридов, ок-сикарбидов и т. д.
[c.98]
Априори невозможно назвать основной механизм, ответственный за повышение фрикционных характеристик, так как он зависит от состава сплава, типа ионов, параметров имплантации и условий трения. Следует отметить, что, обладая большим сродством к С, N, В, О, титан легко образует соответствующие высокопрочные соединения. Их точная идентификация в поверхностных слоях затруднена изоморфизмом кристаллических структур и возможностью образования оксииитридов, карбонитридов, ок-сикарбидов и т. д.
[c.98]
С НИМИ. При последующем нагреве происходят сложные процессы диффузии элементов сплава из его внутренних слоев к поверхности через окисную пленку, а также диффузия кислорода через окисную пленку в сплав. При окислении многих металлов превалирует процесс диффузии ионов металла через окисную пленку, в результате чего последняя наращивается на основном металле. В некоторых случаях преобладает процесс диффузии кислорода через окисную пленку внутрь металла, например при окислении титана при высоких температурах. Диффузионные процессы зависят от строения пленки, во многих случаях рыхлой, с незаполненными узлами кристаллической структуры (вакансиями), градиента концентрации легирующих элементов, а также термодинамических условий, способствующих приближению системы к равновесию. С окисленной поверхности чистого металла в глубь него образуются слои окислов с постепенно уменьшающимся содержанием связанного кислорода (РегОз, Рез04, РеО в железе Т10г, Т120з, ТЮ в титане и т. д.). Окисление легированных сплавов происходит более сложным образом.
[c.124]
Диффузионные процессы зависят от строения пленки, во многих случаях рыхлой, с незаполненными узлами кристаллической структуры (вакансиями), градиента концентрации легирующих элементов, а также термодинамических условий, способствующих приближению системы к равновесию. С окисленной поверхности чистого металла в глубь него образуются слои окислов с постепенно уменьшающимся содержанием связанного кислорода (РегОз, Рез04, РеО в железе Т10г, Т120з, ТЮ в титане и т. д.). Окисление легированных сплавов происходит более сложным образом.
[c.124]
Примечание. В обозначениях марок сп.члвов буквы означают Б — ниобий Д — медь К —кобальт Н—никель С — кремний ( силиций ) Т—титан Ю-алюминий А —столбчатая кристаллическая структура АА—монокристаллическая структура. Цифры указывают процентное содержание элемента. [c.321]
Диаграмма состояния. Строение и кристаллическую структуру сплавов иридия с титаном изучали в работах [1—17]. В исследованиях, выполненных методами термического [9, 16], микроструктурного [9, 13—16], рентгеновского [2—16] и дилатометрического [9] анализов, а также определением температур начала плавления [9, 15], микротвердости [13. 15, 16], электросопротивления [9], плотности [14] и сверхпроводимости [8, 17], установлено существование в системе 1г —Т1 химических соединений 1гэТ1 (7.64% Т1), 1гТ1 (19.88% Т1) и 1гТЬ (42,67% Т ). Во всем интервале концентраций система 1г —Ti была изучена в работах [9] и [16], результаты которых приведены соответствеино на рис. 427 [9] и 428 [16].
[c.620]
15, 16], электросопротивления [9], плотности [14] и сверхпроводимости [8, 17], установлено существование в системе 1г —Т1 химических соединений 1гэТ1 (7.64% Т1), 1гТ1 (19.88% Т1) и 1гТЬ (42,67% Т ). Во всем интервале концентраций система 1г —Ti была изучена в работах [9] и [16], результаты которых приведены соответствеино на рис. 427 [9] и 428 [16].
[c.620]
Титан может находиться в виде двух основных стабильных фаз, отличающихся строением кристаллической решетки. При нормальной температуре он существует в виде а-фазы с мелкозернистой структурой, не чувствительной к скорости охлаждения. При температуре выше 882 °С образуется Р-фаза с крупным зерном и высокой чувствительностью к скорости охлаждения. Легирующие элементы и примеси могут стабилизировать а-фазу (алюминий, кислород, азот) или р-фазу (хром, марганец, ванадий). Поэтому сплавы титана условно разделяют на три группы а, а + 3 и 3 сплавы. Первые (ВТ1, ВТ5-1) термически не упрочняются, пластичны, обладают хорошей свариваемостью.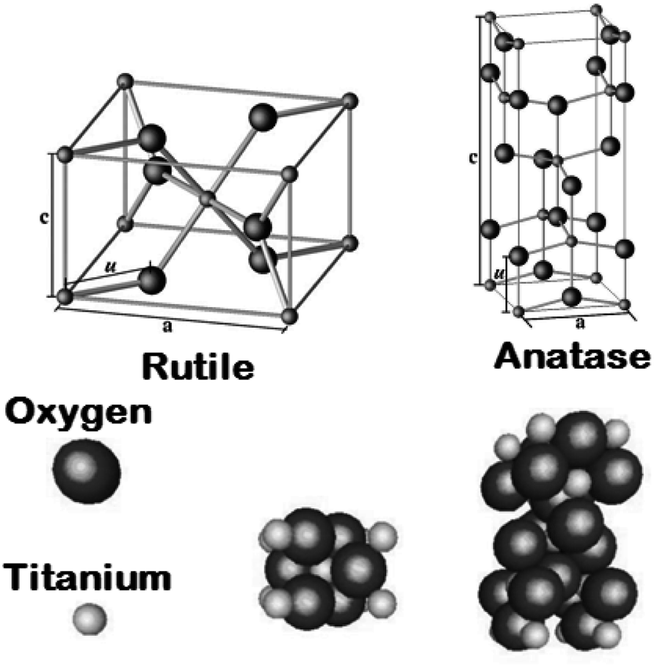 Вторые (ОТ4, ВТЗ, ВТ4, ВТ6, ВТ8) при малых добавках 3-стабилизаторов также свариваются хорошо. Они термически обрабатываются. Сплавы с 3-структурой, например ВТ15, ВТ22, упрочняются термообработкой. Они свариваются хуже, склонны к росту зерен и к холодным трещинам.
[c.199]
Вторые (ОТ4, ВТЗ, ВТ4, ВТ6, ВТ8) при малых добавках 3-стабилизаторов также свариваются хорошо. Они термически обрабатываются. Сплавы с 3-структурой, например ВТ15, ВТ22, упрочняются термообработкой. Они свариваются хуже, склонны к росту зерен и к холодным трещинам.
[c.199]
ИССЛЕДОВАНИЕ СТРУКТУРЫ И СВОЙСТВ КРИСТАЛЛОВ РАФИНИРОВАННОГО ТИТАНА ПОВЫШЕННОЙ ЧИСТОТЫ ПРИ НАГРЕВЕ
УДК 669.295 : 621.762
ИССЛЕДОВАНИЕ СТРУКТУРЫ И СВОЙСТВ КРИСТАЛЛОВ
РАФИНИРОВАННОГО ТИТАНА ПОВЫШЕННОЙ ЧИСТОТЫ ПРИ НАГРЕВЕ
Шаповалова О. М., Бабенко Е. П.
Авторами методом термогравиметрического исследования изучено насыщение
кристаллов титана повышенной чистоты газами при нагреве. Исследована структура
частиц. Изучено влияние примесей внедрения на структуру рафинированного титана при
нагреве.
Общей тенденцией развития цветной металлургии является повышение качества
продукции. Эти исследования направлены на разработку новых технологических процессов
по получению чистых и особо чистых металлов, без которых невозможно развитие
современных отраслей науки и техники. Особую актуальность имеет титан, как металл века
Особую актуальность имеет титан, как металл века
и сплавы на его основе, обладающие уникальными свойствами, которые в первую очередь,
зависят от содержания примесей. Из-за высокой активности металла к газам очень трудная
задача получить титан высокой чистоты. Рафинированный титан повышенной чистоты
представляет интерес как исходный материал для получения сплавов, обладающих
эффектом памяти при нагреве, а также сплавов специального назначения с заданными
свойствами для авиастроения или космической техники. Его получают методом
электролиза, где процесс окисления и восстановления ведут в различных частях аппарата,
что существенно облегчает разделение продуктов электролиза [1]. Кроме того, этот метод
позволяет вести избирательное растворение (окисление) титана на аноде и избирательное его
выделение на катоде, в то время как примеси накапливаются на аноде и в электролите.
Такой металл содержит пониженное количество углерода, кислорода, азота в сравнении с
металлом промышленного электролиза получения титановых порошков или других
существующих способов производства титановых порошков. Поэтому изготовление изделий
с высокой чистотой по примесям, применяемых в авиастроении, является важной задачей.
В таблице 1 представлены сравнительные данные химического анализа титановых
порошков полученных разными способами. Каким бы способом не были получены
титановые порошки, все же они загрязняются примесями, в особенности газовыми [2,3]. Из
всех выпускаемых титановых порошков полупромышленного и промышленного
производства наиболее чистыми являются кристаллы рафинированного титана повышенной
чистоты.
Таблица 1
Содержание газовых примесей в титановых порошках разного производства
Способ производства
титанового порошка
Содержание примесей внедрения, % ∑Cl+Н ∑O+N+C ∑прим.
внедрения
Сl N С Н О
Кристаллы иодидного
титана
0,002 0,005 0,03 0,002 0,010 0,004 0,045 0,049
Электролитическое
рафинирование
0,054 0,012 0,005 0,010
2
0,029 0,064 0,046 0,101
Промышленный
электролиз
0,041 0,017 0,014 0,007
5
0,083 0,0485 0,114 0,162
Восстановление
натрием
0,121 0,010 0,005
6
0,080 0,112 0,201 0,128 0,329
Восстановление
магнием
0,105 0,270 0,085 0,126 0,176 0,231 0,531 0,762
Титан
| Титан | |
|---|---|
| Атомный номер | 22 |
| Внешний вид простого вещества | |
| Свойства атома | |
|
Атомная масса (молярная масса) |
47,88 а. е. м. (г/моль) е. м. (г/моль) |
| Радиус атома | 147 пм |
|
Энергия ионизации (первый электрон) |
657,8(6,82) кДж/моль (эВ) |
| Электронная конфигурация | [Ar] 3d2 4s2 |
| Химические свойства | |
| Ковалентный радиус | 132 пм |
| Радиус иона | (+4e)68 (+2e)94 пм |
|
Электроотрицательность (по Полингу) |
1,54 |
| Электродный потенциал | -1,63 |
| Степени окисления | 4, 3 |
| Термодинамические свойства простого вещества | |
| Плотность | 4,54 г/см? |
| Молярная теплоёмкость | 25,1 Дж/(K·моль) |
| Теплопроводность |
21. 9 Вт/(м·K) 9 Вт/(м·K) |
| Температура плавления | 1933 K |
| Теплота плавления | 18.8 кДж/моль |
| Температура кипения | 3560 K |
| Теплота испарения | 422,6 кДж/моль |
| Молярный объём | 10,6 см3/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки |
гексагональная плотноупакованная (?-Ti) |
| Параметры решётки | a=2,951 с=4,697 (?-Ti) A |
| Отношение c/a | 1,587 |
| Температура Дебая | 380 K |
| Ti | 22 |
| 47,88 | |
| [Ar]3d24s2 | |
| Титан | |
Титан — элемент побочной подгруппы четвёртой группы, четвёртого периода периодической системы химических элементов, с атомным номером 22. Обозначается символом Ti (лат. Titanium). Простое вещество титан (CAS-номер: 7440-32-6) — лёгкий металл серебристо-белого цвета. Существует в двух кристаллических модификациях: ?-Ti с гексагональной плотноупакованной решёткой, -Ti с кубической объёмно-центрированной упаковкой, температура перехода α↔β 883 °C
Обозначается символом Ti (лат. Titanium). Простое вещество титан (CAS-номер: 7440-32-6) — лёгкий металл серебристо-белого цвета. Существует в двух кристаллических модификациях: ?-Ti с гексагональной плотноупакованной решёткой, -Ti с кубической объёмно-центрированной упаковкой, температура перехода α↔β 883 °C
История открытия элемента Титан
Схема атома титана
Открытие TiO2 сделали практически одновременно и независимо друг от друга англичанин У. Грегор и немецкий химик М. Г. Клапрот. У. Грегор, исследуя состав магнитного железистого песка (Крид, Корнуолл, Англия, 1789), выделил новую «землю» (окись) неизвестного металла, которую назвал менакеновой. В 1795 г. немецкий химик Клапрот открыл в минерале рутиле новый элемент и назвал его титаном. Спустя два года Клапрот установил, что рутил и менакеновая земля — окислы одного и того же элемента, за которым и осталось название «титан», предложенное Клапротом. Через 10 лет открытие титана состоялось в третий раз. Французский учёный Л. Воклен обнаружил титан в анатазе и доказал, что рутил и анатаз — идентичные окислы титана.
Французский учёный Л. Воклен обнаружил титан в анатазе и доказал, что рутил и анатаз — идентичные окислы титана.
Первый образец металлического титана получил в 1825 году Й. Я. Берцелиус. Из-за высокой химической активности титана и сложности его очистки чистый образец Ti получили голландцы А. ван Аркел и И. де Бур в 1925 термическим разложением паров иодида титана TiI4.
Происхождение названия
Металл получил своё название в честь титанов, персонажей древнегреческой мифологии, детей Геи. Название элементу дал Мартин Клапрот, в соответствии со своими взглядами на химическую номенклатуру в противоход французской химической школе, где элемент старались называть по его химическим свойствам. Поскольку немецкий исследователь сам отметил невозможность определения свойств нового элемента только по его оксиду, он подобрал для него имя из мифологии, по аналогии с открытым им ранее ураном.
Однако согласно другой версии, публиковавшейся в журнале «Техника-Молодежи» в конце 80-х, новооткрытый металл обязан своим именем не могучим титанам из древнегреческих мифов, а Титании — королеве фей в германской мифологии (жена Оберона в шекспировском «Сне в летнюю ночь»).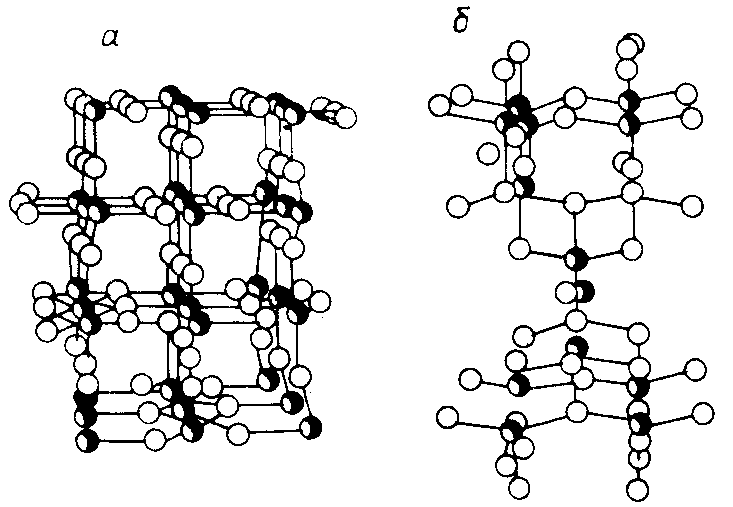 Такое название связано с необычайной «лёгкостью» (малой плотностью) металла.
Такое название связано с необычайной «лёгкостью» (малой плотностью) металла.
Нахождение в природе
Титан находится на 10-м месте по распространённости в природе. Содержание в земной коре 0,57 % по массе. В свободном виде не встречается. Известно более 100 минералов, содержащих титан. Важнейшие из них: рутил TiO2, ильменит FeTiO3, титаномагнетит FeTiO3 + Fe3O4, перовскит CaTiO3, титанит CaTiOSiO4, танталит (Fe,Mn)2+Ta2O6 и манганотанталит MnT2O6. Различают коренные руды титана — ильменит-титаномагнетитовые и россыпные — рутил-ильменит-цирконовые.
Запасы и добыча
Основные руды: ильменит (FeTiO3), рутил (TiO2), титанит (CaTiSiO5).
На 2002 год, 90 % добываемого титана использовалось на производство диоксида титана TiO2. Мировое производство диоксида титана составляло 4,5 млн т.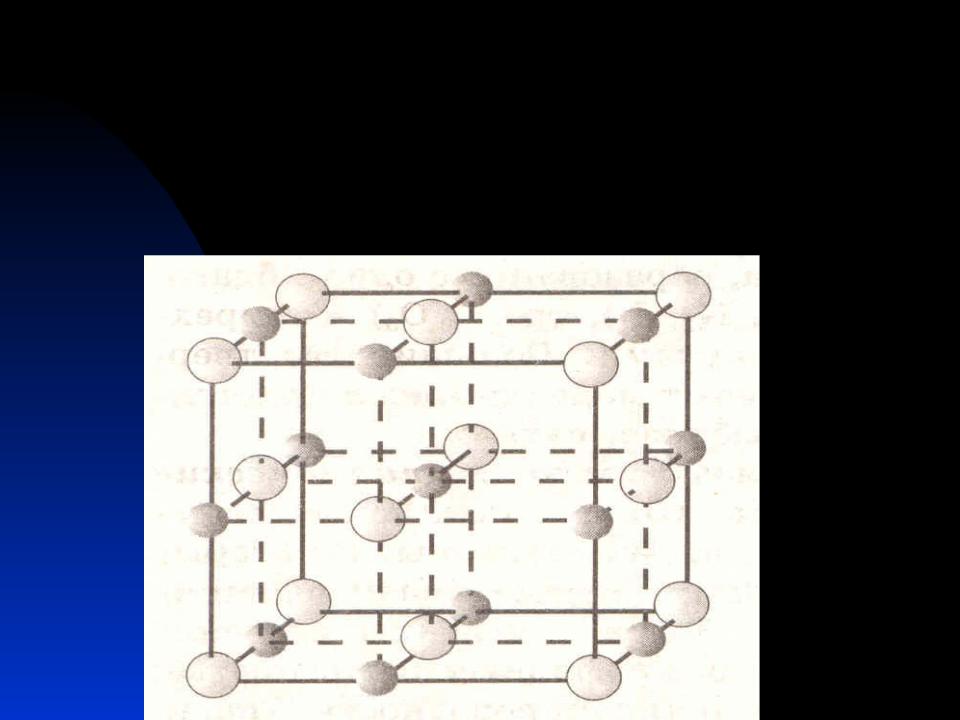 в год. Подтвержденные запасы диоксида титана (без России) составляют около 800 млн т.[2]. На 2006 год, по оценке Геологической службы США, в пересчёте на диоксид титана и без учёта России, запасы ильменитовых руд составляют 603—673 млн т., а рутиловых — 49.7—52.7 млн т. При современных темпах добычи мировых разведанных запасов титана (без учёта России) хватит более чем на 150 лет.
в год. Подтвержденные запасы диоксида титана (без России) составляют около 800 млн т.[2]. На 2006 год, по оценке Геологической службы США, в пересчёте на диоксид титана и без учёта России, запасы ильменитовых руд составляют 603—673 млн т., а рутиловых — 49.7—52.7 млн т. При современных темпах добычи мировых разведанных запасов титана (без учёта России) хватит более чем на 150 лет.
Россия обладает вторыми в мире, после Китая, запасами титана. Минерально-сырьевую базу титана России составляют 20 месторождений (из них 11 коренных и 9 россыпных), достаточно равномерно рассредоточенных по территории страны. Самое крупное из разведанных месторождений находится в 25 км от города Ухта (Республика Коми). Запасы месторождения оцениваются в 2 миллиарда тонн.
Крупнейший в мире производитель титана — российская компания «ВСМПО-АВИСМА».
Получение
Брусок кристаллического титана (чистота 99,995 %, вес ?283 г, длина ?14 см, диаметр ?25 мм), изготовленный на заводе «Уралредмет» иодидным методом ван Аркеля и де Бура
Концентрат титановых руд подвергают сернокислотной или пирометаллургической переработке. Продукт сернокислотной обработки — порошок диоксида титана TiO2. Пирометаллургическим методом руду спекают с коксом и обрабатывают хлором, получая пары тетрахлорида титана TiCl4: TiO2 + 2C + 2Cl2 =TiCl4 + 2CO
Продукт сернокислотной обработки — порошок диоксида титана TiO2. Пирометаллургическим методом руду спекают с коксом и обрабатывают хлором, получая пары тетрахлорида титана TiCl4: TiO2 + 2C + 2Cl2 =TiCl4 + 2CO
Образующиеся пары TiCl4 при 850 °C восстанавливают Mg: TiCl4+ 2Mg = 2MgCl2+ Ti
Полученную титановую «губку» переплавляют и очищают. Ильменитовые концентраты восстанавливают в электродуговых печах с последующим хлорированием возникающих титановых шлаков. Рафинируют титан иодидным способом или электролизом, выделяя Ti из TiCl4. Для получения титановых слитков применяют дуговую, электроннолучевую или плазменную переработку.
Физические свойства
Титан — легкий серебристо-белый металл. Существует в двух кристаллических модификациях: ?-Ti с гексагональной плотноупакованной решёткой (a=2,951 A; с=4,697 A; z=2; пространственная группа C6mmc), ?-Ti с кубической объёмноцентрированной упаковкой (a=3,269 A; z=2; пространственная группа Im3m), температура перехода ?-? 883 °C, ?H перехода 3,8 кДж/моль.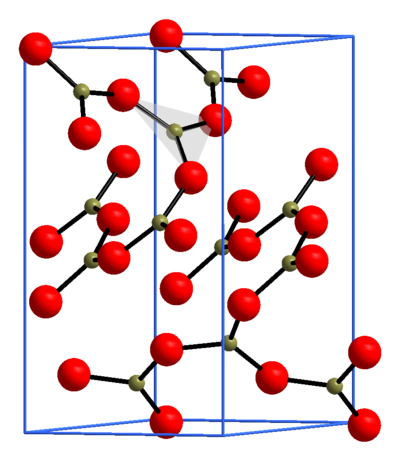 Точка плавления 1671 °C, точка кипения 3260 °C, плотность ?-Ti и ?-Ti соответственно равна 4,505 (20 °C) и 4,32 (900 °C) г/см?, атомная плотность 5,71×1022 ат/см³. Пластичен, сваривается в инертной атмосфере.
Точка плавления 1671 °C, точка кипения 3260 °C, плотность ?-Ti и ?-Ti соответственно равна 4,505 (20 °C) и 4,32 (900 °C) г/см?, атомная плотность 5,71×1022 ат/см³. Пластичен, сваривается в инертной атмосфере.
Имеет высокую вязкость, при механической обработке склонен к налипанию на режущий инструмент, и поэтому требуется нанесение специальных покрытий на инструмент, различных смазок.
При обычной температуре покрывается защитной пассивирующей пленкой оксида TiO2, благодаря этому коррозионностоек в большинстве сред (кроме щелочной).
Титановая пыль имеет свойство взрываться. Температура вспышки 400°С.
Химические свойства
Устойчив к коррозии благодаря оксидной плёнке, но при измельчении в порошок горит на воздухе.
Титан устойчив к разбавленным растворам многих кислот и щелочей (кроме HF,H3PO4 и концентрированной H2SO4).
Легко реагирует даже со слабыми кислотами в присутствии комплексообразователей, например, с плавиковой кислотой HF он взаимодействует благодаря образованию комплексного аниона [TiF6]2-.
При нагревании на воздухе до 1200°C Ti загорается с образованием оксидных фаз переменного состава TiOx. Из растворов солей титана осаждается гидроксид TiO(OH)2·xH2O, осторожным прокаливанием которого получают оксид TiO2. Гидроксид TiO(OH)2·xH2O и диоксид TiO2амфотерны.
TiO2 взаимодействует с серной кислотой при длительном кипячении. При сплавлении с содой Na2CO3 или поташом K2CO3 оксид TiO2 образует титанат: TiO2+K2CO3=K2TiO3+CO2.
При нагревании Ti взаимодействует с галогенами. Тетрахлорид титана TiCl4 при обычных условиях — желтоватая, сильно дымящая на воздухе жидкость, что объясняется сильным гидролизом TiCl4 содержащимися в воздухе парами воды и образованием мельчайших капелек HCl и взвеси гидроксида титана.
Восстановлением TiCl4водородом, Al, Si, другими сильными восстановителями, получен трихлорид и дихлорид титана TiCl3 и TiCl2 — твердые вещества с сильно восстановительными свойствами. Ti взаимодействует с Br2 и I2.
Ti взаимодействует с Br2 и I2.
С N2 выше 400 °C титан образует нитрид TiNx(x=0,58-1,00). При взаимодействии титана с C образуется карбид титана TiCx (x=0,49-1,00).
При нагревании Ti поглощает H2 с образованием соединения переменного состава TiHх (x=1,0). При нагревании эти гидриды разлагаются с выделением H2. Титан образует сплавы со многими металлами.
Применение
Часы из титанового сплаваВ виде сплавов
- Металл применяется в химической промышленности (реакторы, трубопроводы, насосы), лёгких сплавах, остеопротезах. Является важнейшим конструкционным материалом в авиа-, ракето-, кораблестроении.
- Используется в художественном литье[5]
- Титан является легирующей добавкой в некоторых марках стали.
-
Нитинол (никель-титан) — сплав, обладающий памятью формы, применяемый в медицине и технике.

- Алюминиды титана являются очень стойкими к окислению и жаропрочными, что в свою очередь определило их использование в авиации и автомобилестроении в качестве конструкционных материалов.
В виде соединений
- Белый диоксид титана (TiO2) используется в красках (например, титановые белила), а также при производстве бумаги и пластика. Пищевая добавка E171.
- Титанорганические соединения (напр. тетрабутоксититан) применяются в качестве катализатора и отвердителя в химической и лакокрасочной промышленности.
- Неорганические соединения титана применяются в химической электронной, стекловолоконной промышленности в качестве добавки или покрытий.
- Диборид титана — важный компонент сверхтвердых материалов для обработки металлов.
- Нитрид титана применяется для покрытия инструментов.
-
Титанат бария BaTiO3, титанат свинца PbTiO3 и ряд других титанатов —- сегнетоэлектрики.

Анализ рынков потребления
В 2005 компания Titanium Corporation опубликовала следующую оценку потребления титана в мире:
60 % — краска;
20 % — пластик;
13 % — бумага;
7 % — машиностроение.
Цены
15-25 $ за килограмм, в зависимости от чистоты.
Чистота и марка чернового титана (титановой губки) обычно определяется по степени её пластичности.
Физиологическое действие
Нитрид титана
Соединения титана
Химики впервые синтезировали полупроводящий нитрид титана
Venkata S. Bhadram et al./ Physical Review Materials, 2018
Американские химики впервые получили нитрид титана состава Ti3N4.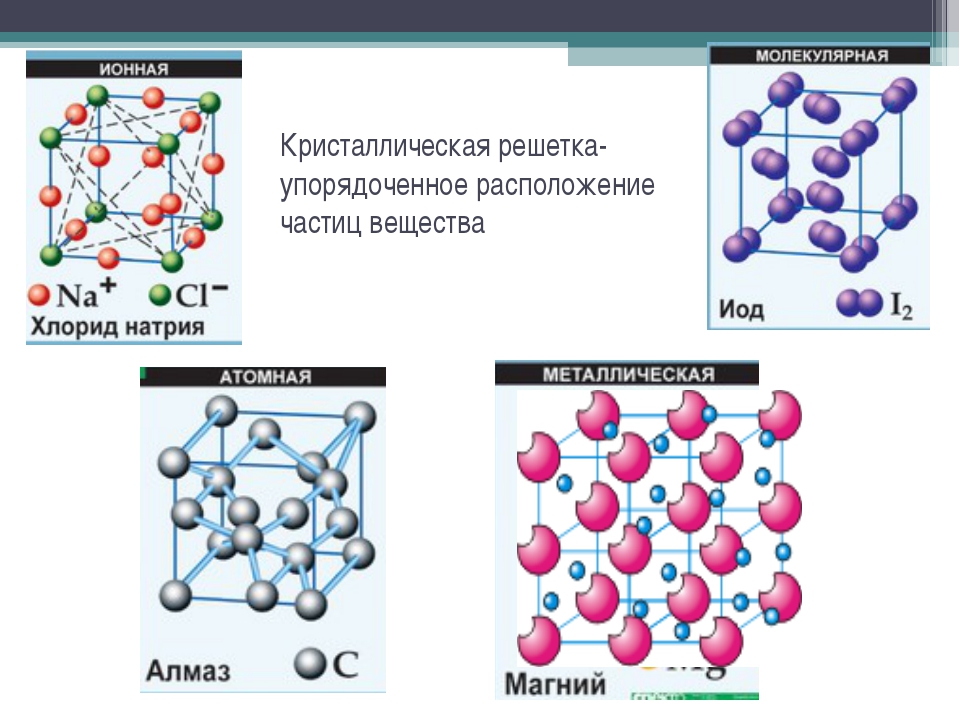 Полученное соединение имеет кубическую симметрию и обладает полупроводниковыми свойствами. Получить его удается пока только при очень больших давлениях и температурах выше 2 тысяч градусов Цельсия, пишут ученые в Physical Review Materials.
Полученное соединение имеет кубическую симметрию и обладает полупроводниковыми свойствами. Получить его удается пока только при очень больших давлениях и температурах выше 2 тысяч градусов Цельсия, пишут ученые в Physical Review Materials.
Наиболее устойчивый нитрид титана имеет состав TiN и обладает кристаллической решеткой со структурой NaCl, в которой атомы титана и азота чередуются в узлах кубической сетки. Такое соединение (как и другие мононитриды элементов той же группы: гафния и циркония) известны своей твердостью, очень высокой температурой плавления и химической инертностью. Предполагалось, что, как гафний и цирконий, титан может образовывать с азотом бинарные соединения с другим стехиометрических составом, в котором на три атома титана приходится четыре атома азота, однако получить и описать такое вещество до настоящего времени не удавалось. Недавно химикам удалось синтезировать метастабильную фазу пернитрида титана TiN2, но все попытки синтезировать нитрид титана со стехиометрическим соотношением 3/4 до настоящего дня заканчивались неудачно.
Впервые получить нитрид титана состава Ti3N4 удалось американским ученым под руководством Тимоти Стробела (Timothy A. Strobel) из Института Карнеги в Вашингтоне. Для этого химики использовали ячейки с алмазными наковальнями с лазерным нагреванием. Давление, при котором происходило образование нужной фазы, составляло около 75 гигапаскалей (это в 750 тысяч больше атмосферного давления), а температура — около 2200 градусов Цельсия. Кристаллическая структура полученного соединения была подтверждена методами рентгено-структурного анализа и рамановской спектроскопии.
Кристаллическая структура полученного нитрида титана. Серыми шариками обозначены атомы титана, синими — атомы азота
Venkata S. Bhadram et al./ Physical Review Materials, 2018
Оказалось, что полученный кристалл имеет структуру типа тетрафосфида тритория Th3P4 c кубической симметрией, в которой атом азота находится в октаэдрическом окружении атомов титана, а титан в свою очередь окружен восемью атомами азота.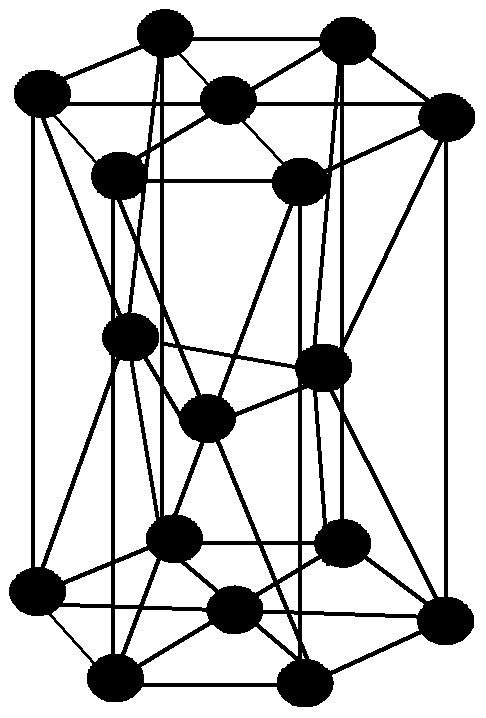 Как и предполагалось, полученное вещество обладает полупроводниковыми свойствами. При этом ширина запрещенной зоны в нем оказалась больше, чем предполагалось по предварительным оценкам, и составила около 0,8 — 0,9 электронвольт.
Как и предполагалось, полученное вещество обладает полупроводниковыми свойствами. При этом ширина запрещенной зоны в нем оказалась больше, чем предполагалось по предварительным оценкам, и составила около 0,8 — 0,9 электронвольт.При снижении давления полученная кристаллическая фаза довольно долго остается устойчивой. Однако при внешнем давлении около 5 гигапаскалей кристалл начинает разлагаться на азот и мононитрид титана. Все термодинамические и электронные свойства полученного вещества были также подтверждены теоретическими оценками с использованием теории функционала плотности. Расчеты показали, что при атмосферном давлении может быть устойчива другая фаза нитрида титана Ti3N4, которая тоже обладает полупроводниковыми свойствами, но имеет моноклинную симметрию.
По словам ученых, полученное соединение — первый пример нитрида титана с полупроводниковыми свойствами. За счет сочетания механических и электрических свойств такой материал может быть весьма перспективным для различных оптоэлектрических приложений, если удастся сделать его устойчивым при атмосферном давлении.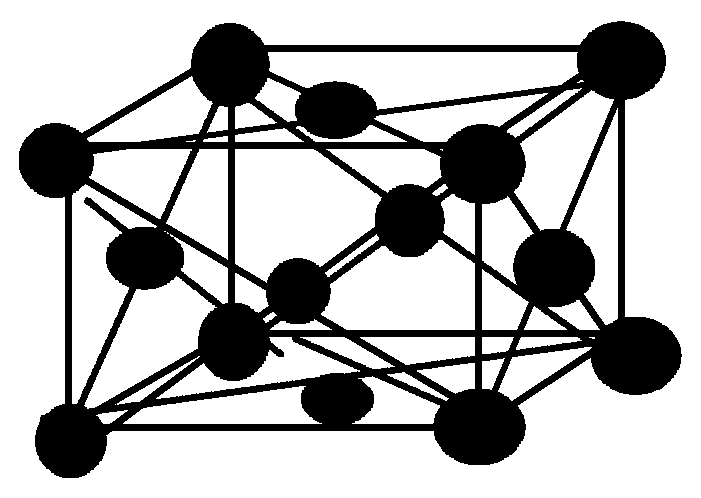
Многие материалы на основе нитридов элементов группы титана весьма интересны с точки зрения их механических и физических свойств. Так, по теоретическими оценкам соединению на основе нитрида гафния принадлежит рекорд тугоплавкости. А нитрид титана состава TiN обладает еще и прекрасными адгезионными свойствами, что позволяет использовать его для увеличения адгезии клеток к пластинам, используемым в «заплатках» на сердце.
Александр Дубов
Структура и фазовый состав продуктов СВС в порошковых смесях титана, углерода и алюминия | Прибытков
1. Yang Chen, Jin Songzhe, Liang Baoyan, Liu Guojun, Duan Lianfeng, Jia Shusheng. Synthesis of Ti3AlC2 by spark plasma sintering of mechanically milled 3Ti/xAl/2C powder mixtures. J. Alloys and Compd. 2009. Vol. 472. P. 79—83.
J. Alloys and Compd. 2009. Vol. 472. P. 79—83.
2. Zhou Aiguo, Wang Chang-an, Ge Zhenbin, Wu Lifeng. Preparation of Ti3AlC2 and Ti2AlC by self-propagating hightemperature synthesis. J. Mater. Sci. Lett. 2001. Vol. 20. P. 1971—1973
3. Birol Yucel. Grain refining efficiency of Al—Ti—C alloys. J. Alloys and Compd. 2006. Vol. 422. P.128—131.
4. Ding Haimin, Liu Xiangfa, Yu Lina, Zhao Guoqun. The influence of forming processes on the distribution and morphologies of TiC in Al—Ti—C master alloys. Scripta Mater. 2007. Vol. 57. P. 575—578.
5. Gezer Berke Turgay, Toptan Fatih, Daglilar Sibel, Kerti Isil. Production of Al—Ti—C grain refiners with the addition of elemental carbon. Mater. Design. 2010. Vol. 31. Р. 30—35.
Design. 2010. Vol. 31. Р. 30—35.
6. Nie Jinfeng, Ma Xiaoguang, Li Pengting, Liu Xiangfa. Effect of B/C ratio on the microstructure and grain refining efficiency of Al—Ti—C—B master alloy. J. Alloys and Compd. 2011. Vol. 509. P. 1119—1123.
7. Wang Enzhao, Gao Tong, Nie Jinfeng, Liu Xiangfa. Grain refinement limit and mechanical properties of 6063 alloy inoculated by Al—Ti—C (B) master alloys. J. Alloys and Compd. 2014. Vol. 594. P. 7—11.
8. Liu Xiaoteng, Hao Hai. The influence of carbon content on Al—Ti—C master alloy prepared by the self-propagating high-temperature synthesis in melt method and its refining effect on AZ31 alloy. J. Alloys and Compd. 2015. Vol. 623. P. 266—273.
9. Yang Huabing, Gao Tong, Wang Haichao, Nie Jinfeng, Liu Xiangfa. Influence of C/Ti stoichiometry in TiCx on the grain refinement efficiency of Al—Ti—C master alloy. J. Mater. Sci. Technol. 2017. Vol. 33. P. 616—622.
Yang Huabing, Gao Tong, Wang Haichao, Nie Jinfeng, Liu Xiangfa. Influence of C/Ti stoichiometry in TiCx on the grain refinement efficiency of Al—Ti—C master alloy. J. Mater. Sci. Technol. 2017. Vol. 33. P. 616—622.
10. Луц А.Р., Амосов А.П., Ермошкин Анд.А., Ермошкин Ант.А., Никитин К.В., Тимошкин И.Ю. Самораспространяющийся высокотемпературный синтез высокодисперсной фазы карбида титана из смеси порошков в расплаве алюминия. Изв. вузов. Порошк. металлургия и функц. покрытия. 2013. No. 3. С. 28—35. Luts A.R., Amosov A.P., Ermoshkin And. A., Ermoshkin Ant.A., Nikitin K.V., Timoshkin I.Yu. Self propagating high temperature synthesis of highly dispersed titanium carbide phase from powder mixtures in the aluminum melt. Russ. J. Non-Ferr. Met. 2014. Vol. 55. No. 6. P. 606—612.
11. Shahin N., Kazemi Sh., Heidarpour A. Mechanochemical synthesis mechanism of Ti3AlC2 MAX phase from elemental powders of Ti, Al and C. Adv. Powd. Technol. 2016. Vol. 27. P. 1775—1780.
Adv. Powd. Technol. 2016. Vol. 27. P. 1775—1780.
12. Stolin A.M., Vrel D., Galyshev S.N., Hendaoui A., Bazhin P.M., Sytschev A.E. Hot forging of MAX compounds SHS-produced in the Ti—Al—C System. Int. J. of SHS. 2009. Vol. 18. No. 3. P. 194—199.
13. Hendaoui A., Vrel D., Amara A., Langlois P., Andasmas M., Guerioune M. Synthesis of high-purity polycrystalline MAX phases in Ti—Al—C system through mechanically activated self-propagating high-temperature synthesis. J. Eur. Ceram. Soc. 2010. Vol. 30. P. 1049—1057.
14. Zhou Aiguo, Wang Chang-an, Huang Yong. A possible mechanism on synthesis of Ti3AlC2. Mater. Sci. Eng. A. 2003. Vol. 352. No. 1-2. P. 333—339.
15. Hendaoui A., Andasmas M. , Amara A., Benaldjia A., Langlois P., Vrel D. SHS of high-purity MAX compounds in the Ti—Al—C system. Int. J. of SHS. 2008. Vol. 17. No. 2. P. 129—135.
, Amara A., Benaldjia A., Langlois P., Vrel D. SHS of high-purity MAX compounds in the Ti—Al—C system. Int. J. of SHS. 2008. Vol. 17. No. 2. P. 129—135.
16. Potanin A.Yu., Loginov P.A., Levashov E.A., Pogozhev Yu.S., Patsera E.I., Kochetov N.A. Effect of mechanical activation on Ti3AlC2 MAX phase formation under self-propagating high-temperature synthesis. Eur. Chem.-Technol. J. 2015. Vol. 17. P. 233—242.
17. Tzenov N.V., Barsoum M.W. Synthesis and Characterization of Ti3AlC2. J. Amer. Ceram. Soc. 2000. Vol. 83(4). P. 825—832.
18. Yoshida Michiyuki, Hoshiyama Yasuhiro, Ommyoji Junji, Yamaguchi Akira. Microstructural evolution during the formation of Ti3AlC2. Mater. Sci. Eng. B. 2010. Vol. 173. No. 1-3. P. 126—129.
19. Liu Zhiwei, Rakita Milan, Xu Wilson, Wang Xiaoming, Han Qingyou. Ultrasound assisted combustion synthesis of TiC in Al—Ti—C system. Ultrasonics Sonochemistry. 2015. Vol. 27. P. 631—637.
Liu Zhiwei, Rakita Milan, Xu Wilson, Wang Xiaoming, Han Qingyou. Ultrasound assisted combustion synthesis of TiC in Al—Ti—C system. Ultrasonics Sonochemistry. 2015. Vol. 27. P. 631—637.
20. Chaubey A.K., Prashanth K.G., Ray N., Wang Zhi. Study on in-situ synthesis of Al—TiC composite by self propagating high temperature synthesis process. Mater. Sci. 2015. Vol. 12. No. 12. P. 454—461.
21. Li Y.X., Hu J.D., Liu Y.H., Yang Y., Guo Z.X. Effect of C/Ti ratio on the laser ignited self-propagating high-temperature synthesis reaction of Al—Ti—C system for fabricating TiC/Al composites. Mater. Lett. 2007. Vol. 61. P. 4366—4369.
22. Song M.S., Huang B., Huo Y.Q., Zhang S.G., Zhang M.X., Hu Q.D., Li J.G. Growth of TiC octahedron obtained by self-propagating reaction.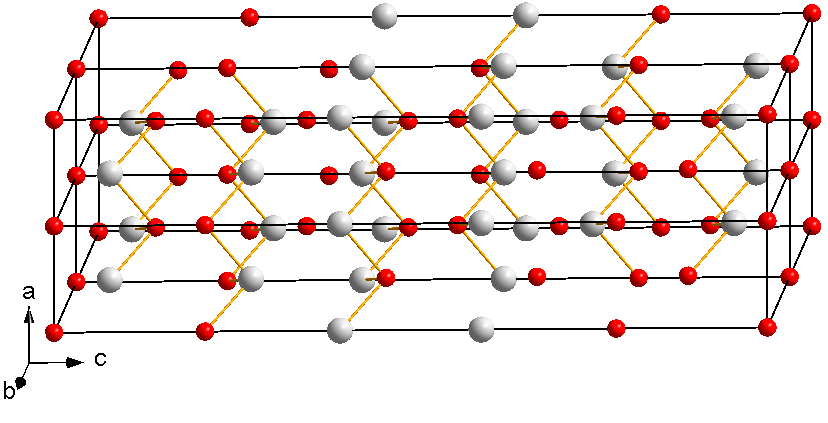 J. Crystal Growth. 2009. Vol. 311. P. 378—382.
J. Crystal Growth. 2009. Vol. 311. P. 378—382.
23. Li Y.X., Hu J.D., Liu S.Y., Wang H.Y., Yang Y., Guo Z.X. Laser igniting synthesis of powders with Al, Ti and C powders. J. Laser Appl. 2006. Vol. 18. No. 2. P. 113—116.
24. Song M.S., Huang B., Zhang M.X., Li J.G. Study of formation behavior of TiC ceramic obtained by self-propagating high-temperature synthesis from Al—Ti—C elemental powders. Int. J. Refract. Met. Hard Mater. 2009. Vol. 27. P. 584—589.
25. Li Y.X., Hu J.D., Wang H.Y., Guo Z.X., Chumakov A.N. Thermodynamic and lattice parameter calculation of TiCx produced from Al—Ti—C powders by laser igniting self-propagating high-temperature synthesis. Mater. Sci. Eng. A. 2007. Vol. 458. P. 235—239.
26. Прибытков Г.А., Криницын М.Г., Коржова В.В. Исследование продуктов СВ-синтеза в порошковых смесях титана и углерода, содержащих избыток титана. Перспективные материалы. 2016. No. 5. C. 59—68. Pribytkov G.A., Krinitsyn M.G., Korzhova V.V. Investigation of products of SHS in powder mixtures of titanium and carbon containing an excess of titanium. Perspektivnye materialy. 2016. No. 5. P. 59—68 (in Russ.).
Прибытков Г.А., Криницын М.Г., Коржова В.В. Исследование продуктов СВ-синтеза в порошковых смесях титана и углерода, содержащих избыток титана. Перспективные материалы. 2016. No. 5. C. 59—68. Pribytkov G.A., Krinitsyn M.G., Korzhova V.V. Investigation of products of SHS in powder mixtures of titanium and carbon containing an excess of titanium. Perspektivnye materialy. 2016. No. 5. P. 59—68 (in Russ.).
27. Прибытков Г.А., Коржова В.В., Барановский А.В., Криницын М.Г. Фазовый состав и структура композиционных порошков карбида титана со связкой из стали Р6М5, полученных методом СВС. Изв. вузов. Порошк. металлургия и функц. покрытия. 2017. No. 2. C. 64—71. Pribytkov G.A., Korzhova V.V., Baranovskiy A.V., Krinitsyn M.G. Phase composition and structure of composite powders of titanium carbide with a bundle of P6M5 steel obtained by the SHS method. Izv. vuzov. Poroshk. metallurgiya i funkts. pokrytiya. 2017. No. 2. P. 64—71 (In Russ.).
P. 64—71 (In Russ.).
28. Прибытков Г.А., Криницын М.Г., Фирсина И.А., Дураков В.Г. Твердость и абразивная износостойкость электронно-лучевых покрытий «карбид титана — титановая связка», наплавленных синтезированными композиционными порошками. Вопросы материаловедения. 2017. No. 4. C. 52—61. Pribytkov G.A., Krinitsyn M.G., Firsina I.A., Durakov V.G. Hardness and abrasive wear resistance of electronbeam coatings «titanium carbide — titanium binder», cladded with synthesized composite powders. Voprosy materialovedeniya. 2017. No. 4. P. 52—61 (In Russ.).
29. Pribytkov G.A., Kalita V.I., Komlev D.I., Korzhova V.V., Radyuk A.A., Baranovsky A.V., Ivannikov A.Yu., Krinitcyn M.G., Mikhailova A.B. Structure and wear resistance of plasma coatings sputtered using TiC + HSS binder composite powder. Inorg. Mater.: Appl. Res. 2018. Vol. 9. No.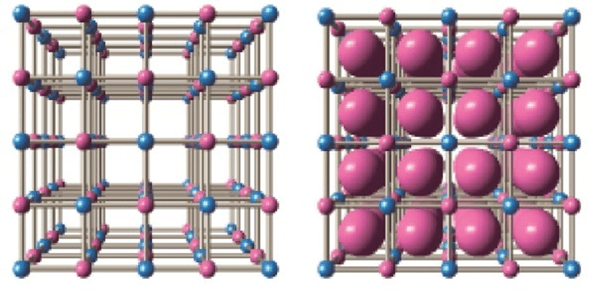 3. P. 442—450.
3. P. 442—450.
30. Прибытков Г.А., Барановский А.В., Фирсина И.А., Дураков В.Г., Криницын М.Г. Твердость и абразивная износостойкость электронно-лучевых покрытий, наплавленных СВС композиционными порошками «TiC + сталь Р6М5». Упрочняющие технологии и покрытия. 2017. No. 10. C. 446—452. Pribytkov G.A., Baranovsky A.V., Firsina I.A., Durakov V.G., Krinitsyn M.G. Hardness and abrasive wear resistance of electron beam coatings deposited by SHS composite powders «TiC + steel P6M5». Uprochnyayushchie tekhnologii i pokrytiya. 2017. No. 10. P. 446—452 (In Russ.).
31. Зуев Л.В., Гусев А.И. Влияние нестехиометрии и упорядочения на период базисной структуры кубического карбида титана. Физика твердого тела. 1999. Т. 41. No. 4. C. 1134—1141. Zuev L.V., Gusev A.I. Influence of nonstoichiometry and ordering on the period of the basic structure of cubic titanium carbide.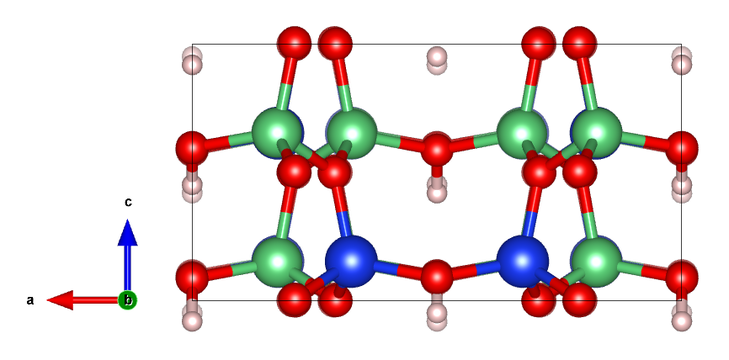 Fizika tverdogo tela. 1999. Vol. 41. No. 4. P. 1134—1141 (In Russ.).
Fizika tverdogo tela. 1999. Vol. 41. No. 4. P. 1134—1141 (In Russ.).
32. Zhang W.N., Wang H.Y., Wang P.J., Zhang J., He L., Jiang Q.C. Effect of Cr content on the SHS reaction of Cr—Ti—C system. J. Alloys and Compd. 2008. Vol. 465. P. 127—131.
33. Рогачев А.С., Мукасьян А.С. Горение для синтеза материалов: введение в структурную макрокинетику. М.: Физматлит, 2012. Rogachev A.S., Mukas’yan A.S. Combustion for the synthesis of materials: an introduction to structural macrokinetics. Mosсow: Fizmatlit, 2012 (In Russ.).
Добавление титана изменило решетку мультиферроика
Исследователи из России, Германии и США выяснили, что добавление титана в гексаферрит бария изменяет кристаллическую решетку материала и позволяет создать особую подструктуру в ней. Результаты работы, опубликованные в журнале Scientific Reports, позволят создать сверхбыструю компьютерную память.
Мультиферроики представляют собой материалы, которые обладают одновременно несколькими упорядочениями. Например, они могут одновременно быть сегнетоэлектриками (ферроэлектриками) и ферромагнетиками. Свойства этих материалов можно изменять направленным образом, благодаря чему они находят применение в технологиях сверхбыстрой магнитной памяти, терагерцовой телекоммуникации или антирадарных покрытиях.
Используя терагерцовую спектроскопию и исследование поглощения и скорости ультразвука, ученые из МФТИ, УрФУ, ЮУрГУ и ФТИ им. А. Ф. Иоффе совместно с зарубежными коллегами смогли провести анализ кристаллической решетки гексаферрита бария с примесью титана. В результате авторы смогли увидеть интересные особенности в поведении материала.
В результате работы исследователи нашли объяснение необычным оптическим и акустическим свойствам материала. Они выяснили, что при добавлении титана в гексаферрите бария меняется структура подрешетки ионов железа. Часть атомов железа под влиянием примеси меняет свою степень окисления и образует подструктуру в основной решетке — так называемую ян-теллеровскую подрешетку.
Это связано с тем, что при добавлении примеси в основную решетку новые атомы встраиваются в структуру, заменяя «старые». Если в гексаферрит бария добавить титан, он начинает занимать место некоторых атомов железа. При этом атомы титана и железа находятся в разных валентных состояниях. «Когда маленький четырехвалентный ион титана замещает трехвалентный ион железа, возникает искажение решетки и нарушается электронейтральность. Электронейтральность должна поддерживаться — это фундаментальное правило. Поэтому часть соседей титана — трехвалентных ионов железа — переходят в двухвалентное состояние, чтобы компенсировать возникший заряд»,— отмечает один из исследователей, заведующий лабораторией терагерцовой спектроскопии МФТИ Борис Горшунов.
«Мы впервые обнаружили новый механизм формирования подрешетки ян-теллеровских центров. В нашем случае ее образуют не атомы примеси, как это обычно происходит, а часть атомов исходного кристалла», — рассказывает другой автор работы, профессор Уральского федерального университета Владимир Гудков.
Подрешетка Яна — Теллера в структуре придает материалу необычные свойства. Она позволяет управлять магнитными подсистемами с помощью электрического поля, например, с помощью терагерцовых волн можно перемагничивать биты сверхбыстрой компьютерной памяти.
Кристаллическая структура титана
Как правило, чистый титан может кристаллизоваться в двух кристаллических структурах : α-титан и β-титан. Когда он кристаллизуется при низких температурах (комнатная температура), образуется гексагональная плотноупакованная (ГПУ) структура альфа-титана. Когда он кристаллизуется при высоких температурах, образуется объемно-центрированная кубическая (ОЦК) структура бета-титана.Полное преобразование одной кристаллической структуры в другую называется аллотропным преобразованием. Температура репродуктивного превращения называется температурой перехода. Титан HCP α стабилен при комнатной / низких температурах, а титан BCC β стабилен при высоких температурах.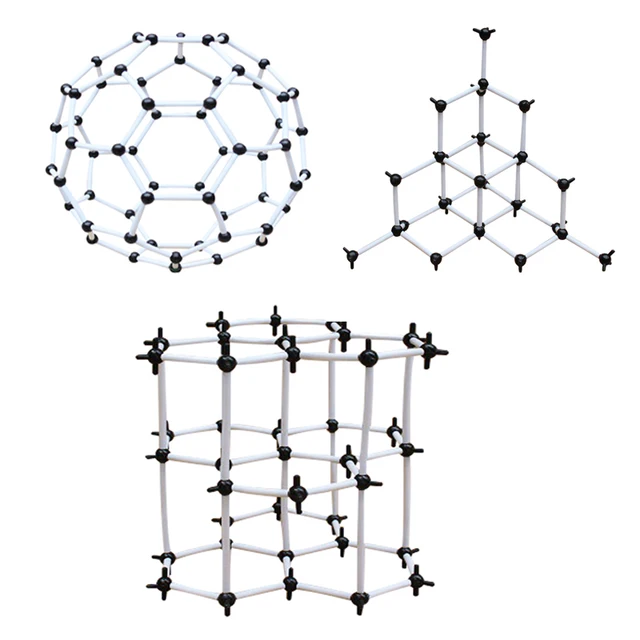 Температура β-перехода для чистого титана составляет 882 ± 2 ° C.
Температура β-перехода для чистого титана составляет 882 ± 2 ° C.
Кристаллическая структура α-титана HCP и β-титана BCC.
Для нелегированного титана , который также известен как коммерчески чистый титан , ASTM Grade 1, 2, 3 и 4, в зависимости от уровня примесей, температуры β-перехода обычно выше, чем у чистого титана.Микроструктура нелегированного титана при комнатной температуре обычно представляет собой 100% альфа-кристаллическую структуру. По мере увеличения количества примесных элементов (в первую очередь железа) металлографически наблюдаются небольшие, но возрастающие количества бета-фазы, обычно на границах альфа-зерен. Отожженный нелегированный титан может иметь равноосную или игольчатую альфа-микроструктуру.
Как схематично показано на рисунке выше:
- Для α-титана постоянные решетки: a = 0,295 нм, c = 0,468 нм; плотно упакованное направление: <1120>; плотно упакованный самолет: {0001}; координационный номер: 12; коэффициент упаковки: 0.
 74; атомов в элементарной ячейке: 6.
74; атомов в элементарной ячейке: 6. - Для β-титана постоянные решетки: a = 0,332 нм; направление плотной упаковки <111>; плотно упакованный самолет: {110}; координационный номер: 8; коэффициент упаковки: 0,68; атомов в элементарной ячейке: 2.
Сопутствующие товары
Гранецентрированный кубический титан — новая кристаллическая структура Ti в сплаве Ti-8Mo-6Fe
Основные характеристики
- •
Микроструктура сплава Ti-8Mo-6Fe, полученного методом порошкового спекания, является ультратонкой.
- •
Обнаружена фаза FCC (Fm-3m) Ti с постоянной решетки 0,431 нм.
- •
Металлические свойства и стабильность FCC Ti были выявлены расчетами из первых принципов.
- •
Периодические дуговые полосы, образованные диффузным рассеянием электронов, были обнаружены на SAED-картинах ОЦК фазы TiMoFe.

Abstract
Микроструктура тройного сплава Ti-8Mo-6Fe с ультрамелкими зернами систематически изучалась с помощью полевого просвечивающего электронного микроскопа Tecnai-G2 F20 и просвечивающего электронного микроскопа JEMS 2010.Обнаружена новая фаза Ti с гранецентрированно-кубической структурой (Fm-3m). Морфология этих фаз ГЦК Ti была эллиптической, и они были широко распределены на границах раздела между полигональными фазами ГЦК TiMoFe. Размер фаз ГЦК Ti концентрировался в диапазоне 200–450 нм. Постоянная решетки ГЦК-фазы Ti составляла 0,431 нм. Для доказательства того, что структура ГЦК в сплаве Ti-8Mo-6Fe действительно является ГЦК TiC, а не ГЦК TiC, TiN и TiO.Расчеты из первых принципов показали металлические свойства и стабильность FCC Ti. Все легирующие элементы Mo и Fe находились в полигональных ОЦК фазах TiMoFe. Полукруглые дуговые периодические полосы, образованные диффузным рассеянием электронов, присутствовали на выбранных диаграммах дифракции электронов (SAED) фазы BCC TiMoFe, которые могут происходить из упорядоченного домена Mo и Fe или локального упорядочения Mo, Fe и Ti.
Ключевые слова
Сплав Ti-8Mo-6Fe
Гранецентрированный кубический
Дифракция электронов в выбранной области
Диффузное рассеяние электронов
Рекомендуемые статьи Цитирующие статьи (0)
Полный текст© 2018 Elsevier B.V. Все права защищены.
Рекомендуемые статьи
Цитирующие статьи
Описание кристаллической структуры титана (а) (ГПУ), (б) …
Контекст 1
… поскольку чистый металл имеет кристалл ГПУ структура (гексагональная закрытая упаковка, -фаза) и ОЦК-кристаллическая структура (кубический центр тела,-фаза). На рисунке 1 представлена иллюстрация кристаллической структуры титана. -Фаза, образованная в чистом Ti, нестабильна при комнатной температуре, за исключением сплавов Ti, таких как сплав Ti-6% Al-6% V….
Context 2
… далее наблюдая за влиянием Nb на образование фазы, образцы нагревают до 1100 ° C с последующим охлаждением на воздухе. На рисунке 10 показано изменение морфологии матрицы. При 2% Nb матрица имеет 1/4 фазы (рис. 10а). …
На рисунке 10 показано изменение морфологии матрицы. При 2% Nb матрица имеет 1/4 фазы (рис. 10а). …
Контекст 3
… 10 показывает изменение морфологии матрицы. При 2% Nb матрица имеет 1/4 фазы (рис. 10а). При 4% Nb матрица по-прежнему представляет собой большую часть фазы (рис. 10b). …
Контекст 4
… 2% Nb, матрица фаза (рис. 10а). При 4% Nb матрица по-прежнему представляет собой большую часть фазы (рис. 10b). -Фаза значительно образуется при содержании 6% Nb (рис. 10с). …
Контекст 5
… 4% Nb, матрица по-прежнему является большей частью фазы (рисунок 10b). -Фаза значительно образуется при содержании 6% Nb (рис. 10с). Тогда ясно, что Nb может действовать как стабилизатор фазы во время термообработки при 1100 o C. …
Контекст 6
… Измерение проводится после ковки, которой предшествовала термообработка при 1000 ° C. Увеличение содержания Mo и Nb до 6% в Ti-6% Al приводит к увеличению твердости (Рисунок 11). Это означает, что содержание Mo и Nb влияет на твердость сплавов Ti-Al-Mo / Nb. …
Это означает, что содержание Mo и Nb влияет на твердость сплавов Ti-Al-Mo / Nb. …
Контекст 7
… означает, что содержание Mo и Nb влияет на твердость сплавов Ti-Al-Mo / Nb. На Рисунке 11 увеличение твердости связано с образованием фазы (Рисунки 8a, 8b, 10a и 10b).При 6% Mo твердость достигает максимального значения 456 HV при прочности 1021 МПа. …
Контекст 8
… означает, что содержание Mo и Nb влияет на твердость сплавов Ti-Al-Mo / Nb. На Рисунке 11 увеличение твердости связано с образованием фазы (Рисунки 8a, 8b, 10a и 10b). При 6% Mo твердость достигает максимального значения 456 HV при прочности 1021 МПа. …
Контекст 9
… Роль содержания Nb преобладает после повторного нагрева при 1100 ° C с последующим охлаждением на воздухе.Твердость и прочность значительно увеличиваются до 642 HV (Рисунок 12) и 1400 МПа соответственно. Это говорит о том, что образование-фазы при комнатной температуре влияет на повышенную твердость и прочность Ti-сплавов. …
…
Контекст 10
… предполагает, что образование фазы при комнатной температуре влияет на повышенную твердость и прочность титановых сплавов. При воздушном охлаждении от 1100 ° C большая часть фазы остается нетрансформированной, так что фаза доминирует в матрице при комнатной температуре (рис. 10c)….
Context 11
… соединение между слоем CaPO 4 и подложкой из сплава происходит из-за очень высокоскоростного горячего распыления CaPO 4 на поверхность сплава. CaPO 4 внедряется в поверхность Ti-сплавов, как показано на рисунке 13. Результат XRD-теста (рисунок 14) показывает, что высокоскоростная жидкость CaPO 4 обладает способностью поглощать воду из воздуха с образованием гидратного соединения. …
Контекст 12
… 4 встраивается в поверхность Ti-сплавов, как показано на рисунке 13.Результат XRD-теста (Рисунок 14) показывает, что высокоскоростная жидкость CaPO 4 обладает способностью поглощать воду из воздуха с образованием гидратного соединения. Кривая с углом при вершине 2 между 30 o -32 o указывает на гидратное соединение гидроксиапатита Ca 5 (PO 4) 3 OH. …
Кривая с углом при вершине 2 между 30 o -32 o указывает на гидратное соединение гидроксиапатита Ca 5 (PO 4) 3 OH. …
Контекст 13
… содержания Mo и Nb в зависимости от скорости коррозии показано на рисунке 15. Увеличение содержания Mo и Nb до 6% снижает скорость коррозии. …
mp-46: Ti (шестиугольный, P6_3 / mmc, 194)
@article {Jain2013,
автор = {Джайн, Анубхав и Онг, Шьюе Пинг и Хотье, Джеффрой и Чен, Вей и Ричардс, Уильям Дэвидсон и Дацек, Стивен и Чолия, Шреяс и Гюнтер, Дэн и Скиннер, Дэвид и Седер, Гербранд и Перссон, Кристин а.},
doi = {10.1063 / 1.4812323},
issn = {2166532X},
journal = {APL Materials},
число = {1},
pages = {011002},
title = {{Комментарий: The Materials Project: подход с использованием генома материалов к ускорению разработки материалов}},
url = {https://doi.org/10.1063/1.4812323},
объем = {1},
год = {2013}
} @article {Pawar1968,
author = «Павар Р. Р. и Дешпанде В. Т.»,
title = «Анизотропия теплового расширения альфа-титана»,
journal = «Acta Crystallographica A (24,1968-38,1982)»,
год = «1968»,
volume = «24»,
pages = «316-317»,
ASTM_id = «ACACBN»
} @article {KurtLejaegher2014,
author = «Лежегере, Курт и Спейбрук, Вероника Ван и Ост, Гвидо Ван и Коттенье, Стефан»,
title = «Оценка ошибок для предсказаний теории функционала плотности твердого тела: обзор с помощью элементарных кристаллов в основном состоянии»,
journal = «Критические обзоры в области твердого тела и материаловедения»,
год = «2014»,
volume = «39»,
pages = «1-24»,
ASTM_id = «CCRSDA»
} @article {Новоселова2004,
author = «Новоселова Т. и Малинов С., Ша В. и Жечева А. »,
title = «Исследование фаз в гамма-сплаве Ti Al методом высокотемпературной синхротронной дифракции рентгеновских лучей»,
journal = «Материаловедение и инженерия A: Структурные матрицы: свойства, микроструктура и обработка»,
год = «2004»,
volume = «371»,
pages = «103-112»,
ASTM_id = «MSAPE3»
} @article {Meschel2011,
author = «Мешель, С.В. и Павлу, Дж. и Нэш, П.»,
title = «Термохимическое поведение некоторых бинарных сплавов с памятью формы с помощью калориметрии прямого высокотемпературного синтеза»,
journal = «Журнал сплавов и соединений»,
год = «2011»,
volume = «509»,
pages = «5256-5262»,
ASTM_id = «JALCEU»
} @article {Kriegel2014,
author = «Кригель, Марио Дж.и Павлючков, Дмитрий и Хмелик, Давид и Фабричная, Ольга и Корниенко, Константин и Хегер, Дитрих и Рафая, Давид и Зейферт, Ганс Дж. «,
title = «Состав поверхностей ликвидуса и солидуса системы Al-Ti-Cr»,
journal = «Журнал сплавов и соединений»,
год = «2014»,
volume = «584»,
pages = «438-446»,
ASTM_id = «JALCEU»
} @article {Bumps1953,
author = «Шишки, Э.
и Малинов С., Ша В. и Жечева А. »,
title = «Исследование фаз в гамма-сплаве Ti Al методом высокотемпературной синхротронной дифракции рентгеновских лучей»,
journal = «Материаловедение и инженерия A: Структурные матрицы: свойства, микроструктура и обработка»,
год = «2004»,
volume = «371»,
pages = «103-112»,
ASTM_id = «MSAPE3»
} @article {Meschel2011,
author = «Мешель, С.В. и Павлу, Дж. и Нэш, П.»,
title = «Термохимическое поведение некоторых бинарных сплавов с памятью формы с помощью калориметрии прямого высокотемпературного синтеза»,
journal = «Журнал сплавов и соединений»,
год = «2011»,
volume = «509»,
pages = «5256-5262»,
ASTM_id = «JALCEU»
} @article {Kriegel2014,
author = «Кригель, Марио Дж.и Павлючков, Дмитрий и Хмелик, Давид и Фабричная, Ольга и Корниенко, Константин и Хегер, Дитрих и Рафая, Давид и Зейферт, Ганс Дж. «,
title = «Состав поверхностей ликвидуса и солидуса системы Al-Ti-Cr»,
journal = «Журнал сплавов и соединений»,
год = «2014»,
volume = «584»,
pages = «438-446»,
ASTM_id = «JALCEU»
} @article {Bumps1953,
author = «Шишки, Э. С. и Кесслер, Х.Д. и Хансен, М.»,
title = «Титано-кислородная система»,
journal = «Сделки Американского общества металлов»,
год = «1953»,
volume = «45»,
pages = «1008-1025»,
ASTM_id = «TASEA7»
} @article {Cadoff1953,
author = «Кадофф, И.и Nielsen, J.P. «,
title = «Фазовая диаграмма титан-углерод»,
journal = «Труды Американского института инженеров горной, металлургической и нефтяной промышленности»,
год = «1953»,
volume = «197»,
pages = «248-252»,
ASTM_id = «TAIMAF»
} @article {Srivastava2011,
author = «Шривастава, А. и Чаухан, М. и Сингх, Р.К.»,
title = «Фазовые переходы, индуцированные давлением в нитридах переходных металлов: исследование ab initio»,
journal = «Physica Status Solidi B — Основы физики твердого тела»,
год = «2011»,
volume = «248»,
pages = «2793-2800»,
ASTM_id = «PSSBBD»
} @article {Нерсесян1984,
author = «Нерсесян, М.Д. «,
title = «Синтез гидридов нитридов титана и циркония в условиях горения»,
journal = «Российский журнал неорганической химии»,
год = «1984»,
volume = «29»,
pages = «495-497»,
ASTM_id = «RJICAQ»
} @article {Holmberg1962,
author = «Холмберг, Б.
С. и Кесслер, Х.Д. и Хансен, М.»,
title = «Титано-кислородная система»,
journal = «Сделки Американского общества металлов»,
год = «1953»,
volume = «45»,
pages = «1008-1025»,
ASTM_id = «TASEA7»
} @article {Cadoff1953,
author = «Кадофф, И.и Nielsen, J.P. «,
title = «Фазовая диаграмма титан-углерод»,
journal = «Труды Американского института инженеров горной, металлургической и нефтяной промышленности»,
год = «1953»,
volume = «197»,
pages = «248-252»,
ASTM_id = «TAIMAF»
} @article {Srivastava2011,
author = «Шривастава, А. и Чаухан, М. и Сингх, Р.К.»,
title = «Фазовые переходы, индуцированные давлением в нитридах переходных металлов: исследование ab initio»,
journal = «Physica Status Solidi B — Основы физики твердого тела»,
год = «2011»,
volume = «248»,
pages = «2793-2800»,
ASTM_id = «PSSBBD»
} @article {Нерсесян1984,
author = «Нерсесян, М.Д. «,
title = «Синтез гидридов нитридов титана и циркония в условиях горения»,
journal = «Российский журнал неорганической химии»,
год = «1984»,
volume = «29»,
pages = «495-497»,
ASTM_id = «RJICAQ»
} @article {Holmberg1962,
author = «Холмберг, Б. «,
title = «Структурные исследования системы титан-азот»,
journal = «Acta Chemica Scandinavica (1-27,1973-42,1988)»,
год = «1962»,
volume = «16»,
pages = «1255-1261»,
ASTM_id = «ACSAA4»
} @article {Rostoker1952,
author = «Ростокер, В.»,
title = «Наблюдение за параметрами решетки альфа и Ti O — фаз в системе Ti — O»,
journal = «Труды Американского института инженеров горной, металлургической и нефтяной промышленности»,
год = «1952»,
volume = «194»,
pages = «981-982»,
ASTM_id = «TAIMAF»
} @article {Spreadborough2959,
author = «Спредборо, Дж. и Кристиан, Дж. У.»,
title = «Измерение размеров решетки и температур Дебая титана и серебра рентгеновскими методами»,
journal = «Труды Физического общества, Лондон»,
год = «1959»,
volume = «74»,
pages = «609-615»,
ASTM_id = «PPSOAU»
} @article {Szanto1955,
author = «Сзанто, И.»,
title = «Об определении параметров решетки альфа-титана высокой чистоты»,
journal = «Acta Technica Academiae Scientarum Hungaricae»,
год = «1955»,
volume = «13»,
pages = «363-372»,
ASTM_id = «ATSHA8»
} @article {Clark1949,
author = «Кларк, H.
«,
title = «Структурные исследования системы титан-азот»,
journal = «Acta Chemica Scandinavica (1-27,1973-42,1988)»,
год = «1962»,
volume = «16»,
pages = «1255-1261»,
ASTM_id = «ACSAA4»
} @article {Rostoker1952,
author = «Ростокер, В.»,
title = «Наблюдение за параметрами решетки альфа и Ti O — фаз в системе Ti — O»,
journal = «Труды Американского института инженеров горной, металлургической и нефтяной промышленности»,
год = «1952»,
volume = «194»,
pages = «981-982»,
ASTM_id = «TAIMAF»
} @article {Spreadborough2959,
author = «Спредборо, Дж. и Кристиан, Дж. У.»,
title = «Измерение размеров решетки и температур Дебая титана и серебра рентгеновскими методами»,
journal = «Труды Физического общества, Лондон»,
год = «1959»,
volume = «74»,
pages = «609-615»,
ASTM_id = «PPSOAU»
} @article {Szanto1955,
author = «Сзанто, И.»,
title = «Об определении параметров решетки альфа-титана высокой чистоты»,
journal = «Acta Technica Academiae Scientarum Hungaricae»,
год = «1955»,
volume = «13»,
pages = «363-372»,
ASTM_id = «ATSHA8»
} @article {Clark1949,
author = «Кларк, H.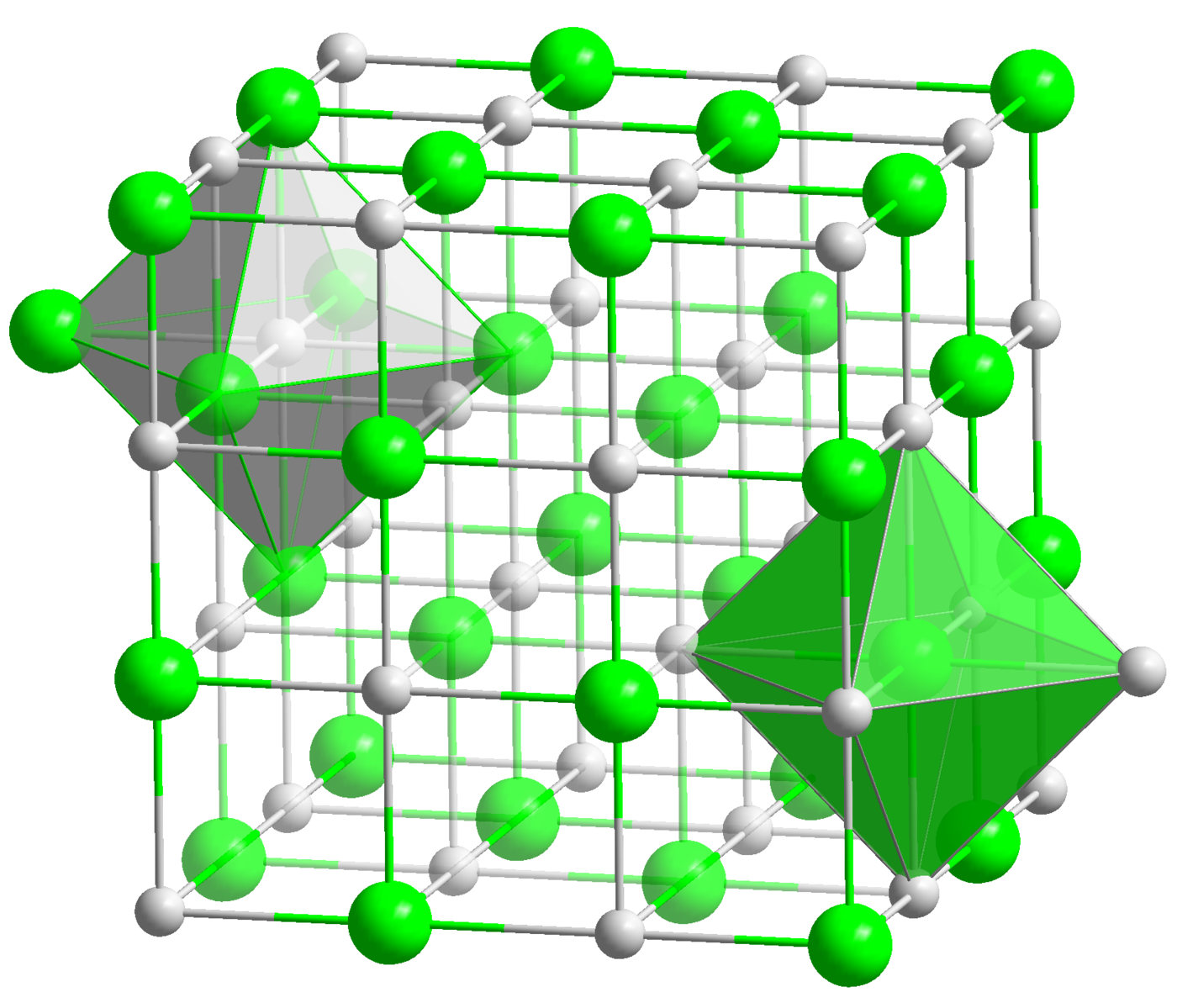 T.»,
title = «Параметры решетки альфа-титана высокой чистоты; и влияние на них кислорода и азота»,
journal = «Журнал металлов»,
год = «1949»,
volume = «1»,
pages = «588-589»,
ASTM_id = «JOMTAA»
} @article {Василевский1961,
author = «Василевский, Р.J. «,
title = «Термическое расширение титана и некоторых титаново-кислородных сплавов»,
journal = «Операции Металлургического общества Эйме»,
год = «1961»,
volume = «221»,
pages = «1231-1235»,
ASTM_id = «TMSAAB»
} @article {Fang2013,
author = «Фанг, Цинсонг и Бай, Вэньцзи и Ян, Цзинсу и Ронг, Хэ и Ши, Ничэн и Ли, Гуову и Сюн, Мин и Ма, Чжешэн»,
title = «Титан, Ti, новый минеральный вид из Луобуши, Тибет, Китай»,
journal = «Acta Geologica Sinica»,
год = «2013»,
volume = «87»,
pages = «1275-1280»,
ASTM_id = «AGSIDP»
} @article {Schuster1980,
author = «Шустер, Дж.К. и Новотны, Х. и Ваккаро, К. «,
title = «Тройные системы: Cr — Al — C, V — Al — C и Ti — Al — C и поведение H-фаз (M2 Al C)»,
journal = «Журнал химии твердого тела»,
год = «1980»,
volume = «32»,
pages = «213-«,
ASTM_id = «JSSCBI»
} @article {Wood1962,
author = «Вуд, Р.
T.»,
title = «Параметры решетки альфа-титана высокой чистоты; и влияние на них кислорода и азота»,
journal = «Журнал металлов»,
год = «1949»,
volume = «1»,
pages = «588-589»,
ASTM_id = «JOMTAA»
} @article {Василевский1961,
author = «Василевский, Р.J. «,
title = «Термическое расширение титана и некоторых титаново-кислородных сплавов»,
journal = «Операции Металлургического общества Эйме»,
год = «1961»,
volume = «221»,
pages = «1231-1235»,
ASTM_id = «TMSAAB»
} @article {Fang2013,
author = «Фанг, Цинсонг и Бай, Вэньцзи и Ян, Цзинсу и Ронг, Хэ и Ши, Ничэн и Ли, Гуову и Сюн, Мин и Ма, Чжешэн»,
title = «Титан, Ti, новый минеральный вид из Луобуши, Тибет, Китай»,
journal = «Acta Geologica Sinica»,
год = «2013»,
volume = «87»,
pages = «1275-1280»,
ASTM_id = «AGSIDP»
} @article {Schuster1980,
author = «Шустер, Дж.К. и Новотны, Х. и Ваккаро, К. «,
title = «Тройные системы: Cr — Al — C, V — Al — C и Ti — Al — C и поведение H-фаз (M2 Al C)»,
journal = «Журнал химии твердого тела»,
год = «1980»,
volume = «32»,
pages = «213-«,
ASTM_id = «JSSCBI»
} @article {Wood1962,
author = «Вуд, Р. М.»,
title = «Константы решетки альфа-титана высокой чистоты»,
journal = «Труды Физического общества, Лондон»,
год = «1962»,
volume = «80»,
pages = «783-786»,
ASTM_id = «PPSOAU»
} @article {Schmitz-Pranghe1968,
author = «Шмитц-Пранге, Н.и Дуэннер, П. «,
title = «Gitterstruktur und thermische Ausdehnung der Uebergangsmetalle Scandium, Titan, Vanadin und Mangan»,
journal = «Zeitschrift fuer Metallkunde»,
год = «1968»,
volume = «59»,
pages = «377-382»,
ASTM_id = «ZEMTAE»
} @article {Hull1921,
author = «Халл, A.W.»,
title = «Кристаллическая структура Ti и Zr»,
journal = «Physical Review (1,1893-132,1963 / 141,1966-188,1969)»,
год = «1921»,
volume = «18»,
pages = «88-89»,
ASTM_id = «PHRVAO»
} @article {Malov1994,
author = «Малов Ю.И., Фокин В. и Троицкая, С. и Фокина Е.Е., Шилкин С.П. »,
title = «Исследование электрофизических свойств гидридных фаз в системе титан-водород»,
journal = «Российский журнал неорганической химии»,
год = «1994»,
volume = «39»,
pages = «1712-1714»,
ASTM_id = «RJICAQ»
} @article {Bulanova2014,
author = «Буланова М.
М.»,
title = «Константы решетки альфа-титана высокой чистоты»,
journal = «Труды Физического общества, Лондон»,
год = «1962»,
volume = «80»,
pages = «783-786»,
ASTM_id = «PPSOAU»
} @article {Schmitz-Pranghe1968,
author = «Шмитц-Пранге, Н.и Дуэннер, П. «,
title = «Gitterstruktur und thermische Ausdehnung der Uebergangsmetalle Scandium, Titan, Vanadin und Mangan»,
journal = «Zeitschrift fuer Metallkunde»,
год = «1968»,
volume = «59»,
pages = «377-382»,
ASTM_id = «ZEMTAE»
} @article {Hull1921,
author = «Халл, A.W.»,
title = «Кристаллическая структура Ti и Zr»,
journal = «Physical Review (1,1893-132,1963 / 141,1966-188,1969)»,
год = «1921»,
volume = «18»,
pages = «88-89»,
ASTM_id = «PHRVAO»
} @article {Malov1994,
author = «Малов Ю.И., Фокин В. и Троицкая, С. и Фокина Е.Е., Шилкин С.П. »,
title = «Исследование электрофизических свойств гидридных фаз в системе титан-водород»,
journal = «Российский журнал неорганической химии»,
год = «1994»,
volume = «39»,
pages = «1712-1714»,
ASTM_id = «RJICAQ»
} @article {Bulanova2014,
author = «Буланова М. и Фартушна И. и Мелешевич К. и Самелюк А.»,
title = «Изотермический разрез при температуре 850 ° C системы Ti — Dy — Al в области Ti — Ti Al — Dy Al2 — Dy»,
journal = «Журнал сплавов и соединений»,
год = «2014»,
volume = «598»,
pages = «61-67»,
ASTM_id = «JALCEU»
} @article {David1979,
author = «Дэвид, Д.и Гарсия, Э.А. и Лукас, X. и Беранже, Г. «,
title = «Этюд диффузии оксигена в альфа-оксиде титана между 700 и 950 ° C»,
journal = «Журнал менее распространенных металлов»,
год = «1979»,
volume = «65»,
pages = «51-69»,
ASTM_id = «JCOMAH»
} @article {Palty1954,
author = «Палти, А.Е. и Марголин, Х. и Нильсен, Дж. П.»,
title = «Система титан-азот и титан-бор»,
journal = «Сделки Американского общества металлов»,
год = «1954»,
volume = «46»,
pages = «312-328»,
ASTM_id = «TASEA7»
} @article {Hahn1959,
author = «Хан, Х.и Несс, П. «,
title = «Ueber Subchalcogenidphasen des Titans»,
journal = «Zeitschrift fuer Anorganische und Allgemeine Chemie (1950) (DE)»,
год = «1959»,
volume = «302»,
pages = «17-36»,
ASTM_id = «ZAACAB»
} @article {Chattaraj2011,
author = «Chattaraj, D.
и Фартушна И. и Мелешевич К. и Самелюк А.»,
title = «Изотермический разрез при температуре 850 ° C системы Ti — Dy — Al в области Ti — Ti Al — Dy Al2 — Dy»,
journal = «Журнал сплавов и соединений»,
год = «2014»,
volume = «598»,
pages = «61-67»,
ASTM_id = «JALCEU»
} @article {David1979,
author = «Дэвид, Д.и Гарсия, Э.А. и Лукас, X. и Беранже, Г. «,
title = «Этюд диффузии оксигена в альфа-оксиде титана между 700 и 950 ° C»,
journal = «Журнал менее распространенных металлов»,
год = «1979»,
volume = «65»,
pages = «51-69»,
ASTM_id = «JCOMAH»
} @article {Palty1954,
author = «Палти, А.Е. и Марголин, Х. и Нильсен, Дж. П.»,
title = «Система титан-азот и титан-бор»,
journal = «Сделки Американского общества металлов»,
год = «1954»,
volume = «46»,
pages = «312-328»,
ASTM_id = «TASEA7»
} @article {Hahn1959,
author = «Хан, Х.и Несс, П. «,
title = «Ueber Subchalcogenidphasen des Titans»,
journal = «Zeitschrift fuer Anorganische und Allgemeine Chemie (1950) (DE)»,
год = «1959»,
volume = «302»,
pages = «17-36»,
ASTM_id = «ZAACAB»
} @article {Chattaraj2011,
author = «Chattaraj, D.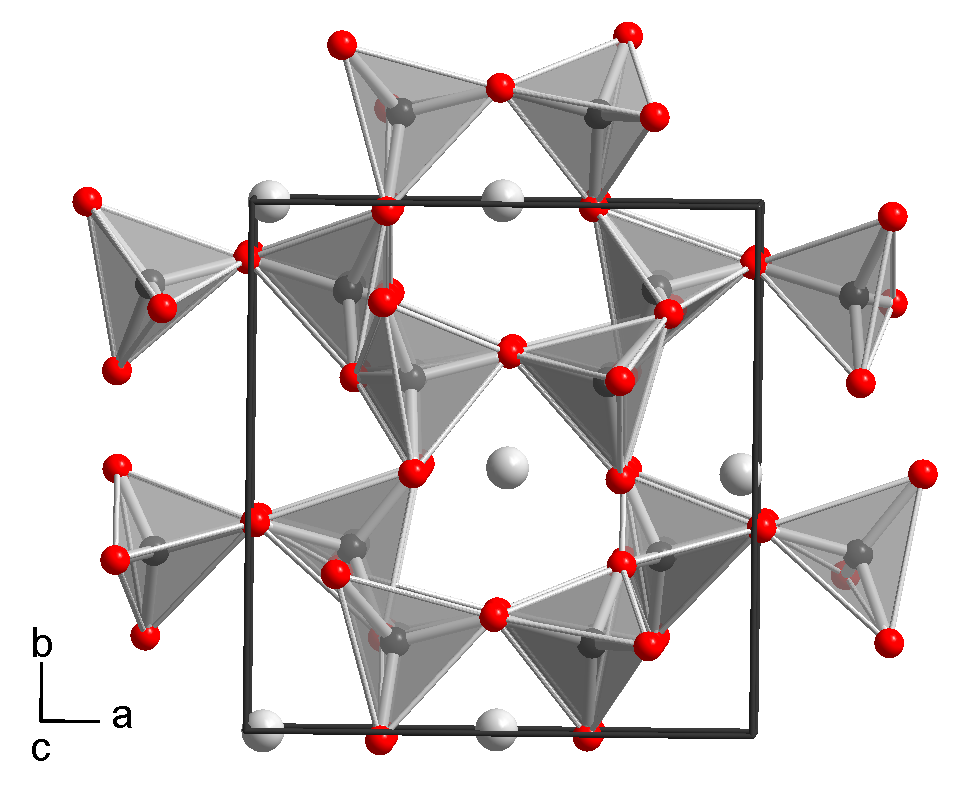 and Parida, S.C. and Majumder, C.»,
title = «Структурные и электронные свойства U2 Ti: исследование первых принципов»,
journal = «Physica B, конденсированное вещество»,
год = «2011»,
volume = «406»,
pages = «4317-4321»,
ASTM_id = «PHYBE3»
} @article {Swanson1954,
author = «Суонсон, Х.Э. и Фуят Р. и Угринич Г.М. «,
title = «Стандартные порошковые дифракционные рентгенограммы III»,
journal = «Национальное бюро стандартов (США), циркуляр»,
год = «1954»,
volume = «539»,
pages = «1-73»,
ASTM_id = «NBSCAA»
} @article {Er2010,
author = «Эр, С. и ван Сеттен, М.Дж., и де Вийс, Г.А., и Брокс, Г.»,
title = «Моделирование из первых принципов гидридов магния и титана»,
journal = «Журнал физики: конденсированное вещество»,
год = «2010»,
volume = «22»,
pages = «074208-1-074208-13»,
ASTM_id = «JCOMEL»
} @article {Makarov1960,
author = «Макаров, Э.С., Кузнецов Л.М. »,
title = «Кристаллическая структура и химическая природа низших оксидов титана Ti O0,48»,
journal = «Журнал Структурной химии (Выпуск № 1981)»,
год = «1960»,
volume = «1»,
pages = «170-177»,
ASTM_id = «ZSTKAI»
}
and Parida, S.C. and Majumder, C.»,
title = «Структурные и электронные свойства U2 Ti: исследование первых принципов»,
journal = «Physica B, конденсированное вещество»,
год = «2011»,
volume = «406»,
pages = «4317-4321»,
ASTM_id = «PHYBE3»
} @article {Swanson1954,
author = «Суонсон, Х.Э. и Фуят Р. и Угринич Г.М. «,
title = «Стандартные порошковые дифракционные рентгенограммы III»,
journal = «Национальное бюро стандартов (США), циркуляр»,
год = «1954»,
volume = «539»,
pages = «1-73»,
ASTM_id = «NBSCAA»
} @article {Er2010,
author = «Эр, С. и ван Сеттен, М.Дж., и де Вийс, Г.А., и Брокс, Г.»,
title = «Моделирование из первых принципов гидридов магния и титана»,
journal = «Журнал физики: конденсированное вещество»,
год = «2010»,
volume = «22»,
pages = «074208-1-074208-13»,
ASTM_id = «JCOMEL»
} @article {Makarov1960,
author = «Макаров, Э.С., Кузнецов Л.М. »,
title = «Кристаллическая структура и химическая природа низших оксидов титана Ti O0,48»,
journal = «Журнал Структурной химии (Выпуск № 1981)»,
год = «1960»,
volume = «1»,
pages = «170-177»,
ASTM_id = «ZSTKAI»
}
Изучение точечных дефектов и примесей в титане из первых принципов
Титан в чистом виде при комнатной температуре и атмосферном давлении кристаллизуется в ГПУ-структуре с симметрией пространственной группы P6 3 / mmc (международная космическая группа no. 194). Кристаллическая структура содержит два атома на примитивную ячейку. 32 Параметры решетки, определенные в результате экспериментов и теоретических исследований, показаны в таблице 1, где вычисленные значения с использованием функционалов обменно-корреляции, таких как приближение локальной плотности (LDA 33 ) и две различные параметризации приближения обобщенного градиента (GGA ), PW’91 34 и PBE.
194). Кристаллическая структура содержит два атома на примитивную ячейку. 32 Параметры решетки, определенные в результате экспериментов и теоретических исследований, показаны в таблице 1, где вычисленные значения с использованием функционалов обменно-корреляции, таких как приближение локальной плотности (LDA 33 ) и две различные параметризации приближения обобщенного градиента (GGA ), PW’91 34 и PBE.
Чтобы сравнить относительную стабильность различных дефектов, мы вычисляем энергию образования, которая получается из полные энергии, рассчитанные из DFT.Энергия формации задается как: 35,36,37
$$ E_f \ left ({\ mathrm {D}} \ right) = E _ {{\ mathrm {Supercell}}} \ left ({\ mathrm { D}} \ right) — E _ {{\ mathrm {Ti}} — {\ mathrm {host}}} — pn_X \ mu _X $$
(1)
Здесь, E f (D) — энергия образования дефекта D, которая измеряется в эВ / суперячейка, E Supercell (D) и E Ti-host — это полная энергия дефекта и чистая суперячейки соответственно.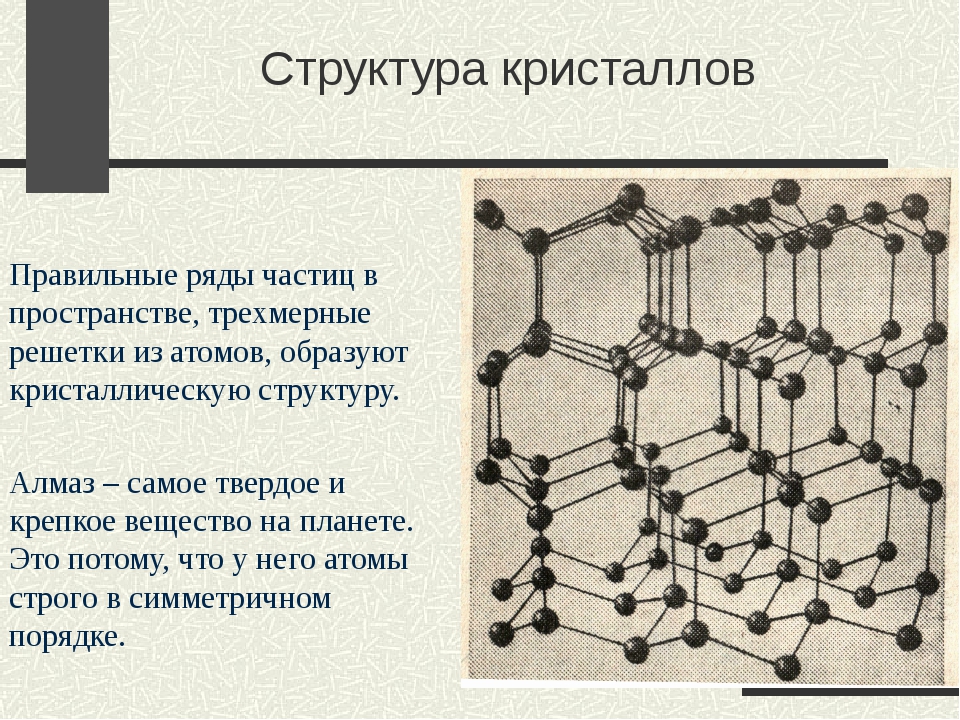 мкм X — химический потенциал видов X и n X — количество таких примесей в дефектной суперячейке. p = ± 1 в зависимости от того, удаляется ли атом из суперячейки-хозяина или добавляется к ней, чтобы сконструировать дефектную суперячейку. Концентрация точечных дефектов пропорциональна экспоненте энергии образования. Энергия образования также помогает определить коэффициент диффузии для кинематики дефектов. 38 Однако первые принципы определения энергии формации, рассчитанной по формуле. (1) зависит от выбора мкм X ; следовательно, правильный выбор химических потенциалов улучшает интерпретацию энергий формации. В нашем исследовании мкм X Значения выбираются из чистого состояния примесей, называемых химическими потенциалами «элементов», а оксиды соответствующих примесных элементов называются химическими потенциалами «оксидов».
мкм X — химический потенциал видов X и n X — количество таких примесей в дефектной суперячейке. p = ± 1 в зависимости от того, удаляется ли атом из суперячейки-хозяина или добавляется к ней, чтобы сконструировать дефектную суперячейку. Концентрация точечных дефектов пропорциональна экспоненте энергии образования. Энергия образования также помогает определить коэффициент диффузии для кинематики дефектов. 38 Однако первые принципы определения энергии формации, рассчитанной по формуле. (1) зависит от выбора мкм X ; следовательно, правильный выбор химических потенциалов улучшает интерпретацию энергий формации. В нашем исследовании мкм X Значения выбираются из чистого состояния примесей, называемых химическими потенциалами «элементов», а оксиды соответствующих примесных элементов называются химическими потенциалами «оксидов».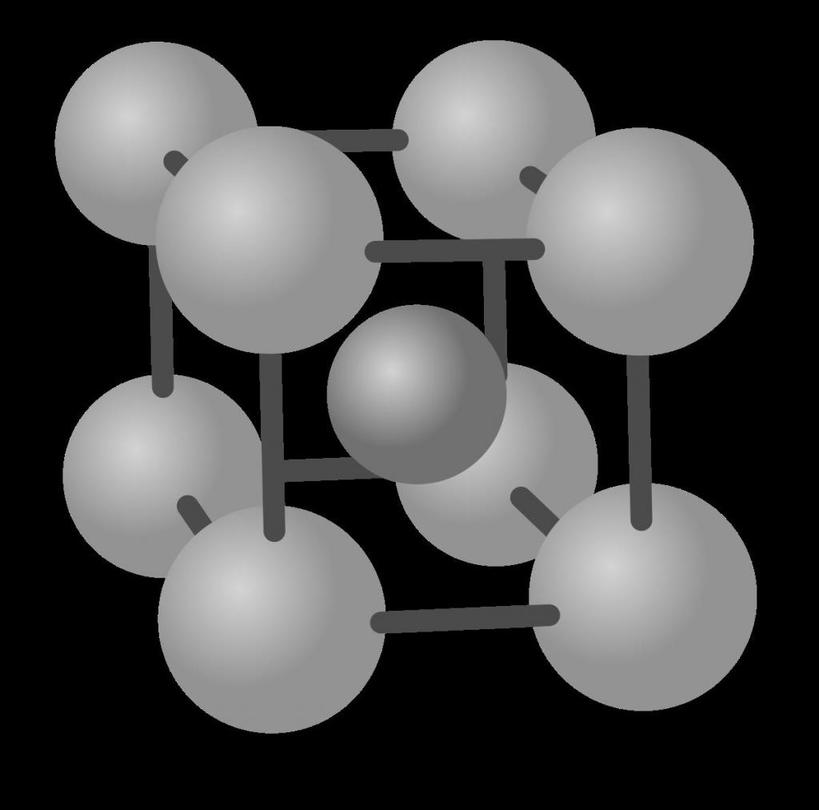 Подробно об источниках μ X и их роль в термодинамике представлена во вспомогательной информации.
Подробно об источниках μ X и их роль в термодинамике представлена во вспомогательной информации.
Отметим, что LDA и GGA не позволяют предсказывать свойства основного состояния сильно коррелированных систем, в первую очередь оксидов переходных металлов, проявляющих сегнетоэлектричество, сверхпроводимость, переходы металл-изолятор и магнетизм. Проблема является более острой для свойств полупроводников и магнитных свойств, а не для простых металлических элементов.Ситуацию в идеале можно преодолеть, включив термин «кулоновское отталкивание», специфичный для конкретного элемента и орбитально-селективного кулоновского отталкивания, называемый Hubbard U (метод DFT + U ). Однако нет единого мнения относительно использования конкретного значения U для всех расчетов, поскольку значения не подлежат передаче. Фактическое значение U меняется в зависимости от элементов переходных металлов и их соответствующих соединений.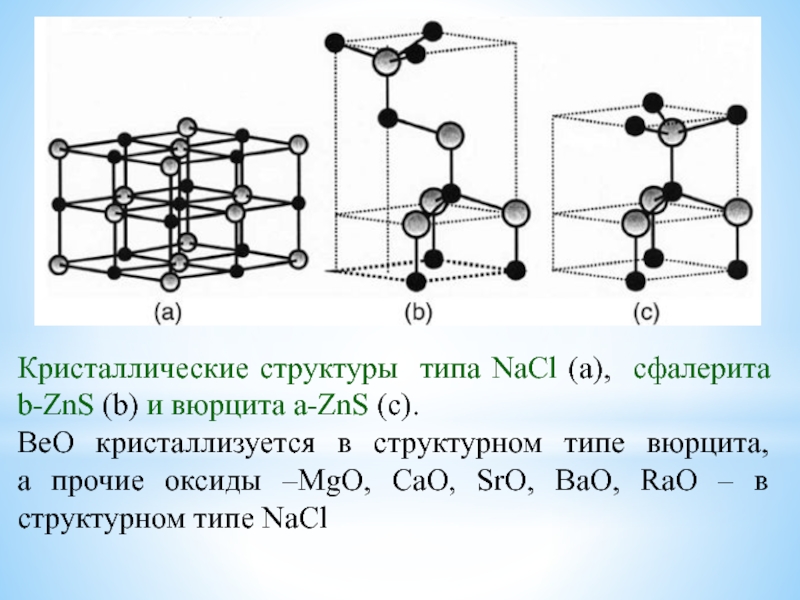 Это дополнительно осложняется тем фактом, что не ожидается, что значение U будет одинаковым для разных кристаллических структур одного и того же элемента или соединения.Таким образом, полная энергия зависит от значения U в методе DFT + U . Поскольку общая энергия является основой нашего анализа, мы пытаемся здесь избежать неоднозначностей, которые могут возникнуть из-за включения двух различных уровней теории, DFT и DFT + U и изменения значения U индивидуально для каждого элемента.
Это дополнительно осложняется тем фактом, что не ожидается, что значение U будет одинаковым для разных кристаллических структур одного и того же элемента или соединения.Таким образом, полная энергия зависит от значения U в методе DFT + U . Поскольку общая энергия является основой нашего анализа, мы пытаемся здесь избежать неоднозначностей, которые могут возникнуть из-за включения двух различных уровней теории, DFT и DFT + U и изменения значения U индивидуально для каждого элемента.
Само-межузельные атомы
Атомы титана, занимающие межузельные узлы решетки, являются собственными междоузлиями. В кристаллической решетке ГПУ межузельный дефект может располагаться в шести узлах элементарной ячейки, как показано на рис.1. 39 Они называются ортогональными (O) и тетраэдрическими (T) узлами. Примеси в базально-тетраэдрических (BT) и базально-октаэдрических (BO) узлах лежат в базисной плоскости, на полпути между двумя соседними узлами T и узлами O вдоль направления c, соответственно.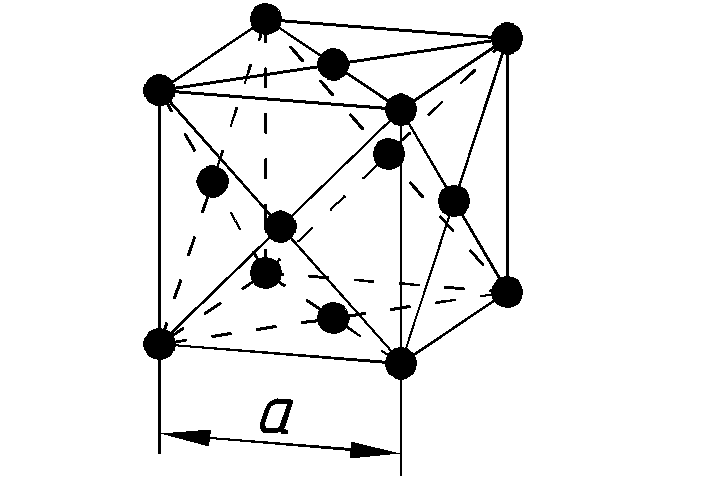 Краудионы представляют собой интерстициальные позиции между центром связи Ti-Ti, и были идентифицированы две различные конфигурации: базальный (CB) и небазальный (CN) краудионы. В отличие от этих примесных узлов, которые могут содержать только один примесный атом на узел, димероподобные межузельные дефекты содержат два атома.Два атома димероподобной примеси симметрично смещены относительно вакантного узла решетки. Из-за гексагональной симметрии существуют две ориентации димероподобных точечных дефектов. Конфигурация гантели, ориентированная в направлении c (DC), и конфигурация гантели, лежащая в базовой плоскости (DB), являются уникальным выбором. Конфигурации DC и DB представляют собой разделенные межстраничные объявления, которые представляют собой самостоятельные межстраничные объявления. Положение всех восьми межузельных конфигураций показано на схематическом изображении рис.1. Энергии образования суммированы для восьми межузельных конфигураций в Ti, перечисленных в Таблице 2.
Краудионы представляют собой интерстициальные позиции между центром связи Ti-Ti, и были идентифицированы две различные конфигурации: базальный (CB) и небазальный (CN) краудионы. В отличие от этих примесных узлов, которые могут содержать только один примесный атом на узел, димероподобные межузельные дефекты содержат два атома.Два атома димероподобной примеси симметрично смещены относительно вакантного узла решетки. Из-за гексагональной симметрии существуют две ориентации димероподобных точечных дефектов. Конфигурация гантели, ориентированная в направлении c (DC), и конфигурация гантели, лежащая в базовой плоскости (DB), являются уникальным выбором. Конфигурации DC и DB представляют собой разделенные межстраничные объявления, которые представляют собой самостоятельные межстраничные объявления. Положение всех восьми межузельных конфигураций показано на схематическом изображении рис.1. Энергии образования суммированы для восьми межузельных конфигураций в Ti, перечисленных в Таблице 2.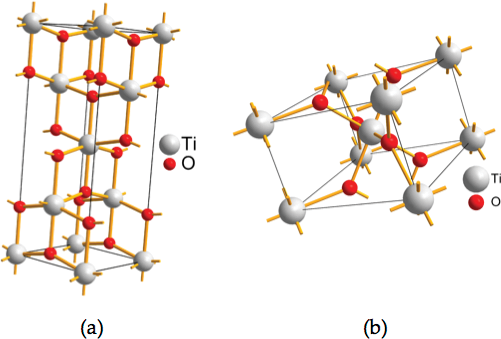 Сверхъячейка состоит из периодического повторения элементарных ГПУ элементарных решеток, в которых размещены примесные атомы. Эта суперячейка геометрически оптимизирована схемой сопряженного градиента, чтобы минимизировать внутреннюю деформацию. Характерные положения примесей в оптимизированной суперячейке устанавливаются путем исследования ближайшего соседа. Разница энергий образования и разность полной энергии идентичны для изолированных межузельных дефектов.Однако энергия образования имеет преимущество, так как она позволяет сравнивать расщепленную межузельную энергетику со случаями конфигураций дефектов замещения и межузельных дефектов.
Сверхъячейка состоит из периодического повторения элементарных ГПУ элементарных решеток, в которых размещены примесные атомы. Эта суперячейка геометрически оптимизирована схемой сопряженного градиента, чтобы минимизировать внутреннюю деформацию. Характерные положения примесей в оптимизированной суперячейке устанавливаются путем исследования ближайшего соседа. Разница энергий образования и разность полной энергии идентичны для изолированных межузельных дефектов.Однако энергия образования имеет преимущество, так как она позволяет сравнивать расщепленную межузельную энергетику со случаями конфигураций дефектов замещения и межузельных дефектов.
Схематическая кристаллическая структура, показывающая положения различных типов собственных междоузлий в решетке ГПУ Ti. Положения тетраэдрической (T), ортогональной (O), базовой тетраэдрической (BT), базовой ортогональной (BO), краудиона в базальной (CB) и небазальной (CN) плоскостях, а также расщепленной межузельной плоскости вдоль c Обозначены -направление (DC) и в базисной плоскости (DB).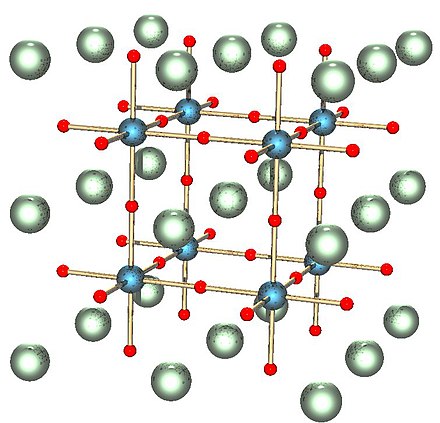 В таблице 2 приведена относительная стабильность этих дефектов в Ti-матрице
В таблице 2 приведена относительная стабильность этих дефектов в Ti-матрице
Длина связи расслоенного межузельного перехода была рассчитана как 1,663 и 1,930 Å для DC и DB, соответственно. Начальная геометрия была выбрана путем выбора конфигурации с наименьшей полной энергией после выполнения проверки полной энергии как функции длины связи пары примесей в чистой решетке.Энергии пласта показаны в Таблице 2 для начальных ( E f U ) и расслабленный ( E f R ) суперячейки для различных конфигураций. Другими словами, E f U указывает энергию примесных межузельных димеров, когда основные атомы не релаксированы.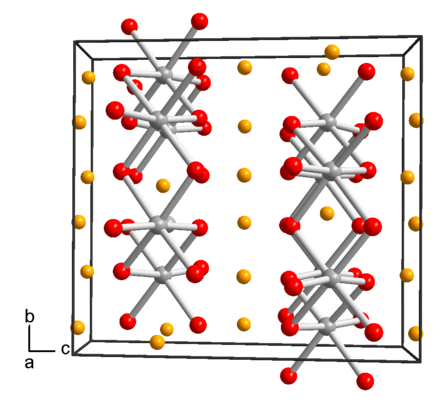 Разница в энергии (Δ E f UR = E f U — E f R ) учитывает выигрыш химической энергии за счет локальных искажений решетки.Длины связей Ti – Ti составляют 1,430 и 1,463 Å для конфигураций CN и CB соответственно, что составляет примерно половину постоянной равновесной решетки. Δ E f UR кажется большим для краудиновых межстраничных объявлений; 9,4 и 9,8 эВ для CB и CN соответственно из-за величины E f U , который уже является большим из-за дополнительного атома Ti между равновесными связями Ti – Ti.По сравнению с этим, разница в энергии Δ E f UR является минимальным для разделенных межузельных конфигураций, DC и DB, так как два примесных атома расположены в межузельной области близко к их равновесному разделению из-за способа приготовления моделей DC и DB.
Разница в энергии (Δ E f UR = E f U — E f R ) учитывает выигрыш химической энергии за счет локальных искажений решетки.Длины связей Ti – Ti составляют 1,430 и 1,463 Å для конфигураций CN и CB соответственно, что составляет примерно половину постоянной равновесной решетки. Δ E f UR кажется большим для краудиновых межстраничных объявлений; 9,4 и 9,8 эВ для CB и CN соответственно из-за величины E f U , который уже является большим из-за дополнительного атома Ti между равновесными связями Ti – Ti.По сравнению с этим, разница в энергии Δ E f UR является минимальным для разделенных межузельных конфигураций, DC и DB, так как два примесных атома расположены в межузельной области близко к их равновесному разделению из-за способа приготовления моделей DC и DB.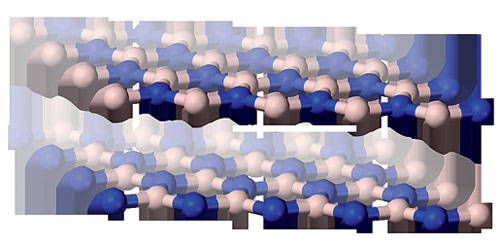
Мы обнаружили, что конфигурация BO является наиболее подходящей внутренней конфигурацией. Энергия конфигурации CB аналогична энергии конфигурации BO.{\ mathrm {U}} \) в таблице 2).
Вакансия-межузельные пары
Энергия образования атома, отсутствующего в узле решетки, т.е. вакансии ( V Ti , не путать с ванадием, замещенным в узле Ti, V Ti ), составляет рассчитывается как
$$ E_f \ left ({V _ {{\ mathrm {Ti}}}} \ right) = E \ left ({{\ mathrm {Ti}} + V _ {{\ mathrm {Ti}}}} \ right) — \ mu _ {{\ mathrm {Ti}}} $$
(2)
, где E — полная энергия, а значение μ Ti , полученное из массы Ti, оказывается равным 1.94 эВ, что аналогично значению, полученному при расчетах сверхмягких псевдопотенциалов. 40 Энергии вакансий Ti получены в аналогичном диапазоне с другими обменно-корреляционными функционалами, 41 , которые завышены, чем указано в эксперименте (1,55 эВ в ссылке 42 и 1,27 эВ по спектроскопии аннигиляции позитронов в ссылке.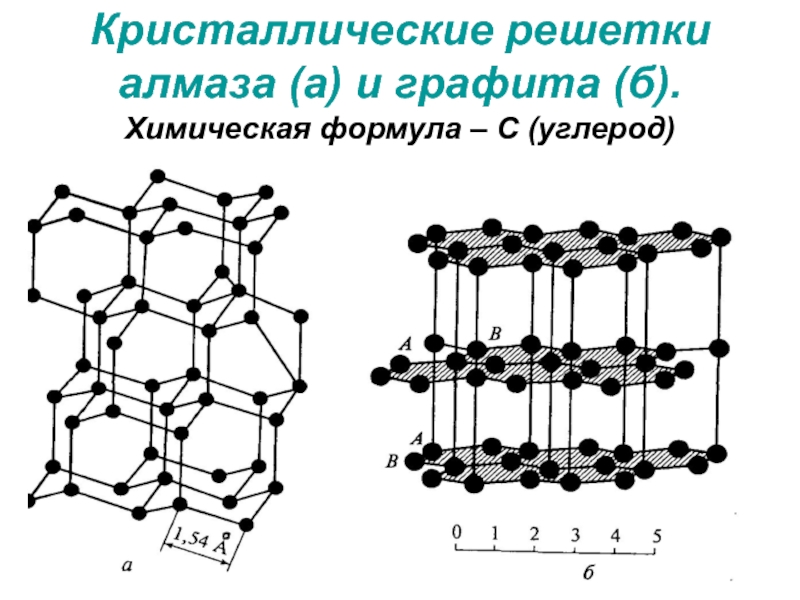 43 ). Расхождение связано с отсутствием обменной корреляции на основе плотности для точной обработки электронной корреляции. 44 Есть способ преодолеть ограничения GGA, добавив поправочный член Хаббарда U . Однако в нашем исследовании он не использовался из-за неоднозначности, которую он вносит в обработку химических потенциалов, влияющих на расчет энергий формации. Энергетика показывает, что величина энергии образования вакансий сравнима с величиной энергии межузельных связей, см. Таблицу 2. Таким образом, можно предположить, что и вакансии, и межузельные атомы, вероятно, будут одновременно реагировать на термодинамические возмущения, которые могут быть объединены для получения механизм миграции для перехода атома Ti из положения решетки в ближайшее межузельное положение.Рассмотрение μ Ti , полученного из объемных моделей Ti, включает ситуацию, когда решетка вакансий находится в термодинамическом равновесии с идеальным объемным Ti. Однако это может быть нереалистично в технологических процессах, особенно если интересующий смещенный атом Ti остается глубоко в объеме образца, образуя вторичные фазы с другими дефектами / примесями в решетке.
43 ). Расхождение связано с отсутствием обменной корреляции на основе плотности для точной обработки электронной корреляции. 44 Есть способ преодолеть ограничения GGA, добавив поправочный член Хаббарда U . Однако в нашем исследовании он не использовался из-за неоднозначности, которую он вносит в обработку химических потенциалов, влияющих на расчет энергий формации. Энергетика показывает, что величина энергии образования вакансий сравнима с величиной энергии межузельных связей, см. Таблицу 2. Таким образом, можно предположить, что и вакансии, и межузельные атомы, вероятно, будут одновременно реагировать на термодинамические возмущения, которые могут быть объединены для получения механизм миграции для перехода атома Ti из положения решетки в ближайшее межузельное положение.Рассмотрение μ Ti , полученного из объемных моделей Ti, включает ситуацию, когда решетка вакансий находится в термодинамическом равновесии с идеальным объемным Ti. Однако это может быть нереалистично в технологических процессах, особенно если интересующий смещенный атом Ti остается глубоко в объеме образца, образуя вторичные фазы с другими дефектами / примесями в решетке.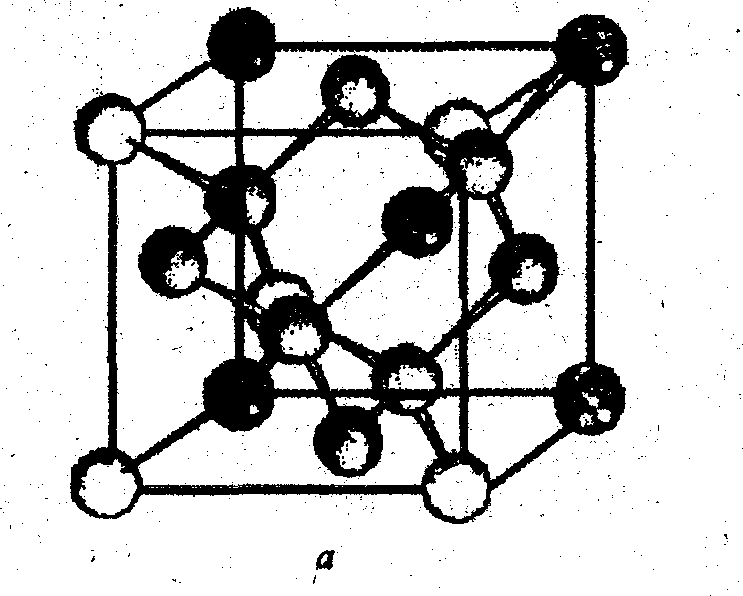 Наиболее тривиальным случаем для нашего обсуждения были бы комплексы дефектов, состоящие из вакансии и собственной межузельной примеси.
Наиболее тривиальным случаем для нашего обсуждения были бы комплексы дефектов, состоящие из вакансии и собственной межузельной примеси.
Чтобы получить представление о дефектных комплексах, мы рассчитали энергию образования пары V Ti – межузельный Ti как функцию разделения отдельных компонентов, то есть вакансии титана, V Ti и межузельный атом титана. Модели Supercell были подготовлены с промежуточным Ti в конфигурации BO и V Ti , созданным в разных положениях, так что расстояние V Ti от промежуточного Ti равно 2.15, 4.20, 4.58, 6.44 и 9.23 Å. После минимизации внутренних сил в суперъячейках (геометрическая оптимизация) было обнаружено, что для первых трех более коротких парных разделений ожидается, что промежуточный Ti будет притягиваться к пустому узлу решетки, что может привести к устранению дефекта. Однако при больших расстояниях 6,44 и 9,23 Å взаимодействие между V Ti и межузельным атомом титана экранируется атомами хозяина между ними.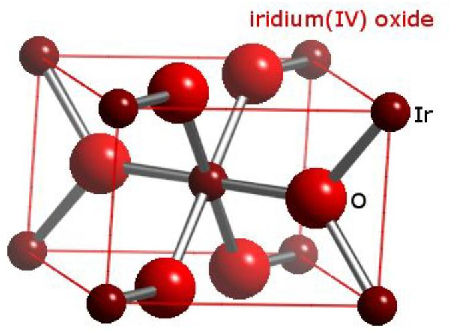 В результате V Ti и межузельный атом Ti захватываются в локальные энергетические минимумы без какого-либо заметного изменения расстояния между ними.Энергии образования для трех самых коротких разделительных расстояний идентичны и почти на 3,9 эВ ниже энергии образования двух больших расстояний. В идеале из энергетики можно было бы ожидать, что вакансии и межузельные частицы должны аннигилировать друг друга и, таким образом, воссоздать среду идеальной ГПУ-решетки, если эти дефекты находятся в непосредственной близости.
В результате V Ti и межузельный атом Ti захватываются в локальные энергетические минимумы без какого-либо заметного изменения расстояния между ними.Энергии образования для трех самых коротких разделительных расстояний идентичны и почти на 3,9 эВ ниже энергии образования двух больших расстояний. В идеале из энергетики можно было бы ожидать, что вакансии и межузельные частицы должны аннигилировать друг друга и, таким образом, воссоздать среду идеальной ГПУ-решетки, если эти дефекты находятся в непосредственной близости.
Примеси внедрения и замещения
Энергии образования примесей для положений внедрения и замещения в решетке ГПУ-Ti рассчитываются на основе «элементарных» химических потенциалов ( μ элемент ) и химических потенциалов «оксида» ( μ оксид ), см. Дополнительную информацию, которая указана в таблицах 3 и 4 соответственно.Например, на рис. 2а показаны рассчитанные энергии образования примеси O в Ti. Энергии образования в нижнем диапазоне получены из полной энергии молекулы O 2 , что может быть интерпретировано как термодинамическое состояние с богатой кислородом окружающей средой, в то время как энергии образования в направлении верхнего диапазона получены из TiO 2 в структура рутила, которую можно интерпретировать как термодинамическое состояние с дефицитом кислорода в среде.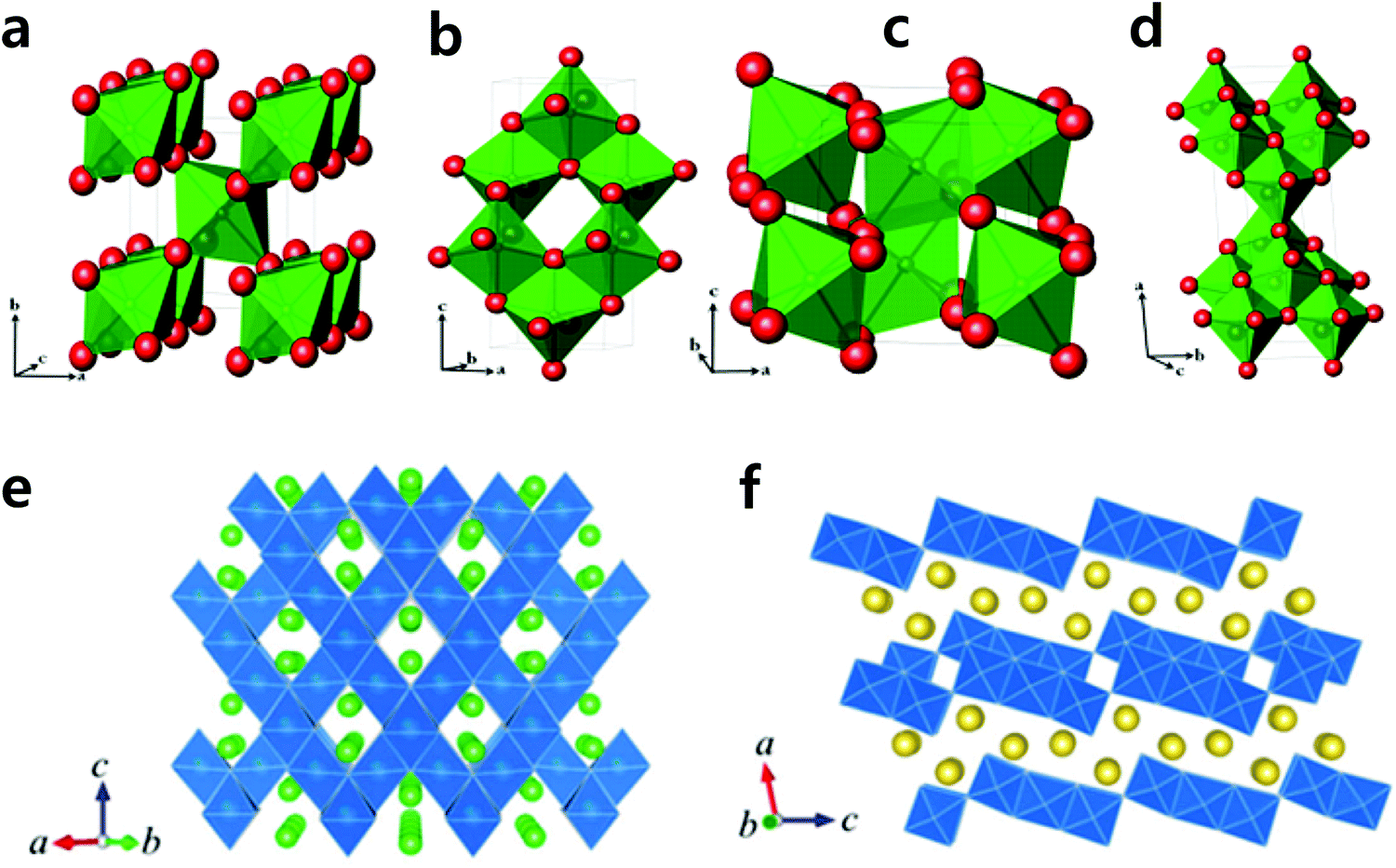 Горизонтальные пунктирные линии на этом рисунке обозначают конфигурацию с самыми низкими энергиями формации в каждом случае.Замечено, что атом O предпочитает октаэдрическое межузельное положение, когда окружающая среда является дефицитной по кислороду. С другой стороны, в среде с богатым поступлением кислорода термодинамически стабильной фазой являются пары примесей кислорода, приводящие к конфигурациям DB и DC (см. Рис. 1). Относительные различия в энергиях образования позиций внедрения и замещения для двух типов химического окружения можно оценить по данным рис. 2а.
Горизонтальные пунктирные линии на этом рисунке обозначают конфигурацию с самыми низкими энергиями формации в каждом случае.Замечено, что атом O предпочитает октаэдрическое межузельное положение, когда окружающая среда является дефицитной по кислороду. С другой стороны, в среде с богатым поступлением кислорода термодинамически стабильной фазой являются пары примесей кислорода, приводящие к конфигурациям DB и DC (см. Рис. 1). Относительные различия в энергиях образования позиций внедрения и замещения для двух типов химического окружения можно оценить по данным рис. 2а.
Сравнение энергий образования примесных элементов в различных положениях внедрения и на сайт.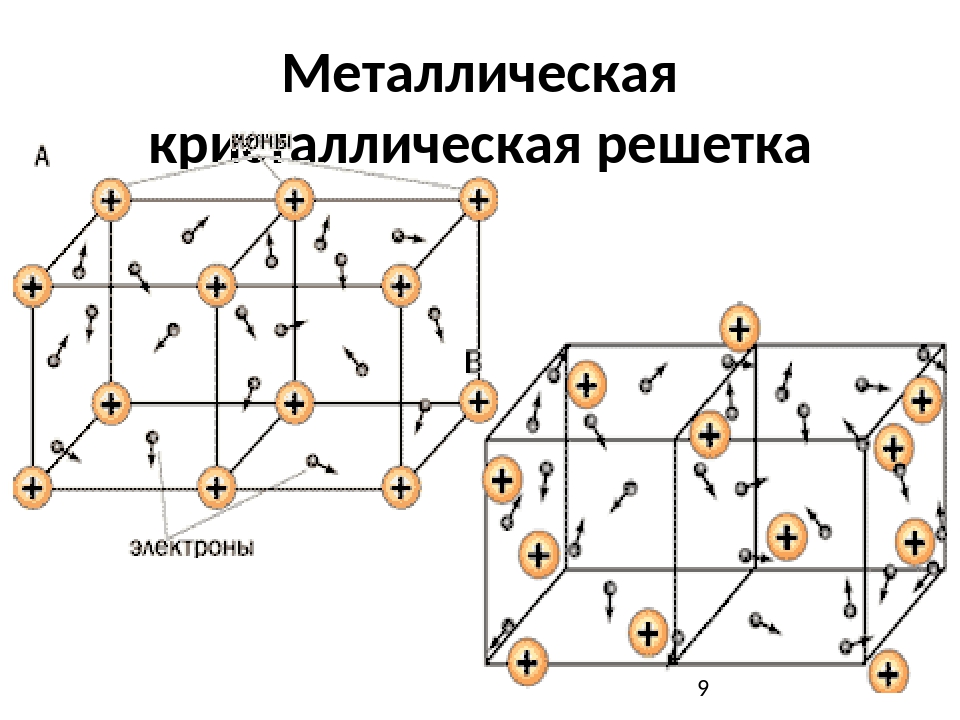 Примесь O выбрана в качестве примера в ( a ). Нижний и верхний диапазоны энергий пласта получены с использованием мкм оксида и мкм элемента , полученного из молекулы O 2 и твердого тела TiO 2 , соответственно, значения которых показаны пунктирными горизонтальными линиями. b Минимальное значение энергии образования исследуемых примесей от двух источников химических потенциалов. Символы соответствуют примесным конфигурациям, как в ( a ). Энергии формирования данных для выбранных элементов 3d, 4d и 5d показаны на заштрихованном (желтом) фоне.
Примесь O выбрана в качестве примера в ( a ). Нижний и верхний диапазоны энергий пласта получены с использованием мкм оксида и мкм элемента , полученного из молекулы O 2 и твердого тела TiO 2 , соответственно, значения которых показаны пунктирными горизонтальными линиями. b Минимальное значение энергии образования исследуемых примесей от двух источников химических потенциалов. Символы соответствуют примесным конфигурациям, как в ( a ). Энергии формирования данных для выбранных элементов 3d, 4d и 5d показаны на заштрихованном (желтом) фоне.
Чем ниже энергия образования конфигурации дефекта, тем выше вероятность обнаружения такого дефекта в образце. На рис. 2b показаны самые низкие энергии образования, полученные для различных элементов, от H (атомный номер = 1) до Ca (атомный номер = 20), за исключением элементов из благородных газов He и Ne.Дополнительные выбранные элементы из элементов переходных металлов серий 3d, 4d и 5d, V, Ni, Cu, Zr, Mo, Ag, Ta, W, Au и Pb, рассматриваются для сравнения тенденции энергий образования элементов для относительно больший размер атома. Энергии образования для этих случаев показаны в заштрихованной области на рис. 2б. Тенденция самых низких энергий образования (среди различных конфигураций примесей) на фиг. 2b, которая происходит от μ элемента , отмечена красной линией.Энергии образования, полученные из мкм оксида , отмечены синей линией на том же рисунке. Было обнаружено, что такая обработка химическим потенциалом приводит к двум различным тенденциям в наименьшей энергии пласта.
Энергии образования для этих случаев показаны в заштрихованной области на рис. 2б. Тенденция самых низких энергий образования (среди различных конфигураций примесей) на фиг. 2b, которая происходит от μ элемента , отмечена красной линией.Энергии образования, полученные из мкм оксида , отмечены синей линией на том же рисунке. Было обнаружено, что такая обработка химическим потенциалом приводит к двум различным тенденциям в наименьшей энергии пласта.
В целом металлические примеси, независимо от их атомных размеров и воздействия химического окружения (учет двух различных химических потенциалов), благоприятствуют центрам замещения. С другой стороны, обычные элементы с высокой электроотрицательностью, такие как C, N, O, F, S и Cl, не поддерживают сайт замещения.Вместо этого элементы C, N и Cl предпочитают октаэдрические межузельные участки для двух химических сред. H, O и S стабилизируют различные конфигурации примесей при различной обработке химическим потенциалом: октаэдрические конфигурации примесей для μ оксида и конфигурации примесных димеров (DB и DC) для μ элемента .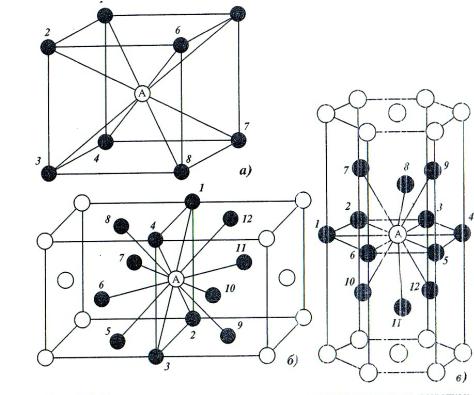 Фтор — единственный элемент, который образует примесный димер в Ti для обоих типов химических потенциалов. Следует подчеркнуть, что H, который может легко потерять свой электрон, образуя катион H + , на самом деле ведет себя аналогично электроотрицательным элементам при введении в качестве примеси в Ti.Этот результат подтверждает анализ переноса заряда, в котором H приобретает электроны от соседних атомов Ti, что обсуждается в следующем разделе.
Фтор — единственный элемент, который образует примесный димер в Ti для обоих типов химических потенциалов. Следует подчеркнуть, что H, который может легко потерять свой электрон, образуя катион H + , на самом деле ведет себя аналогично электроотрицательным элементам при введении в качестве примеси в Ti.Этот результат подтверждает анализ переноса заряда, в котором H приобретает электроны от соседних атомов Ti, что обсуждается в следующем разделе.
Анализ заряда
Химическая гибридизация играет важную роль для конфигурации примесных атомов в кристаллических решетках. Идеальной мерой силы орбитальной гибридизации является перенос заряда между примесью и атомами хозяина. Анализ заряда Бадера 45,46 обеспечивает количественную оценку сопровождаемого переноса заряда.{{\ mathrm {hybridized}}} \) — это рассчитанный заряд Бейдера после достижения самосогласованных полевых решений. Согласно этому определению отрицательные значения для Δ q B ( X ) будет означать накопление заряда по соседству с атомным участком X (определение согласуется с определением заряда электрона, рассматриваемого как отрицательный), а положительное значение будет означать потерю заряда из атомного узла X к окружающему. Тенденция Δ q B Ожидается, что ( X ) для примесных и основных атомов будут иметь обратную связь, так как потеря или накопление заряда в примесном узле должны коррелировать с изменениями заряда в соседних основных атомах. Отрицательные значения Δ q B являются признаком электроотрицательных примесей, таких как C, N, O и F. Перенос заряда на соседний основной Ti (<Δ q B (Ti)>) усредняется по координации ближайших соседей 4, 6 и 12 для примесного атома, расположенного в тетраэдрических, октаэдрических и замещающих примесных узлах соответственно.
Тенденция Δ q B Ожидается, что ( X ) для примесных и основных атомов будут иметь обратную связь, так как потеря или накопление заряда в примесном узле должны коррелировать с изменениями заряда в соседних основных атомах. Отрицательные значения Δ q B являются признаком электроотрицательных примесей, таких как C, N, O и F. Перенос заряда на соседний основной Ti (<Δ q B (Ti)>) усредняется по координации ближайших соседей 4, 6 и 12 для примесного атома, расположенного в тетраэдрических, октаэдрических и замещающих примесных узлах соответственно.
Перенос заряда между примесными атомами и ближайшими соседними основными атомами Ti показан как функция атомного номера (за исключением благородных газов) на рис. 3а для октаэдрических и замещающих примесных узлов. Перенос заряда следует той же тенденции периодов в периодической таблице для обоих примесных узлов. Средний перенос заряда на Ti ниже по величине, потому что несколько атомов Ti из соседней связи связаны с атомом примеси. Перенос заряда на примесные атомы в октаэдрических межузельных узлах и позициях замещения различается в зависимости от среднего переноса заряда Ti, как показано на рис.3b. Синие и черные сплошные линии представляют собой линии тренда для данных о примесях в октаэдрических положениях внедрения и замещения, соответственно. Из рис. 3b видно, что перенос заряда на примеси в случаях замещения (наклон черной линии) обычно больше, чем для октаэдрических позиций примеси (наклон синей линии). Та же информация также изображена на рис. 3a, где мы отмечаем разницу в значениях переноса заряда между случаями замещения (закрашенные квадраты) и промежуточными (пустой кружок) случаями.Как уже указывалось в предыдущем разделе, H в металлическом Ti имеет отрицательные значения Δ q B как для случая замещения, так и для случая внедрения (см.
Средний перенос заряда на Ti ниже по величине, потому что несколько атомов Ti из соседней связи связаны с атомом примеси. Перенос заряда на примесные атомы в октаэдрических межузельных узлах и позициях замещения различается в зависимости от среднего переноса заряда Ti, как показано на рис.3b. Синие и черные сплошные линии представляют собой линии тренда для данных о примесях в октаэдрических положениях внедрения и замещения, соответственно. Из рис. 3b видно, что перенос заряда на примеси в случаях замещения (наклон черной линии) обычно больше, чем для октаэдрических позиций примеси (наклон синей линии). Та же информация также изображена на рис. 3a, где мы отмечаем разницу в значениях переноса заряда между случаями замещения (закрашенные квадраты) и промежуточными (пустой кружок) случаями.Как уже указывалось в предыдущем разделе, H в металлическом Ti имеет отрицательные значения Δ q B как для случая замещения, так и для случая внедрения (см. Рис. 3a, b), предполагая, что он действует как примесь, притягивающая электроны, аналогично C, O и F.
Рис. 3a, b), предполагая, что он действует как примесь, притягивающая электроны, аналогично C, O и F.
Предпочтительная конфигурация для рассмотренных элементов представлена на рис.4, где энергии образования примесей замещения сравниваются с минимальной энергией образования из межузельных конфигураций. Установлено, что высоко электроотрицательные элементы, H, C, N, O, F, S и Cl, благоприятствуют межузельным положениям (см. Рис. 2b. Химическая гибридизация играет более решающую роль, чем другие конкурирующие термины. Линия y = x — случай, когда как примеси замещения, так и примеси замещения равновероятны.Чем дальше от этой линии, тем выше вероятность наличия примесей замещения или замещения.Случаи примесей P и Ni отличаются от ожидаемого поведения. Другими словами, их энергии образования лежат относительно близко к линии y = x .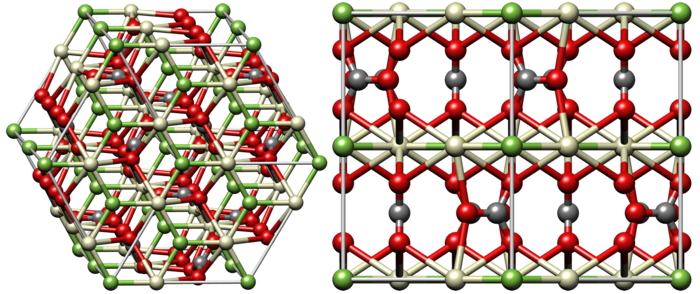 Интуитивно ожидается, что P будет благоприятствовать промежуточному положению, тогда как ожидается, что Ni будет способствовать замещающему сайту. Пересмотр исходных соединений, из которых происходит химический потенциал, потенциально может помочь исправить это несоответствие. Кроме того, для Ni трудность может заключаться в величине химического потенциала, который получается из оксидного соединения NiO.NiO является примером соединения, в котором приближение GGA не учитывает сильные эффекты электронной корреляции. 47
Интуитивно ожидается, что P будет благоприятствовать промежуточному положению, тогда как ожидается, что Ni будет способствовать замещающему сайту. Пересмотр исходных соединений, из которых происходит химический потенциал, потенциально может помочь исправить это несоответствие. Кроме того, для Ni трудность может заключаться в величине химического потенциала, который получается из оксидного соединения NiO.NiO является примером соединения, в котором приближение GGA не учитывает сильные эффекты электронной корреляции. 47
Сравнение энергий образования между сайтом замещения (по оси абсцисс) и наиболее благоприятной межузельной конфигурацией (по оси ординат). Линия y = x показывает четкое разделение и указывает на благоприятную конфигурацию точечных дефектов.
Микроструктура и механические характеристики решетчатых структур Ti – 6Al – 4V, изготовленных методом электронно-лучевой плавки (EBM): Обзор
org/Book»> [1]И.Полмеар, Д. Сент-Джон, Дж. Ф. Ни, М. Цянь, Легкие сплавы: металлургия легких металлов (Butterworth-Heinemann, Oxford, 2017)
Google ученый
A. Saboori, D. Gallo, S. Biamino, P. Fino, M. Lombardi, Appl. Sci. 7 (9), 883 (2017)
Google ученый
M. Peters, Титан и титановые сплавы (Wiley, New York, 2003)
Google ученый
E.Brandl, A. Schoberth, C. Leyens, Mater. Sci. Англ. А 532 , 295 (2012)
CAS Google ученый
H.M. Ван, С.К. Чжан, X.M. Ван, Чин. J. Лазеры 36 , 3204 (2009)
Google ученый
F.G. Arcella, F.H. Froes, JOM 52 , 28 (2000)
CAS Google ученый
H.Галаррага, Р.Дж. Уоррен, Д.А. Ладос, Р.Р. Дехофф, М. Кирка, П. Нандвана, Mater. Sci. Англ. А 685 , 417 (2017)
CAS Google ученый
А. Митчелл, Mater. Sci. Англ. А 243 , 257 (1998)
Google ученый
W.E. Frazier, J. Mater. Англ. Выполнять. 23 , 1917 (2014)
CAS Google ученый
B.Бауфельд, О. Ван дер Бист, Р. Голт, Mater. Des. 31 , S106 (2010)
CAS Google ученый
B. Dutta, F.H.S. Froes, Met. Порошковая Реп. 72 , 1 (2017)
Google ученый
ASTM F2792-12a, Стандартная терминология для технологий аддитивного производства, F42.19, Ed. (ASTM International, West Conshohocken). https: // doi.org / 10.1520 / F2792-12A
А. Хейдарзаде, Х. Пуралиакбар, С. Махдави, М. Р. Джандаги, Ceram. Int. 44 , 3128 (2018)
CAS Google ученый
И. Гибсон, Д.У. Розен, Б. Стакер, Технологии аддитивного производства (Спрингер, Нью-Йорк, 2010)
Google ученый
B. Onuike, A. Bandyopadhyay, Mater.Lett. 252 , 256 (2019)
CAS Google ученый
Л. Хитцлер, М. Меркель, В. Холл, А. Экснер, Adv. Англ. Mater. 20 , 1700658 (2018)
Google ученый
S.L. Пой, W.Y. Yeong, F.E. Wiria, J. Alloy. Compd. 660 , 461 (2016)
КАС Google ученый
Q.Цзя, Д. Гу, Дж. Сплавы Compd. 585 , 713 (2014)
КАС Google ученый
Ю. Куо, А. Камигаичи, К. Какехи, Металл. Mater. Пер. А 49 , 3831 (2018)
CAS Google ученый
А. Сабури, Ф. Босио, Э. Либрера, М. Де Кирико, С. Биамино, М. Ломбарди, П. Фино, в размере 90 187 евро PM2018 Congr. Exhebition (Бильбао, Испания, 2018), стр.1–6
Ф. Босио, А. Сабури, А. Лаканьина, Э. Либрера, М. Де Кирико, С. Биамино, П. Фино, М. Ломбарди, в 90 187 евро PM2018 Congr. Выставка (Бильбао, Испания, 2018), стр. 1–6
А. Сабури, А. Аверса, Ф. Босио, Э. Бассини, Э. Либрера, М. Де Кирико, С. Биамино , Д. Угуз, П. Фино, М. Ломбарди, Mater. Sci. Англ. А 766 , 138360 (2019)
CAS Google ученый
А.Saboori, A. Aversa, G. Marchese, S. Biamino, M. Lombardi, P. Fino, Appl. Sci. 9 , 3316 (2019)
Google ученый
G. Marchese, S. Parizia, M. Rashidi, A. Saboori, D. Manfredi, D.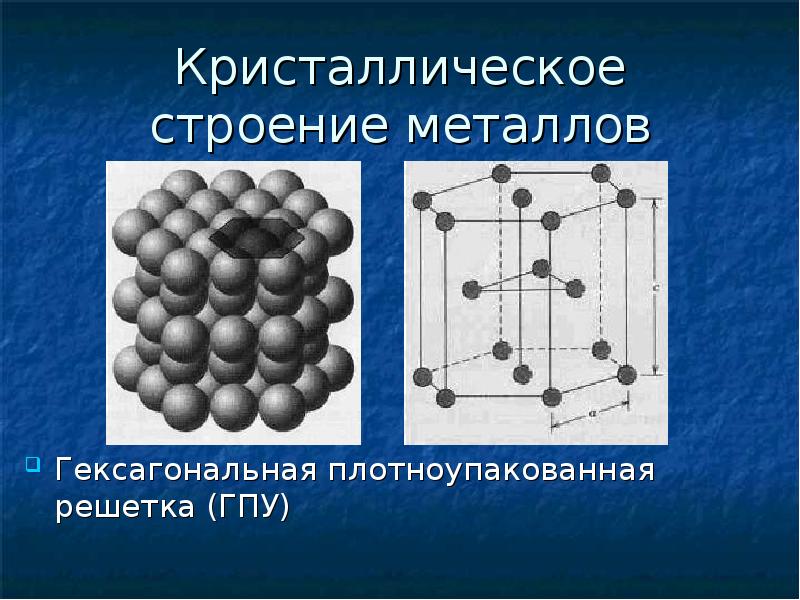 Ugues, M. Lombardi, E. Hryha, S. Biamino, Mater. Sci. Англ. A 769 , 138500 (2020)
Ugues, M. Lombardi, E. Hryha, S. Biamino, Mater. Sci. Англ. A 769 , 138500 (2020)
CAS Google ученый
T.T. Wohlers, Отчет Wohlers за 2006 г .: Состояние отрасли в области быстрого прототипирования и производства: Ежегодный отчет о мировом прогрессе (Wohlers Associates, Fort Collins, 2006)
Google ученый
С.Мари, Rapid Prototyp. J. 19 , 365 (2013)
Google ученый
A.Y. Албагачиев, А. Краско, Н. Баранова, Е. Страмцова, А.А. Мокану, Рус. Англ. Res. 38 , 687 (2018)
Google ученый
С. Биамино, А. Пенна, У. Аккелид, С. Саббадини, О. Тасса, П. Фино, М. Павезе, П. Дженнаро, К. Бадини, Интерметаллиды 19 , 776 ( 2011)
CAS Google ученый
А.Ataee, Y. Li, D. Fraser, G. Song, C. Wen, Mater. Des. 137 , 345 (2018)
КАС Google ученый
М. Тернер, С. Биамино, П. Эпикоко, А. Пенна, О. Хедин, С. Саббадини, П. Фино, М. Павезе, У. Аккелид, П. Дженнаро, Ф. Пелиссеро , К. Бадини, Steel Res. Int. 83 , 943 (2012)
КАС Google ученый
Y. Zhong, L.E. Раннар, Л.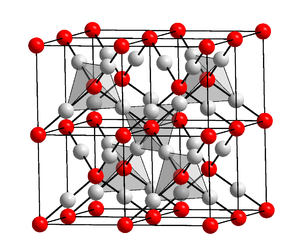 Liu, A. Koptyug, S. Wikman, J. Olsen, D. Cui, Z. Shen, J. Nucl. Mater. 486 , 234 (2017)
Liu, A. Koptyug, S. Wikman, J. Olsen, D. Cui, Z. Shen, J. Nucl. Mater. 486 , 234 (2017)
CAS Google ученый
Д. Кормье, О. Харриссон, Х. Уэст, Rapid Prototyp. J. 10 , 35 (2004)
Google ученый
Я. Чжай, Х. Галаррага, Д.А. Ладос, Тр. Англ. 114 , 658 (2015)
КАС Google ученый
G.Baudana, S. Biamino, D. Ugues, M. Lombardi, P. Fino, M. Pavese, C. Badini, Met. Порошковая Реп. 71 , 193 (2016)
Google ученый
К. Кизиол, Ł. Kaczmarek, G. Brzezinka, A. Kyzioł, Chem. Англ. J. 240 , 516–526 (2014)
Google ученый
М. Ларссон, У. Линд, О. Харриссон, в ежегодном международном симпозиуме по изготовлению твердых тел произвольной формы (2003), стр.438
С. Прайс, Дж. Лайдон, К. Купер, К. Чоу, в Труды Международного конгресса и выставки по машиностроению ASME 2014. Том 2A: Advanced Manufacturing , Монреаль, Квебек, Канада, 14–20 ноября 2014 г. V02AT02A002 (ASME)
К. Кёрнер, Э. Аттар, П. Хейнл, Дж. Матер. Процесс. Technol. 211 , 978 (2011)
Google ученый
Дж.Milberg, M. Sigl, Prod. Англ. 2 , 117 (2008)
Google ученый
М. Галац, Л. Юлиано, Addit. Manuf. 19 , 1–20 (2018)
Google ученый
E. Attar, Simul. Sel. Электронно-лучевой расплав. Процесс. 211 , 978 (2011)
Google ученый
А.Сафдар, Л. Wei, A. Snis, Z. Lai, Mater. Charact. 65 , 8 (2012)
КАС Google ученый
W.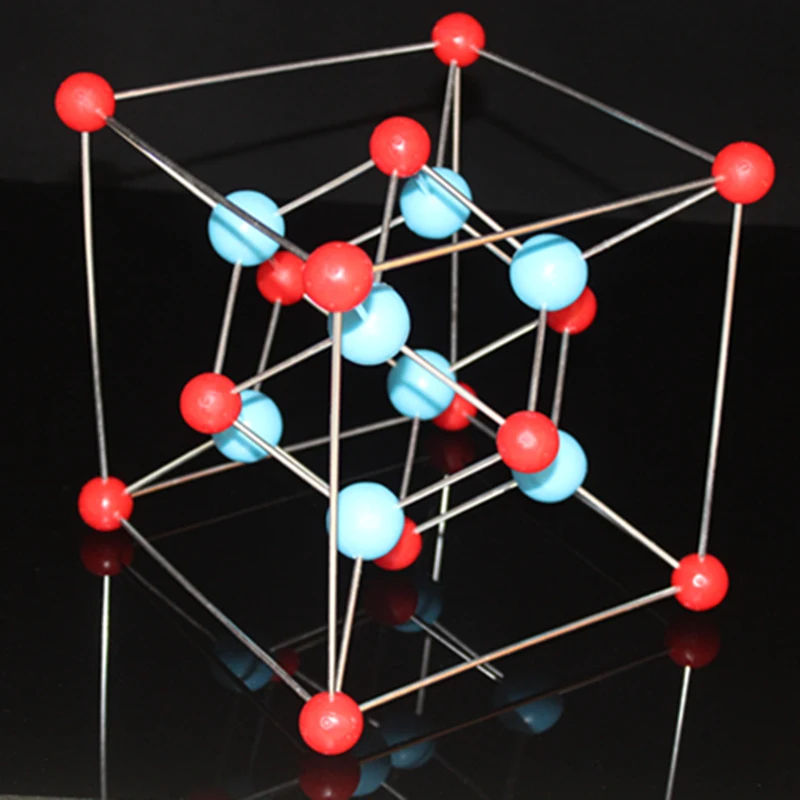 He, W. Jia, H. Liu, H. Tang, X. Kang, Y. Huang, X. Jinshu, X. Jinshu, Xiyou Jinshu Cailiao Yu Gongcheng / Rare Met. Mater. Англ. 40 , 2072 (2011)
He, W. Jia, H. Liu, H. Tang, X. Kang, Y. Huang, X. Jinshu, X. Jinshu, Xiyou Jinshu Cailiao Yu Gongcheng / Rare Met. Mater. Англ. 40 , 2072 (2011)
CAS Google ученый
Т. Р. Махале, Электронно-лучевая плавка современных материалов и конструкций, массовая настройка, массовая персонализация.Кандидатская диссертация, Промышленная инженерия, Роли, 2009
S.M. Гайтан, Л. Мурр, Ф. Медина, Э. Мартинес, М.И. Lopez, R.B. Wicker, Mater. Technol. 24 , 180 (2009)
КАС Google ученый
П. Хайнл, А. Роттмайр, К. Кёрнер, Р.Ф. Певица, адв. Англ. Mater. 9 , 360 (2007)
CAS Google ученый
H.Р.В. Попов, А. Кац-Демьянец, А. Гаркун, Г. Мюллер, Э. Строкин, В. Попов, А. Кац-Демьянец, А. Гаркун, Г. Мюллер, Э. Строкин, Х. Розенсон, Proc. Manuf. 21 , 125–132 (2018)
Google ученый
Э. Эрнандес-Нава, К. Дж. Смит, Ф. Дергути, С. Таммас-Вильямс, Ф. Леонар, П. Дж. Уизерс, И. Тодд, Р. Гудолл, Acta Mater. 108 , 279 (2016)
Google ученый
Т.Персено, Дж. Мартин, Р. Дендивель, Дж. Я. Buffiére, E. Maire, Mater. Charact. 143 , 82 (2018)
CAS Google ученый
R. Cunningham, A.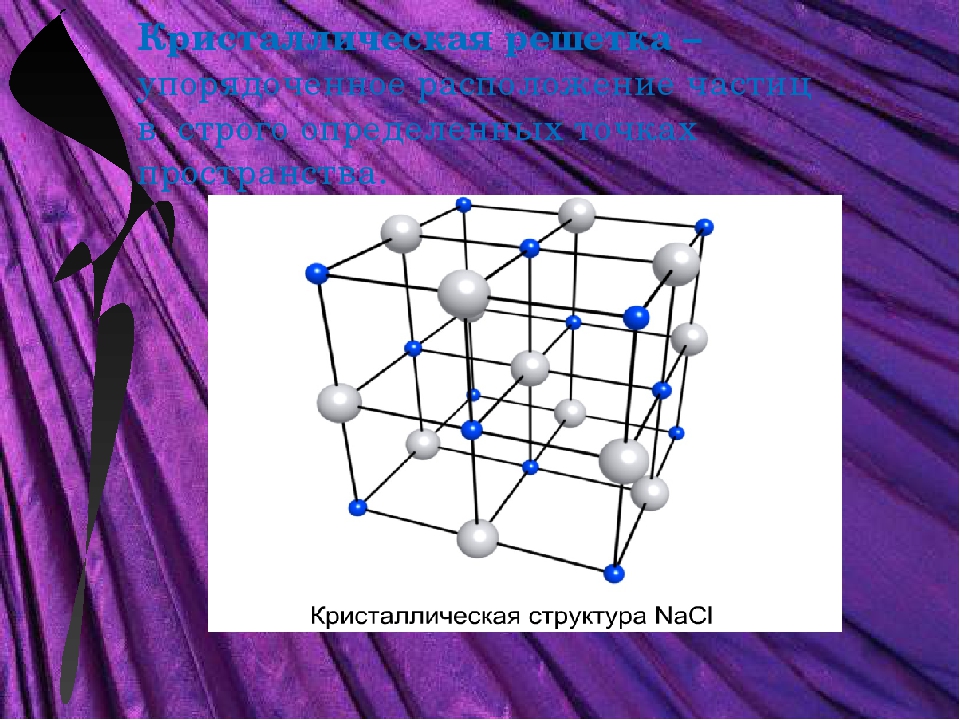 Nicolas, J. Madsen, E. Fodran, E. Anagnostou, M.D. Sangid, A.D. Rollett, Mater. Res. Lett. 5 , 516 (2017)
Nicolas, J. Madsen, E. Fodran, E. Anagnostou, M.D. Sangid, A.D. Rollett, Mater. Res. Lett. 5 , 516 (2017)
CAS Google ученый
С. Таммас-Уильямс, П.Дж. Уизерс, И. Тодд, П.Б. Прангнелл, Металл. Mater. Пер. А 47 , 1939 (2016)
CAS Google ученый
А. Хорасани, И. Гибсон, М. Голдберг, Г. Литтлфейр, Rapid Prototyp. J. 23 , 295 (2017)
Google ученый
A. Saboori, S. Tusacciu, M. Busatto, M. Lai, S. Biamino, P. Fino, M. Lombardi, J. Vis. Exp. 2018 , e56966 (2018)
Google ученый
Л.Э. Мурр, С.А. Хинонес, С.М. Гайтан, М. Лопес, А. Родела, Э.Ю. Martinez, D.H. Hernandez, E. Martinez, F. Medina, R.B. Wicker, J. Mech. Behav. Биомед. Mater. 2 , 20 (2009)
КАС Google ученый
Л.Дж. Гибсон, М.Ф. Ashby, Ячеистые твердые вещества: структура и свойства (Cambridge University Press, Кембридж, 1999)
Google ученый
Н.А. Флек, В. Дешпанде, М.Ф. Эшби, Proc. R. Soc. Математика. Phys. Англ. Sci. 466 , 2495 (2010)
КАС Google ученый
М. Суард, Г. Мартин, П. Люисье, Р.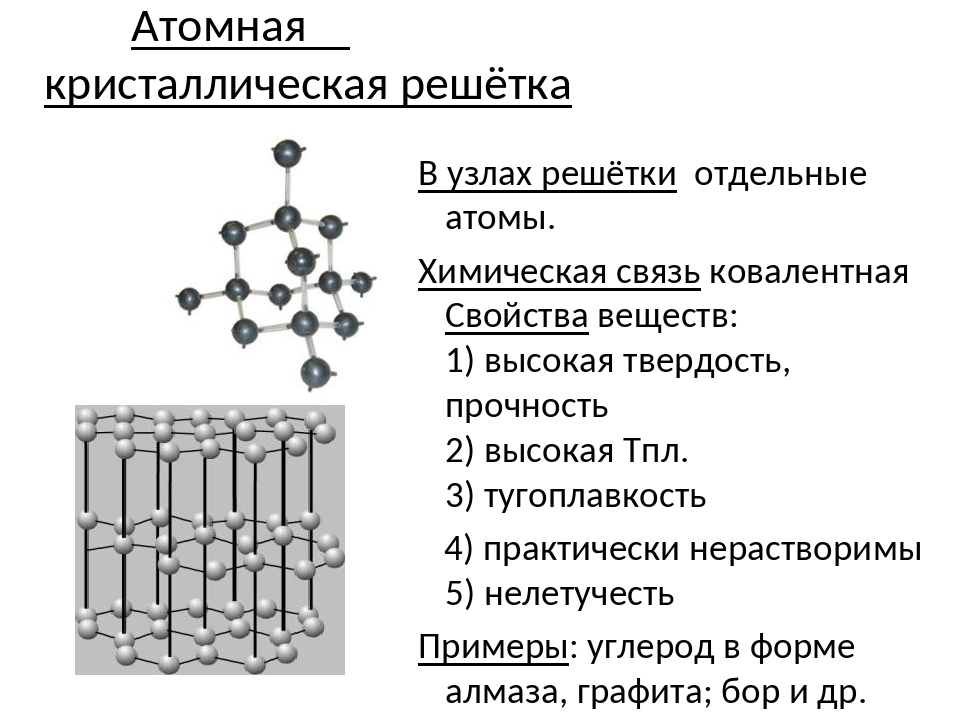 Дендивель, Ф. Винья, Дж. Дж. Blandin, F. Villeneuve, Addit. Manuf. 8 , 124 (2015)
Дендивель, Ф. Винья, Дж. Дж. Blandin, F. Villeneuve, Addit. Manuf. 8 , 124 (2015)
Google ученый
K.J. Мэлони, К. Финк, Т. Шедлер, Дж. Колодзейская, А.J. Jacobsen, C.S. Roper, Int. J. Heat Mass Transf. 55 , 2486 (2012)
КАС Google ученый
A.G. Evans, J.W. Хатчинсон, М.Ф. Эшби, Прог. Mater Sci. 43 , 171 (1998)
КАС Google ученый
G.W. Коойстра, В. Deshpande, H.N.G. Уодли, Acta Mater. 52 , 4229 (2004)
КАС Google ученый
Л.Э. Мурр, С. Гайтан, Ф. Медина, Х. Лопес, Э. Мартинес, Б.И. Мачадо, Д.Х. Эрнандес, Л. Мартинес, М.И. Lopez, R.B. Wicker, J. Bracke, Philos. Пер. R. Soc. Математика. Phys. Англ. Sci. 368 , 1999 (2010)
CAS Google ученый
М. Нииноми, Металл. Mater. Пер. А 33 , 477 (2002)
Google ученый
J.W. Парк, Х.К. Ким, Ю.Дж. Ким, Дж. Х. Джанг, Х. Сонг, Т. Ханава, Acta Biomater. 6 , 2843 (2010)
КАС Google ученый
Ф. Калиньяно, М. Галати, Л. Юлиано, П. Минетола, Дж. Хелс. Англ. 2019 , 9748212 (2019)
2019 , 9748212 (2019)
Google ученый
П. Хайнл, Л. Мюллер, К. Кёрнер, Р.Ф. Зингер, Ф.А.Мюллер, Acta Biomater. 4 , 1536 (2008)
CAS Google ученый
X.Y. Cheng, S.J. Ли, Л. Мурр, З.Б. Чжан, Ю.Л. Hao, R. Yang, F. Medina, R.B. Wicker, J. Mech. Behav. Биомед. Mater. 16 , 153 (2012)
КАС Google ученый
J. Parthasarathy, B. Starly, S. Raman, A. Christensen, J. Mech. Behav. Биомед. Mater. 3 , 249 (2010)
Google ученый
О. Джансизоглу, О. Харриссон, Д. Кормье, Х.West, T. Mahale, Mater. Sci. Англ. А 492 , 468 (2008)
Google ученый
W. van Grunsven, E. Hernandez-Nava, G. Reilly, R. Goodall, Metals (Basel) 4 , 401 (2014)
Google ученый
Л. Сяо, В. Сун, К. Ван, Х. Лю, Х. Тан, Дж. Ван, Mater. Sci. Англ. А 640 , 375 (2015)
CAS Google ученый
М.Jamshidinia, L. Wang, W. Tong, R. Kovacevic, J. Mater. Процесс. Technol. 214 , 1728 (2014)
КАС Google ученый
S.J. Ли, Л. Мурр, X.Y. Ченг, З.Б. Чжан, Ю.Л. Хао, Р. Ян, Ф. Медина, Р. Б. Уикер, Acta Mater. 60 , 793 (2012)
CAS Google ученый
L.E. Мурр, С. Гайтан, Ф. Медина, Э. Мартинес, Х.Л. Мартинес, Д.Х. Эрнандес, Б.И. Мачадо, Д.А. Рамирес, R.B. Wicker, Mater. Sci. Англ. А 527 , 1861 (2010)
Google ученый
М.Ф. Эшби, Филос. Пер. R. Soc. Математика. Phys. Англ. Sci. 364 , 15 (2006)
CAS Google ученый
В.С. Дешпанде, М.Ф. Эшби, Н.А.Флек, Acta Mater. 49 , 1035 (2001)
КАС Google ученый
Дж.К. Максвелл, Dublin Philos. Mag. J. Sci. 27 , 294 (1864)
Google ученый
Э. Эрнандес-Нава, К. Дж. Смит, Ф. Дергути, С. Таммас-Вильямс, Ф. Леонар, П. Дж. Уизерс, И. Тодд, Р. Гудолл, Acta Mater. 85 , 387 (2015)
Google ученый
A. Mortensen, Y. Conde, A. Rossoll, C.S. Marchi, J. Mater. Sci. 48 , 8140 (2013)
КАС Google ученый
Т.Дж. Хорн, О.Л.А. Гарриссон, Д.Дж. Марселлин-Литтл, Х.А. West, B.D.X. Lascelles, R. Aman, Addit. Manuf. 1 , 2 (2014)
Google ученый
З. Фанг, Б. Старли, В. Сан, Comput. Des. 37 , 65 (2005)
Google ученый
Б. Старли, А. Лау, В. Сан, В. Лау, Т. Брэдбери, Comput. Des. 37 , 387 (2005)
Google ученый
Дж.Parthasarathy, B. Starly, S. Raman, J. Manuf. Процесс. 13 , 160 (2011)
Google ученый
М. Джамшидиния, Л. Ван, В. Тонг, Р. Аджлуни, Р. Ковачевич, J. Mater. Процесс. Technol. 226 , 255 (2015)
КАС Google ученый
G. Epasto, G. Palomba, D.D. Андреа, Э. Гульельмино, С. Ди, Ф. Трайна, Mater. Sci. Англ. А 753 , 31 (2019)
CAS Google ученый
Л.Ян, Быстрый прототип. J. 21 , 329e39 (2015)
Google ученый
Л. Сяо, В. Сун, К. Ван, Х. Тан, К. Фань, Н. Лю, Дж. Ван, Int. J. Impact Eng. 100 , 75 (2017)
Google ученый
М. Карл, Дж. Р. Келли, Dent. Mater. 25 , 1426 (2009)
КАС Google ученый
М.Галати, П. Минетола, Г. Рицца, Материалы (Базель) 12 , 2211 (2019)
CAS Google ученый
Ю.Г. Сан, С. Гулиция, С. О, Д. Фрейзер, М. Лири, Ю.Ф. Ян, М. Цянь, JOM 68 , 791 (2016)
Google ученый
M. Suard, P. Lhuissier, R. Dendievel, J.J. Бланден, Ф. Винья, Ф. Вильнев, Powder Metall. 57 , 190 (2014)
КАС Google ученый
К.С. Чан, М. Койке, Р. Л. Мейсон, Т. Окабе, Металл. Mater. Пер. А 44 , 1010 (2013)
CAS Google ученый
ASTM, i , 1 (2019)
С. Таммас-Уильямс, П.Дж. Уизерс, И. Тодд, П.Б. Prangnell, Scr. Mater. 122 , 72 (2016)
КАС Google ученый
К. Де Формануар, С. Мишотт, О.Риго, Л. Жермен, С. Годе, Mater. Sci. Англ. А 652 , 105 (2016)
Google ученый
Температурные изменения кристаллической структуры оксида бария-титана по JSTOR
Оксид бария-титана, который при комнатной температуре является тетрагональным, при температуре около 120 ° C принимает кубическую структуру. Это изменение было подробно отслежено с помощью порошковых рентгеновских снимков, сделанных на расстоянии 19 см. порошковая камера с интервалом в несколько градусов в диапазоне, охватывающем точку перехода. Элементарная ячейка, которая содержит формулу числа атомов, сохраняет свою идентичность на протяжении всего перехода, а атомные параметры не меняются. Изменение заключается просто в осевых длинах, и они непрерывно изменяются с температурой, хотя и не линейно, причем изменение становится более быстрым вблизи точки перехода. В то время как коэффициенты линейного расширения вдоль и перпендикулярно оси тетрад велики и имеют противоположный знак, коэффициент объемного расширения мал и положителен. Нет скачкообразного изменения ни линейного расстояния, ни объема, обнаруживаемого в точке перехода, но есть резкий скачок в коэффициентах линейного расширения и заметное увеличение коэффициента объемного расширения, которое, вероятно, хотя и не определенно, является прерывистым.Переход предполагает типичное изменение λ-точки. Удельная теплоемкость не определена, но кривая теплового расширения имеет характерную форму λ. Сосуществование кубических и тетрагональных структур в пропорциях, зависящих от температуры, происходит в диапазоне нескольких градусов вблизи точки перехода и объясняется влиянием локальных напряжений, облегчающих или затрудняющих изменение между двумя структурами, разность энергий которых составляет очень мало в этом диапазоне температур.
Элементарная ячейка, которая содержит формулу числа атомов, сохраняет свою идентичность на протяжении всего перехода, а атомные параметры не меняются. Изменение заключается просто в осевых длинах, и они непрерывно изменяются с температурой, хотя и не линейно, причем изменение становится более быстрым вблизи точки перехода. В то время как коэффициенты линейного расширения вдоль и перпендикулярно оси тетрад велики и имеют противоположный знак, коэффициент объемного расширения мал и положителен. Нет скачкообразного изменения ни линейного расстояния, ни объема, обнаруживаемого в точке перехода, но есть резкий скачок в коэффициентах линейного расширения и заметное увеличение коэффициента объемного расширения, которое, вероятно, хотя и не определенно, является прерывистым.Переход предполагает типичное изменение λ-точки. Удельная теплоемкость не определена, но кривая теплового расширения имеет характерную форму λ. Сосуществование кубических и тетрагональных структур в пропорциях, зависящих от температуры, происходит в диапазоне нескольких градусов вблизи точки перехода и объясняется влиянием локальных напряжений, облегчающих или затрудняющих изменение между двумя структурами, разность энергий которых составляет очень мало в этом диапазоне температур. При температуре ниже комнатной, наблюдения, проведенные до -183 ° C, предполагают, что структура может иметь вторую точку перехода где-то ниже и снова стать кубической, причем изменение имеет ту же природу, что и при 120 ° C.Утверждается, что структура при комнатной температуре может быть объяснена только существованием направленных связей, и что разрыв этих связей с повышением температуры ответственен за переход на 120 ° C. Низкотемпературный переход объясняется постулированием более полного набора связей, вероятно, октаэдрического комплекса, который частично разрушается при этой температуре с образованием квадрата, наблюдаемого в структуре при комнатной температуре. Качественно обсуждается возможная природа направленных связей.Условием, которое делает возможным образование таких связей, вероятно, является аномальный объем, доступный для атома Ti, что связано с влиянием большого иона Ba на разрушение кислородной решетки. Система направленных связей будет вносить лишь небольшую часть в энергию притяжения решетки, которая в основном носит ионный характер.
При температуре ниже комнатной, наблюдения, проведенные до -183 ° C, предполагают, что структура может иметь вторую точку перехода где-то ниже и снова стать кубической, причем изменение имеет ту же природу, что и при 120 ° C.Утверждается, что структура при комнатной температуре может быть объяснена только существованием направленных связей, и что разрыв этих связей с повышением температуры ответственен за переход на 120 ° C. Низкотемпературный переход объясняется постулированием более полного набора связей, вероятно, октаэдрического комплекса, который частично разрушается при этой температуре с образованием квадрата, наблюдаемого в структуре при комнатной температуре. Качественно обсуждается возможная природа направленных связей.Условием, которое делает возможным образование таких связей, вероятно, является аномальный объем, доступный для атома Ti, что связано с влиянием большого иона Ba на разрушение кислородной решетки. Система направленных связей будет вносить лишь небольшую часть в энергию притяжения решетки, которая в основном носит ионный характер.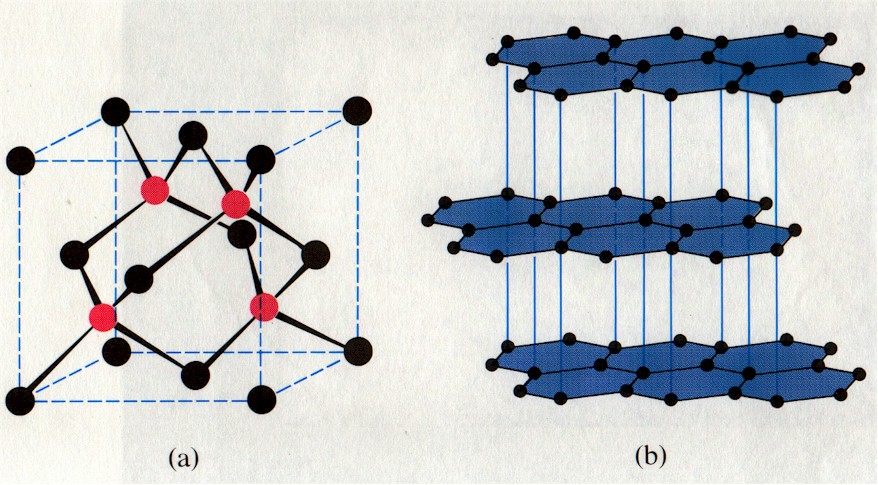 Гипотеза о существовании направленных связей независимо от их происхождения используется для предварительного объяснения аномальных вариаций интенсивности рентгеновских линий, наблюдаемых при температурах вблизи точки перехода.
Гипотеза о существовании направленных связей независимо от их происхождения используется для предварительного объяснения аномальных вариаций интенсивности рентгеновских линий, наблюдаемых при температурах вблизи точки перехода.
Королевское общество — это самоуправляемое товарищество, объединяющее самых выдающихся ученых мира, представляющих все области науки, техники и медицины, и старейшую научную академию, которая постоянно существует. Основная цель Общества, отраженная в его учредительных документах 1660-х годов, заключается в признании, продвижении и поддержке передового опыта в науке, а также в поощрении развития и использования науки на благо человечества. Общество сыграло свою роль в некоторых из самых фундаментальных, значительных и изменяющих жизнь открытий в истории науки, и ученые Королевского общества продолжают вносить выдающийся вклад в науку во многих областях исследований.
.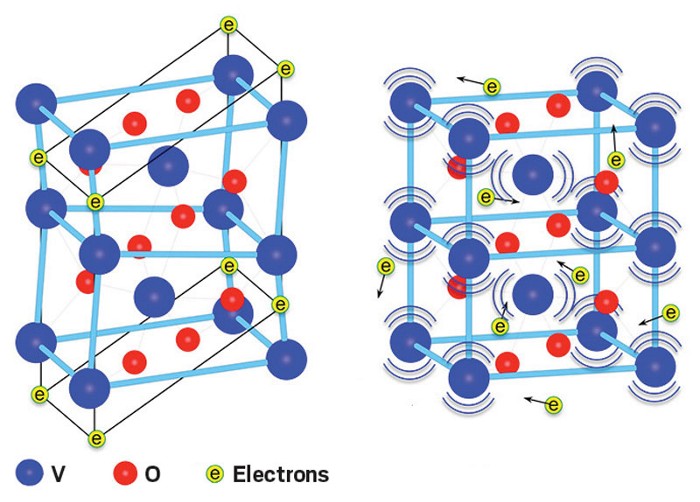

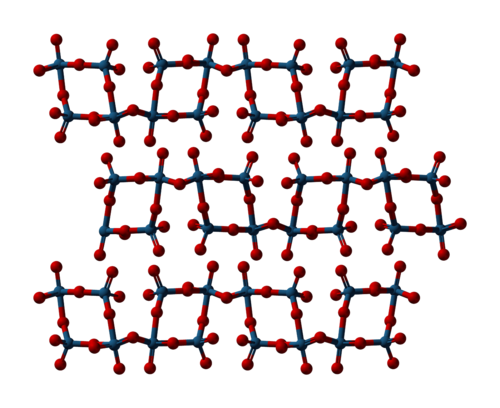
 74; атомов в элементарной ячейке: 6.
74; атомов в элементарной ячейке: 6.