Медь. Сплавы меди. Свойства и применение.
Знакомство человека с медью исчисляется тысячелетиями, где ее прямым конкурентом может выступать только золото, успевшее приобрести статус благородного металла.
Свойства меди и место в жизни человека
В чистом состоянии, элемент таблицы Менделеева, именуемый Cu, встречается крайне редко. Это – пластичный металл с легким розовым оттенком. Человеку же он знаком под другим цветом: желто-красным, чаще коричнево-красным. Это связано с высокой окислительной способностью вещества. Попадая на воздух, медь покрывается тонкой оксидной пленкой, что и делает цвет металла ближе к красному.

медь в чистом виде
Первобытная тяга человека к меди основывалась на свойстве пластичности, позволяющей придавать этому металлу требуемую форму путем несложной обработки. Медь легко поддается гравировке, нанесению резьбы, оставаясь при этом достаточно прочным. Современная ценность меди, как металла – высокие показатели проводимости: электрической и тепловой. Подобная информация позволяет выделить основные направления поиска этого цветного металла в виде отходов и лома.
Удельный вес меди, составляющий округленно 8.9 г/см3, также полезен сборщику металлолома. Зная объем собранного лома, в частности проводов, жил, легко рассчитать его оценочный вес.
Сплавы меди
Помимо относительно чистой формы, характеризуемой ничтожным содержанием примесей, медь – составляющий элемент многих сплавов, среди которых наиболее известны:

Латунь — сплав меди

Бронза

Мельхиор — больше относится к серебру, нежели к меди
Отдельно стоит выделить медный сплав с никелем, именуемый мельхиор. Он известен широкой аудитории по разменным монетам советских времен, начиная с 10 копеек а также подарочные наборы столовых приборов, но существенно уступает первым двум в степени востребованности.
Наиболее перспективными для нужд человека остаются: латунь и бронза. Желтая медь, так иначе называют латунь, на бытовом уровне широко востребована в сантехнике. Те, кто сталкивался с подбором крана или смесителя, хорошо знают это. По химическому составу различают:
- двойные латуни – сплав меди с цинком;
- многокомпонентные, в которых Zn остается основным легирующим элементом.
Процентное содержание цинка, даже в двойной латуни, широко варьируется. Сплавы, где доля Zn составляет не более 20%, именуют томпаком.

Пули из томпака
Определить состав латуни можно исходя из маркировки: для двойных сплавов после буквы «Л» указывается процентное содержание меди, например Л60. Маркировка многокомпонентных сплавов строится аналогично, только за «Л» следуют легирующие примеси с их концентрациями. Таким образом, многокомпонентная латунь марки ЛМц58- 2, использования при изготовлении деталей машин, гаек, болтом, арматуры, подразумевает содержание меди – 58%, цинка – 40%, марганца – 2%.
Бронза – в стандартном понимании, представляет медный сплав с оловом, однако на практике также обладает весьма вариативным составом. Фактически под бронзой принято понимать любой медный сплав, где никель и цинк не являются основными легирующими элементами. Стоит отметить, что найти оловянную бронзу достаточно сложно. Большее распространение получили ее безоловянные сорта.
Медь и ее сплавы, как источник цветного вторичного металла
Взвешивая «чистый» металл и его сплавы на весах прибыльности при сдаче металлолома, можно сказать, что стоимость первого в полтора – два раза выше. Однако весовое содержание меди в металлических конструкциях часто уступает на выходе ее сплавам.
Так, медные сплавы можно обнаружить среди пришедших в негодность изделий сантехники: водопроводные краны, вентили, душевые шланги и трубки. Многие старые светильники, дверная фурнитура также изготовлены из медных сплавов, однако верх пьедестала, по весовому содержанию, занимают радиаторы отопления.
Непосредственно медь стоит искать среди бытовых приборов, желательно уже выработавших свой эксплуатационный ресурс:
- ламповый телевизор — 1,5 кг;

Ламповый телевизор с медью
- полупроводниковый ТВ приемник – 0,5 кг;
- компрессионный холодильник – около килограмма в двигателе, еще столько же могут содержать трубки радиатора;
Незаслуженно обходят вниманием магнитные пускатели, хотя оборудование помимо обмотки содержит медь в шинах. Небольшое содержание металла, менее килограмма принесут автомобильные стартеры и генераторы, дроссели люминесцентных ламп, трансформаторы, реле, компрессоры холодильников.
Смотрите статью — Где искать металлолом меди?
Первичная медь, получение и применение
В зависимости от чистоты металла, различают следующие марки:

Катодная медь М0
Одним из источников сырья для получения металла выступает медный лом, перерабатываемый согласно технологии огневого рафинирования.
Природные ресурсы металла составляет самородная медь и сульфидные руды, в частности медные колчедан и блеск. Существует два металлургических способа получения металла из руды. На основной метод – пирометаллургический, приходится 90% первичного металла, оставшиеся 10% – результат гидрометаллургической технологии.

Медная руда
Физические свойства меди не могли остаться незамеченными в промышленности. Ее высокая электропроводность позволяет использовать металл при изготовлении электродов, проводов, особенно силовых кабелей (марка М0). Относительная химическая инертность меди нашла применение металлу в узлах аппаратуры для работы с огнеопасными веществами.
Высокая теплопроводность металла, наряду с устойчивостью к коррозии, используются при изготовлении сантехнических конструкций, узлов, а также кровельных покрытий. В настоящее время, медь вытеснили тут другие, более дешевые материалы.
Достаточно широкий рынок применения меди — производство сплавов. Латунь и бронза, где Cu является основным компонентом, уже были рассмотренные ранее. Широко используется другой сплав дюралюминий, где содержание меди доходит до 5%.
xlom.ru
Медь. Описание, свойства, происхождение и применение металла

Самородная медь размером около 4 см
Медь — минерал из класса самородных элементов. В природном минерале обнаруживаются Fe, Ag, Au, As и другие элементы в виде примеси или образующие с Cu твёрдые растворы. Простое вещество медь — это пластичный переходный металл золотисто-розового цвета (розового цвета при отсутствии оксидной плёнки). Один из первых металлов, широко освоенных человеком из-за сравнительной доступности для получения из руды и малой температуры плавления. Он входит в семёрку металлов, известных человеку с очень древних времён. Медь является необходимым элементом для всех высших растений и животных.
СТРУКТУРА
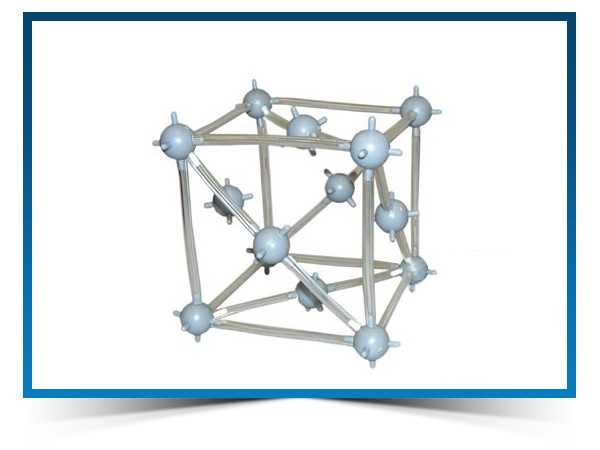
Кристаллическая структура меди
Кубическая сингония, гексаоктаэдрический вид симметрии m3m, кристаллическая структура — кубическая гранецентрированная решётка. Модель представляет собой куб из восьми атомов в углах и шести атомов , расположенных в центре граней (6 граней). Каждый атом данной кристаллической решетки имеет координационное число 12. Самородная медь встречается в виде пластинок, губчатых и сплошных масс, нитевидных и проволочных агрегатов, а также кристаллов, сложных двойников, скелетных кристаллов и дендритов. Поверхность часто покрыта плёнками «медной зелени» (малахит), «медной сини» (азурит), фосфатов меди и других продуктов её вторичного изменения.
СВОЙСТВА
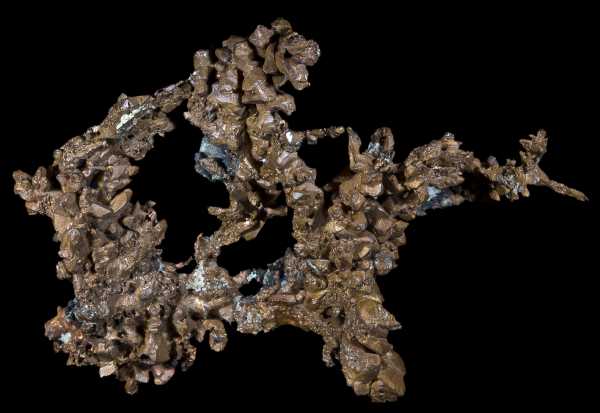
Кристаллы самородной меди, Верхнее озеро, округ Кинави, Мичиган, США. Размер 12 х 8,5 см
Медь — золотисто-розовый пластичный металл, на воздухе быстро покрывается оксидной плёнкой, которая придаёт ей характерный интенсивный желтовато-красный оттенок. Тонкие плёнки меди на просвет имеют зеленовато-голубой цвет.
Наряду с осмием, цезием и золотом, медь — один из четырёх металлов, имеющих явную цветовую окраску, отличную от серой или серебристой у прочих металлов. Этот цветовой оттенок объясняется наличием электронных переходов между заполненной третьей и полупустой четвёртой атомными орбиталями: энергетическая разница между ними соответствует длине волны оранжевого света. Тот же механизм отвечает за характерный цвет золота.
Медь обладает высокой тепло- и электропроводностью (занимает второе место по электропроводности среди металлов после серебра). Удельная электропроводность при 20 °C: 55,5-58 МСм/м. Медь имеет относительно большой температурный коэффициент сопротивления: 0,4 %/°С и в широком диапазоне температур слабо зависит от температуры. Медь является диамагнетиком.
Существует ряд сплавов меди: латуни — с цинком, бронзы — с оловом и другими элементами, мельхиор — с никелем и другие.
ЗАПАСЫ И ДОБЫЧА

Образец меди, 13,6 см. Полуостров Кинави, Мичиган, США
Среднее содержание меди в земной коре (кларк) — (4,7-5,5)·10−3% (по массе). В морской и речной воде содержание меди гораздо меньше: 3·10−7% и 10−7
Медь получают из медных руд и минералов. Основные методы получения меди — пирометаллургия, гидрометаллургия и электролиз. Пирометаллургический метод заключается в получении меди из сульфидных руд, например, халькопирита CuFeS2. Гидрометаллургический метод заключается в растворении минералов меди в разбавленной серной кислоте или в растворе аммиака; из полученных растворов медь вытесняют металлическим железом.
ПРОИСХОЖДЕНИЕ

Небольшой самородок меди
Обычно самородная медь образуется в зоне окисления некоторых медносульфидных месторождений в ассоциации с кальцитом, самородным серебром, купритом, малахитом, азуритом, брошантитом и другими минералами. Массы отдельных скоплений самородной меди достигают 400 тонн. Крупные промышленные месторождения самородной меди вместе с другими медьсодержащими минералами формируются при воздействии на вулканические породы (диабазы, мелафиры) гидротермальных растворов, вулканических паров и газов, обогащенных летучими соединениями меди (например, месторождение озера Верхнее, США).
Самородная медь встречается также в осадочных породах, преимущественно в медистых песчаниках и сланцах.
Наиболее известные месторождения самородной меди — Туринские рудники (Урал), Джезказганское (Казахстан), в США (на полуострове Кивино, в штатах Аризона и Юта).
ПРИМЕНЕНИЕ

Браслеты из меди
Из-за низкого удельного сопротивления, медь широко применяется в электротехнике для изготовления силовых кабелей, проводов или других проводников, например, при печатном монтаже. Медные провода, в свою очередь, также используются в обмотках энергосберегающих электроприводов и силовых трансформаторов.
Другое полезное качество меди — высокая теплопроводность. Это позволяет применять её в различных теплоотводных устройствах, теплообменниках, к числу которых относятся и широко известные радиаторы охлаждения, кондиционирования и отопления.
В разнообразных областях техники широко используются сплавы с использованием меди, самыми широко распространёнными из которых являются упоминавшиеся выше бронза и латунь. Оба сплава являются общими названиями для целого семейства материалов, в которые помимо олова и цинка могут входить никель, висмут и другие металлы.
В ювелирном деле часто используются сплавы меди с золотом для увеличения прочности изделий к деформациям и истиранию, так как чистое золото очень мягкий металл и нестойко к этим механическим воздействиям.
Прогнозируемым новым массовым применением меди обещает стать её применение в качестве бактерицидных поверхностей в лечебных учреждениях для снижения внутрибольничного бактериопереноса: дверей, ручек, водозапорной арматуры, перил, поручней кроватей, столешниц — всех поверхностей, к которым прикасается рука человека.
Медь (англ. Copper) — Cu
| Молекулярный вес | 63.55 г/моль |
| Происхождение названия | От греческого «Kyprium», то есть «кипрский металл», по названию острова Кипр |
| IMA статус | действителен, описан впервые до 1959 (до IMA) |
КЛАССИФИКАЦИЯ
Hey’s CIM Ref1.1
| Strunz (8-ое издание) | 1/A.01-10 |
| Nickel-Strunz (10-ое издание) | 1.AA.05 |
| Dana (7-ое издание) | 1.1.1.3 |
| Dana (8-ое издание) | 1.1.1.3 |
ФИЗИЧЕСКИЕ СВОЙСТВА
| Цвет минерала | медно-красный, тускнеющий в черный или зеленый на воздухе |
| Цвет черты | медно-красный |
| Прозрачность | непрозрачный |
| Блеск | металлический |
| Спайность | нет |
| Твердость (шкала Мооса) | 2,5-3 |
| Прочность | ковкий |
| Излом | зазубренный |
| Плотность (измеренная) | 8.94 — 8.95 г/см3 |
| Радиоактивность (GRapi) | 0 |
| Магнетизм | диамагнетик |
ОПТИЧЕСКИЕ СВОЙСТВА
| Цвет в отраженном свете | розовато-белый |
| Плеохроизм | не плеохроирует |
| Люминесценция в ультрафиолетовом излучении | не флюоресцентный |
КРИСТАЛЛОГРАФИЧЕСКИЕ СВОЙСТВА
| Точечная группа | m3m (4/m 3 2/m) — гексоктаэдрический |
| Пространственная группа | Fm3m (F4/m 3 2/m) |
| Сингония | кубическая |
| Параметры ячейки | a = 3.615Å |
| Морфология | кубы, додекаэдры и тетрагексаэдры; редко октаэдры и сложные комбинации; нитевидные, древовидные |
| Двойникование | Двойники по {111} по шпинелевому закону |
Интересные статьи:
mineralpro.ru 28.07.2016mineralpro.ru
Лечебные свойства Меди. | Журнал Ярмарки Мастеров
Физиологическое воздействие наночастиц меди на организм человека
Медь – важный элемент жизни, она участвует во многих физиологических процессах. Среднее содержание меди в живом веществе 2•10–4%, известны организмы – концентраторы меди. В таежных и других ландшафтах влажного климата медь сравнительно легко выщелачивается из кислых почв, здесь местами наблюдается дефицит меди и связанные с ним болезни растений и животных (особенно на песках и торфяниках). В степях и пустынях, на участках месторождений меди наблюдается ее избыток в почвах и растениях, отчего болеют домашние животные.
Применение меди в медицине
В медицине медь в виде сульфата меди также применяется в качестве антисептического и вяжущего средства в виде глазных капель при конъюнктивитах и глазных карандашей для лечения трахомы. Раствор сульфата медь используют также при ожогах кожи фосфором. Иногда сульфат меди применяют как рвотное средство. Нитрат меди употребляют в виде глазной мази при трахоме и конъюнктивитах.
В 1893 году швейцарский ботаник Карл Негель доложил научному миру о своем открытии – антимикробном действии меди и серебра. Негели наблюдал гибель микроорганизмов в воде при концентрациях в ней металлов, составляющих миллионные доли от количества раствора, т.е. следовые. Эти свойства меди и серебра были названы олигодинамическими, от греческих слов «олигос» и «динамис». В буквальном переводе: «действие следа». Дальнейшими исследованиями было установлено, что наибольшим олигодинамическим действием обладает серебро. Действие меди в 4–5 раз слабее. Но взятые вместе, эти металлы многократно усиливают свойства друг друга. И свойства не только антимикробные.
Медь играет ключевую метаболическую роль в обмене веществ всех живых организмов, начиная от простейшей клетки. Она входит в состав биологических катализаторов – ферментов. Без них невозможна жизнь. Именно поэтому биологи назвали медь «металлом жизни». Прямо или косвенно медь участвует в большинстве обменных процессов и является их главным регулятором.
Основная биохимическая функция меди в организме – это участие в ферментативных реакциях в качестве активатора или в составе медьсодержащих ферментов. Количество меди в растениях колеблется от 0,0001 до 0,05% (на сухое вещество) и зависит от вида растения и содержания меди в почве. В растениях медь входит в состав ферментов-оксидаз и белка пластоцианина. В оптимальных концентрациях медь повышает холодостойкость растений, способствует их росту и развитию. Среди животных наиболее богаты медью некоторые беспозвоночные (у моллюсков и ракообразных в гемоцианине содержится 0,15–0,26% меди). Поступая с пищей, медь всасывается в кишечнике, связывается с белком сыворотки крови – альбумином, затем поглощается печенью, откуда в составе белка церулоплазмина возвращается в кровь и доставляется к органам и тканям.
Практически все заболевания связаны с нарушением обмена веществ. В одних случаях эти нарушения являются следствием болезни, а в других – причиной ее появления.
Уже в начале ХХ века всемирно известный врач – наш соотечественник Александр Залманов писал:
«Никогда не надо забывать, что болезни первоначально являются на деле только незначительным отклонением от физиологических процессов. Чтобы ликвидировать признаки болезни следует, в первую очередь, создать условия для улучшения обмена веществ. Вместо этого современная терапия при помощи антибиотиков охотится на микробов и, в то же время, культивирует «устойчивые» микробы и микозы. Реклама химической промышленности засыпает врачей предложениями бесчисленного множества новых антибиотиков. Это просто фармацевтическая вакханалия».
Слова эти, написанные почти сто лет назад, очень актуальны в наше время. Перспективен поиск лечебных средств, не вызывающих отрицательных побочных действий: снижения иммунитета, аллергических реакций, ухудшения генотипа, появления новых форм патогенных микроорганизмов. И в этом отношении терапия ионами меди и серебра является одним из перспективных лечебных средств антигомотоксической медицины (Антигомотоксическая медицина – совокупность лечебных средств и методов, направленных на выведение из организма человека вредных веществ – токсинов, с целью нормализации обменных процессов. В антигомотоксической медицине не используются средства способные вызывать нежелательные побочные явления.)
Медь – очень важный для жизни металл. Содержание меди в организме человека колеблется (на 100 г сухой массы) от 5 мг в печени до 0,7 мг в костях, в жидкостях тела – от 100 мкг (на 100 мл) в крови до 10 мкг в спинномозговой жидкости. А всего меди в организме взрослого человека около 100 мг. Медь входит в состав ряда ферментов – тирозиназы, цитохромоксидазы, стимулирует кроветворную функцию костного мозга.
Ежедневный прием меди с пищей составляет 0,50–6 мг, из которых усваивается только 30%. Токсическая доза меди больше 250 мг. Попав в организм, соединение меди поступает в печень, которая является главным складом этого микроэлемента. Медь концентрируется также в мозге, сердце и почках, мышечной и костной тканях. Многие растения и животные концентрируют медь, и лечебное действие при их использовании связано в большей мере с этим элементом. Наиболее богаты медью шампиньоны, картофель, печень (особенно палтуса и трески), почки, яичный желток, цельное зерно, а также устрицы и каракатицы. В молоке и молочных продуктах ее очень мало, поэтому длительный молочный рацион может привести к недостаточности меди в организме.
Малые дозы меди влияют на обмен углеводов в организме (снижение содержания сахара в крови), минеральных веществ (уменьшение в крови количества фосфора) и других. Увеличение содержания меди в крови приводит к превращению минеральных соединений железа в органические, стимулирует использование накопленного в печени железа при синтезе гемоглобина.
Недостаток меди в организме может спровоцировать следующие болезни:
• Анемию
• Бронхиальную астму
• Бронхит
• Витилиго
• Глаукому
• Дистрофию мышц
• Импотенцию с отсутствием сексуального влечения
• Ишемическую болезнь сердца
• Миопатию
• Невриты
• Остеопороз
• Псориаз
• Сахарный диабет
• Токсикоз беременности
• Туберкулез легких
• Эпилепсию
При этом потребность в меди увеличивается, особенно при следующих заболеваниях:
• Анемия
• Анкилозирующий спондилоартрит
• Антральный гастрит
• Атеросклероз
• Дуоденит
• Раковые заболевания
• Рахит
• Ревматоидный артрит
• Цирроз печени
• Язвенная болезнь желудка
Кроме этого, при недостатке меди злаковые растения поражаются так называемых болезнью обработки, плодовые – экзантемой; у животных уменьшаются всасывание и использование железа, что приводит к анемии, сопровождающейся поносом и истощением. Для этого применяются поливитамины с полиминералами, содержащими медь.
Особенно высока связь между дефицитом в организме меди и такими «болезнями века», как: ишемическая болезнь сердца, рак, сахарный диабет, инфаркт миокарда, ожирение. Недостаток меди отрицательно влияет на умственную и физическую активность. Потребность в меди возрастает у детей, беременных женщин, людей пожилого возраста, при стрессах, значительных физических и умственных нагрузках.
В большинстве случаев, во время патологических процессов, организм в ответ на болезнь отвечает повышением концентрации меди в крови. При этом используются депонированные запасы меди из печени. И хотя дефицит меди в организме – сравнительно редкое явление, всё же если болезнь затягивается или принимает хронический характер, запасы меди расходуются и наступает медедефицит. Необходимо его ликвидировать путем приема медьсодержащих препаратов. Если меры не будут приняты вовремя – болезнь начнет прогрессировать.
Целебные свойства меди известны с древности. В старину медью лечили глистные заболевания, эпилепсию, хорею, малокровие, менингит. Медь способна убивать микробов; работники медных заводов никогда не болели холерой. Кузнецы, опоясанные медной проволокой, никогда не страдали радикулитами. Для лечения болей в суставах, отложения солей используют старинное средство в виде медного кольца, которое носят на пальце несколько месяцев, боли при этом уменьшаются, а подвижность в суставах увеличивается. В старину существовал оригинальный и простой способ лечения лихорадки. Раскаленный екатерининский пятак из чистой меди бросали в сосуд с горячей водой и давали пить больному эту воду по 1 столовой ложке 3 раза в день. Больным эпилепсией вкладывали в руки медные монеты, шарики и кольца.
Первые серьезные попытки по изучению лечебных свойств меди в нашей стране были предприняты инженером Ниной Михайловной Сафоновой с 1958 года. А с 1975 года и врачи стали применять медные диски – аппликаторы при лечении различных болезней.
19 февраля 1982 года Н.М. Сафонова выступила в Институте курортологии с докладом, обобщающем опыт ее работы:
«…Аппликация меди снижает температуру, снимает боль, действует кровоостанавливающе, является сильным бактерицидным средством, активизирует водный и минеральный обмен, улучшает сон, успокаивает центральную нервную систему, активизирует действие инсулина в крови, усиливает лейкоцитные функции. Аппликация меди рассасывает доброкачественные опухоли (уплотнение грудной железы, фибромы матки, маститы и др.), излечивает туберкулез, все воспалительные процессы в организме (хронический отит, хронический бронхит, бронхопневмонию, воспаление мочевого пузыря, воспаление почек, легких, гайморит, воспаление в организме, инфекционные артриты, почечно-каменную болезнь, холецистит, полиартрит, диабет, кожные заболевания и др.). Излечивает радикулит, фолликулярный конъюнктивит, травмы различного происхождения, сердечно-сосудистую систему (сердце, вены, тромбофлебиты), улучшает послеинфарктное состояние, болезни гастроэнтерологические (т.е. болезни желудочно-кишечного тракта, язвы желудка, 12-перстной кишки, гастриты, колиты). Аппликация меди восстанавливает слух, снимает шум в ушах, излечивает тендовагинит, послеоперационные грыжи, геморрой, холодные абсцессы, улучшает послеоперационные состояния, лечит ревматоидный артрит».
Лауреат Государственной премии 1990 года в области ядерной медицины – врач Сергей Алексеевич Ласкин, многие годы изучавший медетерапию по методу Н.М. Сафоновой, в своей книге «Целебные силы меди. Медетерапия» (М., «Приор», 2001 г.) приводит следующие клинические примеры:
«Для обоснования целесообразности ускорения внедрения в практику лечебных учреждений страны способа стимуляции неспецифической устойчивости организма, предложенного Н.М. Сафоновой, а именно наружной медетерапии, приводим некоторые данные апробации этого способа в медицинских учреждениях.
1. Несомненный интерес и большое практическое значение представляют данные отоларинголога С.П. Атрохова, который за период 1975–1984 годов в поликлинике № 150 г. Москвы на 300 больных с острыми и хроническими ЛОР-заболеваниями получил убедительный терапевтический эффект при лечении гайморита, ринита, фронтита, трахеобронхита и других заболеваний, для которых все примененные ранее традиционные способы оказались неэффективными, из них 50% выздоровели и у 20% наступило улучшение. Первое время для лечения применялись только медные монеты марки БрА-5, в дальнейшем – диски из чистой меди.
2. В начале 80-х годов из поликлиники № 111 Кировского района г. Москвы от невропатолога Г.П. Карасева поступило сообщение о наблюдении по ускорению исчезновения болевого синдрома при лечении болезней периферической нервной системы, достигнутому аппликацией монет из меди марки БрА-5. Наблюдался лечебный эффект у 39 больных с болевым синдромом, обусловленным люмбаго, деформирующим спондилезом и остеохондрозом различных отделов позвоночника и невралгией седалищного нерва. При этом наиболее успешное купирование боли было у больных с люмбаго (в первые 2–3 дня) и примерно в разные сроки (на 4–7 сутки) – резкое ослабление либо купирование боли у больных с корешковым синдромом вертеброгенной этиологии и невралогии седалищного нерва. Ранее все эти больные наблюдались на протяжении 2,5–4 лет, регулярно получая традиционное лечение, при этом эффект был нестойким. Об эффективности медетерапии свидетельствует то, что вышеуказанные больные на протяжении ближайших 1,5–2 лет в поликлинику за медицинской помощью по названной патологии не обращались. Врач Г.П. Карасев обращает внимание на то, что медетерапия проводилась «в чистом виде» – без применения традиционных средств.
3. Профессор Ф.Н. Ромашов (Университет дружбы народов им. П. Лумумбы), проведя апробацию предложенного способа, сообщает в статье «Целебная сила меди» (газета «Социалистическая индустрия», 1984, 16 августа): «По моим наблюдениям, проведенным у 760 больных с различными заболеваниями, аппликации медных дисков и пластин оказывают противоболевое, противовоспалительное и противоотечное действие».
4. На базе физиотерапевтического отделения Московского областного научно-исследовательского клинического института (МОНИКИ) решением МЗ РСФСР от 4 марта 1986 года проводились клинические испытания способа лечения аппликациями меди. Лечение проводилось в местах наличия сцепления меди с кожей по методике, преложенной Н.М. Сафоновой. Под наблюдением находились 65 больных с диагнозами: остеохондроз с корешковым синдромом различной локализации, артрозо-артриты, хронические заболевания желудочно-кишечного тракта, хронические заболевания легких, вегето-сосудистая дистония, обострение хронического гайморита, железодефицитная анемия, инфильтраты после инъекций.
Улучшение отмечено в 60% случаев. Наиболее эффективно применение медетерапии для снятия болевого синдрома различной этиологии, в частности при остеохондрозе, хронических заболеваниях желудочно-кишечного тракта, легких, гайморите. Важно наблюдение, когда у больного железодефицитной анемией при применении медетерапии и на фоне медикаментозной терапии отмечена положительная динамика самочувствия и анализов крови. В ряде случаев улучшение выражалось и в виде нормализации сна, исчезновения раздражительности и повышенной возбудимости.
Сделан весьма важный вывод: «По предварительным данным, метод может найти применение для снятия болевого синдрома у больных, отягощенных заболеваниями сердечно-сосудистой системы, когда другие способы физического воздействия противопоказаны.
Учитывая, что отделение физиотерапии МОНИКИ является практическим, а не научным, работу по уточнению механизма лечебного действия медетерапии и разработку лечебных методик следует продолжать в любом другом научном физиотерапевтическом отделении».
5. В ЦНИИ рефлексотерапии в 1987 году согласно указанию МЗ СССР проведены клинические наблюдения терапевтической эффективности способа лечения аппликациями дисков из чистой меди, а также медными дисками марки БрА-5 (а именно монетами до 1961 года выпуска). Отмечено следующее:
«Наблюдения были проведены у 84 больных с различными заболеваниями (бронхиальная астма, ревматоидный полиартрит, остеохондроз позвоночника, болевой синдром различной этиологии, пояснично-крестцовый радикулит, невралгия тройничного нерва и др.). В случае, когда применяли иглотерапию в комбинации с монетами, аппликации которых применялись именно в точках рефлексотерапии, отмечался более выраженный лечебный эффект. Почти во всех случаях применения медетерапии в комплексной терапии наблюдался положительный эффект, проявляющийся, в особенности, в уменьшении болевого синдрома, а также в положительном влиянии на нервную систему, например улучшение сна.
Учитывая безвредность и эффективность этого способа повышения неспецифической устойчивости организма, по-видимому, будет целесообразно апробирование его в специализированных научных медицинских учреждениях».
6. Из Ленинграда руководитель отделения терапии неспецифических заболеваний легких ВНИИ пульмонологии МЗ СССР, доктор меднаук, профессор А.Н. Кокосов, прислал следующее сообщение.
«По предложенной Н.М.Сафоновой методике «медь-терапии» проведено лечение 19 больных бронхиальной астмой. Для аппликации меди использовались медные диски – монеты 2-, 3-копеечного достоинства выпуска до 1961 года. Эффект от проведенного лечения отмечен у большинства (у 12 из 19 [63%. – С.А.]) больных и выражался в вмде уменьшения интенсивности приступов удушья и, особенно, сопутствующего болевого синдрома рефлекторного генеза (спаечный процесс плевры, остеохондроз грудного отдела позвоночника).
7. В 1986 году больной Бабенков Н.А., 80 лет, с диагнозом хронический пиелонефрит с почечной недостаточностью 1 степени лечился в Центральной клинической больнице № 1 МПС г. Москвы на протяжении месяца. Но уже через несколько дней после выписки по «скорой помощи» госпитализируется в 50-ю городскую клиническую больницу, где по прошествии 12 дней оставалась выраженная слабость, временами спутанность сознания, больной стал позволять грубости в отношении персонала и родственников, нарастали признаки уремии и общей интоксикации. У пациента стало редким мочеиспускание, на этом фоне – сердечная аритмия с дефицитом пульса до 17 в одну минуту. По заключению консультанта, доктора медицинских наук А.И. Мартынова «…с учетом сочетанности патологии больной с почечной недостаточностью и уремией в отношении медикаментозной терапии неперспективен».
Тогда по просьбе родственников больной был выписан из больницы, и врачом С.А. Ласкиным после отмены дигоксина и фурагина в домашних условиях сразу была применена круглосуточная контактная медетерапия над областью проекции почек в количестве 8–10 трехкопеечных монет (по методике Н.М. Сафоновой). К концу вторых суток отмечено обильное мочеиспускание, пульс стал ритмичным, постепенно вернулась ясность сознания. Физически активен (живет один). С сентября 1986 года в течение 2 лет не отмечалось признаков почечной недостаточности, интоксикации, сердечной аритмии.
В этом наблюдении важно то, что медетерапия дала выраженный эффект в условиях прогрессирующего нарастания почечной недостаточности на фоне отмены всех лекарственных препаратов и эвакуации пациента из больницы.
8. Заслуживают внимания письма больных к Н.М. Сафоновой, подтверждающие возможность улучшения ослабленного слуха в пожилом и старческом возрасте посредством медетерапии, излечения от посттравматической эпилепсии. Весьма важными являются наблюдения положительных результатов при постгеморрогической анемии, а также анемии у больного с циррозом печени. Эти наблюдения указывают на благотворное влияние медетерапии на кроветворную функцию костного мозга, что в ряде случаев дает возможность избавиться от переливания крови.
9. В больнице № 29 г. Москвы у больного 66 лет после операции удаления камня из мочеточника на 5-й день повысилась температура до 40оС. Предпринята повторная операция, которая сопровождалась клинической смертью. После реанимационных мероприятий состояние больного оставалось тяжелым, температура стала повышаться, из послеоперационной раны непрерывно выделялся гной. Врачи объявили: «…вынуждены идти на удаление почки, другого выхода нет». Больного уже готовили к операции, когда его жена, случайно узнав о медетерапии, получила от Н.М. Сафоновой консультацию по лечению этим способом и немедленно применила ее на область мочеточника, над обеими почками и поверх бинтов над раной (бесконтактная и контактная медетерапия). Лечебный эффект проявился изумительно быстро: по прошествии ночи гноевыделение из раны прекратилось, а температура несколько снизилась. Через два дня температура нормализовалась, и больного через неделю от начала медетерапии выписали из больницы с выздоровлением. Прошло более 3 лет. Лечения почек не требовалось.
10. Кроме описанного выше, С.А. Ласкин имеет еще около 20 наблюдений при самой разнообразной патологии: травмах, в том числе спортивных, упорных головных болях, гипертонической болезни, болевом обострении глаукомы, не купирующихся традиционными способами аллергических реакциях.
Этот простой, безвредный и эффективный способ профилактики и лечения заболеваний, обеспечивающий усиление защитных сил самого организма, уже получил положительную оценку в клинических и поликлинических условиях, что дает нам право обратиться в Минздрав СССР с просьбой обеспечить формирование социального заказа в науке с целью выявления механизмов притяжения (сцепления) меди с кожей, а также изучения глубинных процессов, происходящих в организме при лечении аппликациями меди, в том числе не только на органном и клеточном уровнях, но и молекулярном».
Большой опыт в области медетерапии был накоплен в клинике госпитальной хирургии и в отделе клинических исследований Университета дружбы народов имени Патриса Лумумбы. В изданных университетом методических рекомендациях, по применению меди в лечебной практике, говорится:
«Применяя аппликацию медных пластин и медь-электрофорезопунктуру, нам удалось получить хорошие результаты при лечении остеопороза и перелома трубчатых костей у лиц пожилого и старческого возраста. Длительное использование указанных лечебных методик выявило еще одно свойство медетерапии – способность к рассасыванию. В этом плане мы имеем многочисленные наблюдения в клинике за рассасывающим действием медных пластин при лечении отеков, подкожных кровоизлияний, инфильтратов и фиброаденом молочной железы».
Такие замечательные свойства меди вызвали в конце 80-х годов настоящий «медный бум». Огромную популярность среди населения получило ношение медных браслетов. Ажиотаж побудил некоторых недобросовестных предпринимателей объявить лечение медью панацеей. Больные желали получить быстрые и радикально положительные результаты. Появилось много поддельных – немедных, выполненных из сплавов – браслетов. И, как это часто бывает, незнание и несоблюдение принципов лечения привело к разочарованию.
За прошедшее десятилетие получен новый научный опыт, позволяющий более рационально осмыслить суть металлоаппликации и многократно усилить ее лечебное действие. Найден принципиально новый подход к осуществлению способов лечения металлами. Созданы и испытаны устройства – биметаллические аппликаторы, которые уже служат новому медицинскому направлению – металлоионотерапии.
Медные браслеты
У медных браслетов, которые считают регулирующими давление, сегодня уже немало поклонников. Аппликации меди снижают температуру, снимают боль, останавливают кровотечения, нормализуют водный и минеральный обмен, улучшают сон, успокаивают нервную систему, снимают воспалительные процессы в организме, включая воспаление суставов, лечат гинекологические заболевания, оказывают антисептическое действие, уменьшают вредный эффект от радиации, служат эффективным реабилитационным средством после инфаркта.
Медный браслет должен быть изготовлен из меди марки МВ – медь вакуумной плавки (содержание меди 99.9%) и отполирован со всех сторон. При покупке браслета обратите внимание, чтобы все детали медного браслета должны быть изготовлены из меди марки МВ. Медный браслет не может считаться медным, если в нем хотя бы одна деталь сделана не из меди.
Также очень важно, чтобы медный браслет замыкался, образуя контур. Обладая хорошей проводимостью медный браслет замыкает каналы, по которым движутся электрические импульсы, образовывая электромагнитное поле и тем самым, усиливает биополе человека.
Специальная термическая обработка делает браслет очень прочным, его практически невозможно разорвать и при этом вес его около 45 грамм, а ширина 14 мм (оптимальна как для мужских, так и для женских рук). В процессе длительного использования медного браслета образуется оксидная пленка, которую можно снять при помощи зубной пасты, тем самым придав браслету первоначальный блеск. Тщательный уход сохранит ювелирный вид изделия на долгие годы.
Медный браслет не является панацеей от всех болезней, но достоверно установлено улучшение состояния при использовании медного браслета в следующих случаях: гипертония, артрит, радикулит, сердечно-сосудистые заболевания, мигрени, метеозависимость, бессонница.
Также обязательна консультация у врача до и в течении курса медетерапии.
Рекомендуется носить браслет два года, периодически его нужно чистить, т. к. его лечебные свойства снижаются из-за окисления металла. Опыты показали, что в случае, если зелёный налёт на браслете не отмывается или отмывается с трудом, то следует сделать перерыв в ношении медного браслета. Чрезмерное употребление чем бы то ни было, даже самым полезным, вредно, поэтому для каждого индивидуума своя норма ношения медного браслета. Если в процессе использования у Вас появились такие признаки, как тошнота, металлический привкус во рту или другие признаки отравления, следует немедленно прекратить курс.
Исследования по применению медных аппликаторов продолжаются и возможно в скором времени будут известны новые, ранее неизвестные терапевтические свойства медного браслета.
Считается, что медь лечит быстро, но помогает не всем. Существует простой способ определения: подходит ли вам лечение медью. Надо приложить медную монету или диск к коже. Если медь хорошо сцепляется с кожей и удерживается на ней долгое время, значит, медь будет вас лечить. Если сцепления нет, медь в качестве лечебного средства вам не подходит.
Может быть и такой случай, что на одном участке тела сцепление меди с кожей хорошее, а на другом его нет. Тогда целесообразно лечить с помощью меди только те больные места или больные органы, в области которых наблюдается сцепление. Ниже приводятся следующие методы народной медицины лечения медью. Мы не претендуем на научность этих методов, но, тем не менее, они применяются в народе издавна.
При сердечных болях положите медную монету в подключичную ямку. Если монета сцепляется с кожей, носите ее в течение 10 дней, зафиксировав пластырем и не снимая даже на ночь: боли пропадают. Такой же способ лечения применяется для облегчения послеинфарктного состояния. При ишемической болезни сердца медные монеты надо накладывать на воротниковую область и держать их 4 дня.
Если часто ломит руки, наденьте на ночь тонкие перчатки, положив в них медную монету или кусок сжатой в комок медной проволоки.
Если в результате ушиба образовался тромбофлебит на ноге, положите в обувь под носок или чулок медную монету. Она должна прилепиться к ноге. Носите монету до тех пор, пока она не начнет скатываться под пятку. Точно таким же способом можно воспользоваться и при варикозном расширении вен.
При фиброме матки прикладывайте медные монеты на ночь к низу живота.
Считается, что медные монеты излечивают геморрой. .
При гайморите следует накладывать мелкие медные монеты на глаза на ночь, а при шуме в ушах — на шею сзади, фиксируя монеты на шее пластырем.
При головной боли приложите 5-копеечную медную монету к самому больному месту на лбу, висках или затылке.
Если приложить медную монету к месту ушиба, боль вскоре уменьшится.
По данным журнала “АИФ Здоровье” медными монетами с лечебной целью могут пользоваться люди любого возраста, в том числе дети, старики и беременные женщины. Обычно монеты способны «работать без отдыха» в течение нескольких дней. Затем делается 2-недельный перерыв, после чего курс лечения можно повторить. Иногда целесообразно периодически обжигать или смачивать монеты соляным раствором для восстановления их целительных свойств.
Медная вода
Кроме использования монет и браслетов из меди, Аюрведа рекомендует еще и прием медной воды. Считается, что такая вода стимулирует работу печени, селезенки, кроветворных органов, борется с анемией любой этиологии и способствует профилактике ожирения. Однако достоверных научных данных, подтверждающих эти эффекты пока не существует.
Для приготовления такой воды нужно взять старинную медную монету, тщательно ее промыть в известковой воде и далее поступать так, как при приготовлении золотой воды. Медную воду следует принимать по 2 чайные ложки 3 раза в день в течение месяца, все это время целесообразно постоянно носить на запястье медный браслет.
Но, стоит подчеркнуть, что в больших количествах медь очень опасна для организма. Отравление медью приводит к тяжелейшим заболеваниям – анемии, заболеванию печени, болезни Вильсона (медная болезнь или гепатоцеребральная дистрофия). И хотя у человека отравление медью возникает редко благодаря тонким механизмам всасывания и выведения меди из организма, в больших дозах медь вызывает рвоту. Также может наступить общее отравление медью (понос, ослабление дыхания и сердечной деятельности, удушье, коматозное состояние). Это всегда следует помнить при лечении медью. Поэтому прежде чем проводить лечение медной водой необходимо проконсультироваться с врачом.
Выдержки из статьи О.В. Мосина
www.livemaster.ru
МЕДЬ | Энциклопедия Кругосвет
МЕДЬ – элемент 11 группы Периодической системы, плотность 8,9 г см–3, один из первых металлов, ставших известными человеку. Считают, что медь начали использовать около 5000 до н.э. В природе медь изредка встречается в виде металла. Из медных самородков, возможно, с помощью каменных топоров, были изготовлены первые металлические орудия труда. У индейцев, живших на его берегах оз. Верхнее (Сев. Америка), где есть очень чистая самородная медь, способы ее холодной обработки были известны до времен Колумба.
Около 3500 до н.э. на Ближнем Востоке медь научились извлекать из руд, ее получали восстановлением углем. Медные рудники были и в Древнем Египте. Известно, что глыбы для знаменитой пирамиды Хеопса обрабатывали медным инструментом.
К 3000 до н.э. в Индии, Месопотамии и Греции для выплавки более твердой бронзы в медь стали добавлять олово. Открытие бронзы могло произойти случайно, однако ее преимущества по сравнению с чистой медью быстро вывели этот сплав на первое место. Так начался «бронзовый век».
Изделия из бронзы были у ассирийцев, египтян, индусов и других народов древности. Однако цельные бронзовые статуи древние мастера научились отливать не раньше 5 в. до н.э. Около 290 до н.э. Харесом в честь бога солнца Гелиоса был создан Колосс Родосский. Он имел высоту 32 м и стоял над входом во внутреннюю гавань древнего порта острова Родоса в восточной части Эгейского моря. Гигантская бронзовая статуя была разрушена землетрясением в 223 н.э. (см. также СЕМЬ ЧУДЕС СВЕТА).
Предки древних славян, жившие в бассейне Дона и в Приднепровье, применяли медь для изготовления оружия, украшений и предметов домашнего обихода. Русское слово «медь», по мнению некоторых исследователей, произошло от слова «мида», которое у древних племен, населявших Восточную Европу, обозначало металл вообще.
Символ Cu происходит от латинского aes cyproum (позднее, Cuprum), так как на Кипре (Cyprus) находились медные рудники древних римлян.
Относительное содержание меди в земной коре составляет 6,8·10–3%. Самородная медь встречается очень редко. Обычно элемент находится в виде сульфида, оксида или карбоната. Важнейшими рудами меди являются халькопирит CuFeS2, который, по оценкам, составляет около 50% всех месторождений этого элемента, медный блеск (халькоцит) Cu2S, куприт Cu2O и малахит Cu2CO3(OH)2. Большие месторождения медных руд найдены в различных частях Северной и Южной Америк, в Африке и на территории нашей страны. В 18–19 вв. близ Онежского озера добывали самородную медь, которую отправляли на монетный двор в Петербург. Открытие промышленных месторождений меди на Урале и в Сибири связано с именем Никиты Демидова. Именно он по указу Петра I в 1704 начал чеканить медные деньги.
Богатые месторождения меди давно выработаны. Сегодня почти весь металл добывается из низкосортных руд, содержащих не более 1% меди. Некоторые оксидные руды меди могут быть восстановлены непосредственно до металла нагреванием с коксом. Однако большая часть меди производится из железосодержащих сульфидных руд, что требует более сложной переработки. Эти руды сравнительно бедные, и экономический эффект при их эксплуатации может обеспечиваться лишь ростом масштабов добычи. Руду обычно добывают в огромных карьерах, где используются экскаваторы с ковшами до 25 м3 и грузовики грузоподъемностью до 250 т. Сырье размалывают и концентрируют (до содержания меди 15–20%) с использованием пенной флотации, при этом серьезной проблемой является сброс многих миллионов тонн тонко измельченных отходов в окружающую среду (см. ЗАГРЯЗНЕНИЕ ОКРУЖАЮЩЕЙ СРЕДЫ). К концентрату добавляют кремнезем, а затем смесь нагревают в отражательных печах (доменные печи для тонко измельченной руды неудобны) до температуры 1400° С, при которой она плавится. Суммарное уравнение протекающих реакций можно представать в виде:
2CuFeS2 + 5O2 + 2SiO2 = 2Cu + 2FeSiO3 + 4SO2
Cu+I + 1e– = Cu0 |
FeIII + 1e– = FeII | –10e–
2S–II – 12e– = 2SIV |
O2 + 4e– = 2O–II
Большую часть полученной черновой меди очищают электрохимическим методом, отливая из нее аноды, которые затем подвешивают в подкисленном растворе сульфата меди CuSO4, а катоды покрывают листами очищенной меди. В процессе электролиза чистая медь осаждается на катодах, а примеси собираются около анодов в виде анодного шлама, который является ценным источником серебра, золота и других драгоценных металлов.
Около 1/3 используемой меди представляет собой вторичную медь, выплавленную из лома. Годовое производство нового металла составляет около 8 млн. т. Лидируют по производству меди Чили (22%), США (20%), СНГ (9%), Канада (7,5%), Китай (7,5%) и Замбия (5%).
Главное применение металла – в качестве проводника электрического тока. Кроме того, медь используется в монетных сплавах, поэтому ее часто называют «монетным металлом». Она также входит в состав традиционных бронзы (сплавы меди с 7–10% олова) и латуни (сплав меди с цинком) и специальных сплавов, таких как монель (сплав никеля с медью). Металлообрабатывающий инструмент из медных сплавов не искрит и может использоваться во взрывоопасных цехах. Сплавы на основе меди служат для изготовления духовых инструментов и колоколов.
В виде простого вещества медь обладает характерной красноватой окраской. Медь металл мягкий и пластичный. По электро- и теплопроводности медь уступает только серебру. Металлическая медь, как и серебро, обладает антибактериальными свойствами.
Медь устойчива в чистом сухом воздухе при комнатной температуре, однако при температуре красного каления образует оксиды. Она реагирует также с серой и галогенами. В атмосфере, содержащей соединения серы, медь покрывается зеленой пленкой основного сульфата. В электрохимическом ряду напряжений медь находится правее водорода, поэтому она практически не взаимодействует с неокисляющими кислотами. Металл растворяется в горячей концентрированной серной кислоте, а также в разбавленной и концентрированной азотной кислоте. Кроме того, медь можно перевести в раствор действием водных растворов цианидов или аммиака:
2Cu + 8NH3·H2O + O2 = 2[Cu(NH3)4](OH)2 + 6H2O
В соответствии с положением меди в Периодической системе, ее единственная устойчивая степень окисления должна быть (+I), но это не так. Медь способны принимать более высокие степени окисления, причем наиболее устойчивой, особенно в водных растворах, является степень окисления (+II). В биохимических реакциях переноса электрона, возможно, участвует медь(III). Эта степень окисления редко встречается и очень легко понижается под действием даже слабых восстановителей. Известно несколько соединений меди(+IV).
При нагревании металла на воздухе или в кислороде образуются оксиды меди: желтый или красный Cu2O и черный CuO. Повышение температуры способствует образованию преимущественно оксида меди(I) Cu2O. В лаборатории этот оксид удобно получать восстановлением щелочного раствора соли меди(II) глюкозой, гидразином или гидроксиламином:
2CuSO4 + 2NH2OH + 4NaOH = Cu2O + N2 + 2Na2SO4 + 5H2O
Эта реакция – основа чувствительного теста Фелинга на сахара и другие восстановители. К испытываемому веществу добавляют раствор соли меди(II) в щелочном растворе. Если вещество является восстановителем, появляется характерный красный осадок.
Поскольку катион Cu+ в водном растворе неустойчив, при действии кислот на Cu2O происходит либо дисмутация, либо комплексообразование:
Cu2O + H2SO4 = Cu + CuSO4 + H2O
Cu2O + 4HCl = 2 H[CuCl2] + H2O
Оксид Cu2O заметно взаимодействует со щелочами. При этом образуется комплекс:
Cu2O + 2NaOH + H2O 2Na[Cu(OH)2]
Для получения оксида меди(II) CuO лучше всего использовать разложение нитрата или основного карбоната меди(II):
2Cu(NO3)2 = 2CuO + 4NO2 + O2
(CuOH)2CO3 = 2CuO + CO2 + H2O
Оксиды меди не растворимы в воде и не реагируют с ней. Единственный гидроксид меди Cu(OH)2 обычно получают добавлением щелочи к водному раствору соли меди(II). Бледно-голубой осадок гидроксида меди(II), проявляющий амфотерные свойства (способность химических соединений проявлять либо основные, либо кислотные свойства), можно растворить не только в кислотах, но и в концентрированных щелочах. При этом образуются темно-синие растворы, содержащие частицы типа [Cu(OH)4]2–. Гидроксид меди(II) растворяется также в растворе аммиака:
Cu(OH)2 + 4NH3.H2O = [Cu(NH3)4](OH)2 + 4H2O
Гидроксид меди(II) термически неустойчив и при нагревании разлагается:
Cu(OH)2 = CuO + H2O
Есть сведения о существовании темно-красного оксида Cu2O3, образующегося при действии K2S2O8 на Cu(OH)2. Он является сильным окислителем, при нагревании до 400° С разлагается на CuO и О2.
Большой интерес к химии оксидов меди в последние два десятилетия связан с получением высокотемпературных сверхпроводников, из которых наиболее известен YBa2Cu3O7. В 1987 было показано, что при температуре жидкого азота это соединение является сверхпроводником. Главные проблемы, препятствующие его широкомасштабному практическому применению, лежат в области обработки материала. Сейчас наиболее перспективным считается изготовление тонких пленок.
Многие из халькогенидов меди – нестехиометрические соединения. Сульфид меди(I) Cu2S образуется при сильном нагревании меди в парах серы или в среде сероводорода. При пропускании сероводорода через водные растворы, содержащие катионы Cu2+, выделяется коллоидный осадок состава CuS. Однако, CuS – не простое соединение меди(II). Оно содержит группу S2 и лучше описывается формулой CuI2CuII(S2)S. Селениды и теллуриды меди проявляют металлические свойства, а CuSe2, CuTe2, CuS и CuS2 при низких температурах являются сверхпроводниками.
При нагревании меди с галогенами можно синтезировать безводные дифторид, дихлорид и дибромид. Растворы галогенидов меди(II) удобнее получать взаимодействием металла, его оксида, гидроксида или карбоната с соответствующей галогеноводородной кислотой. Из водных растворов всегда выделяются кристаллогидраты.
Попытки получить иодид меди(II) приводят к образованию иодида меди(I) CuI:
2Cu2+ + 4I– = 2CuI + I2
При этом раствор и осадок окрашиваются в бурый цвет за счет присутствия иода. Образовавшийся иод можно удалить действием тиосульфат-иона:
I2 + 2SO3S2– = 2I– + S4O62–
Однако при добавлении избытка тиосульфат-иона иодид меди(I) растворяется:
CuI + 2SO3S2– = [Cu(SO3S)2]3– + I–
Точно так же попытки получить цианид меди(II) приводят к образованию CuCN. С другой стороны, с электроотрицательным фтором не удается получить соль меди(I). Три других галогенида меди(I), представляющие собой белые нерастворимые соединения, осаждаются из водных растворов при восстановлении галогенидов меди(II).
В водных растворах бесцветный ион меди(I) очень неустойчив и диспропорционирует
2CuI CuII + Cu(р)
Возможно, причиной этого является размер атома. Ион CuII меньше, чем CuI, и, имея вдвое больший заряд, намного сильнее взаимодействует с водой (теплоты гидратации составляют ~2100 и ~580 кДж моль–1, соответственно). Разница является существенной, так как она перевешивает вторую энергию ионизации для меди. Это делает ион CuII более стабильным в водном растворе (и ионных твердых веществах), чем CuI, несмотря на устойчивую конфигурацию d10 последнего. Тем не менее, CuI может стабилизироваться в соединениях с очень низкой растворимостью или за счет комплексообразования. Комплексы легко образуются в водном растворе при взаимодействии Cu2O с соответствующими лигандами. В водных растворах хлоро- и амминкомплексы меди(I) медленно окисляются кислородом воздуха до соответствующих соединений меди(II).
Катион меди(II), напротив, в водном растворе вполне устойчив. Соли меди(II), в основном, растворимы в воде. Голубой цвет их растворов связан с образованием иона [Cu(H2O)4]2+. Они часто кристаллизуются в виде гидратов. Водные растворы в небольшой степени подвержены гидролизу и из них часто осаждаются основные соли. Основный карбонат есть в природе – это минерал малахит, основные сульфаты и хлориды образуются при атмосферной коррозии меди, а основный ацетат (ярь-медянка) используется в качестве пигмента.
Ярь-медянка известна со времен Плиния Старшего (23–79 н.э.). В русских аптеках ее начали получать в начале 17 в. В зависимости от способа получения она может быть зеленого или голубого цвета. Ею были окрашены стены царских палат в Коломенском в Москве.
Наиболее известную простую соль – пентагидрат сульфата меди(II) CuSO4·5H2O – часто называют медным купоросом. Слово купорос, по-видимому, происходит от латинского Cipri Rosa – роза Кипра. В Росси медный купорос называли синим, кипрским, затем турецким. То, что купорос содержит медь, было впервые установлено в 1644 Ван Гельмонтом. В 1848 Р.Глаубер впервые получил медный купорос из меди и серной кислоты. Сульфат меди широко используется в электролитических процессах, при очистке воды, для защиты растений. Он является исходным веществом для получения многих других соединений меди.
Тетрааммины легко образуются при добавлении аммиака к водным растворам меди(II) до полного растворения первоначально выпавшего осадка. Темно-синие растворы тетраамминов меди растворяют целлюлозу, которую можно вновь осадить при подкислении, что используется в одном из процессов для получения вискозы. Приливание этанола к раствору вызывает осаждение [Cu(NH3)4]SO4·H2O. Перекристаллизация тетраамминов из концентрированного раствора аммиака приводит к образованию фиолетово-синих пентаамминов, однако пятая молекула NH3 легко теряется. Гексааммины можно получить только в жидком аммиаке, и их хранят в атмосфере аммиака.
Медь(II) образует плоско-квадратный комплекс с макроциклическим лигандом фталоцианином. Его производные используются для получения ряда пигментов от синего до зеленого, которые устойчивы вплоть до 500° С и широко используются в чернилах, красках, пластиках и даже в цветных цементах.
Медь имеет важное биологическое значение. Ее окислительно-восстановительные превращения участвуют в различных биохимических процессах растительного и животного мира.
Высшие растения легко переносят сравнительно большое поступление соединений меди из внешней среды, низшие же организмы, наоборот, чрезвычайно чувствительны к этому элементу. Самые незначительные следы соединений меди их уничтожают, поэтому растворы сульфата меди или их смеси с гидроксидом кальция (бордосская жидкость) применяют как противогрибковые средства.
Из представителей животного мира наибольшие количества меди содержатся в телах осьминогов, устриц и других моллюсков. В их крови она играет ту же роль, что железо в крови других животных. В составе белка гемоцианина она участвует в переносе кислорода. Неокисленный гемоцианин бесцветен, а в окисленном состоянии он приобретает голубовато-синюю окраску. Поэтому не зря говорят, что у осьминогов – голубая кровь.
Организм взрослого человека содержит около 100 мг меди, сосредоточенной, в основном, в белках, только содержание железа и цинка выше. Ежедневная потребность человека в меди составляет около 3–5 мг. Дефицит меди проявляется в анемии, однако избыток меди также опасен для здоровья.
Елена Савинкина

www.krugosvet.ru
Области применения меди — назначение и использование
Медь находится на втором месте по популярности среди всех цветных металлов. Основной источник получения меди – это медная руда, которую добывают в многочисленных месторождениях сланца и песчаника.
Чистый металл имеет красно-розовый цвет и характеризуется высокими показателями тепло- и электропроводности. К примеру, по уровню теплопроводности она лучше железа в 6 раз.
Область применения меди
Как в форме чистого металла, так и в сочетании со сплавами медь применяется в разных промышленных областях.
Ее свойства позволяют активно применять этот металл электротехники. Свыше 50% добытого металла используется для производства всевозможных электроприборов и электропередач.
Высокие показатели электро- и теплопроводности обуславливают широкое использование меди в строительной отрасли. Как известно, металл отличается устойчивостью к отрицательному действию коррозии и ультрафиолетовых лучей, также не деформируется в условиях резких колебаний температурного режима.
Самым популярным продуктом из меди являются провода. Для их изготовления применяется максимально чистый металл, потому что дополнительные примеси в значительной степени уменьшают показатель токопроводимости. К примеру, если в готовом продукте будет присутствовать свыше 0,02% алюминия, то способность продукта проводить ток падает на 10%. Хорошая вязкость и пластичность обуславливают популярность меди для создания продукции с различными узорами. В результате обжига, проволока, созданная из красной меди, приобретает максимальный уровень пластичности и мягкости. Из нее можно формировать узоры и орнаменты любой сложности.
Хорошая вязкость и пластичность обуславливают популярность меди для создания продукции с различными узорами. В результате обжига, проволока, созданная из красной меди, приобретает максимальный уровень пластичности и мягкости. Из нее можно формировать узоры и орнаменты любой сложности.
Такую проволоку применяют в:
- электротехнике
- электроэнергетике
- автомобилестроении
- судостроении
- производстве кабеля и проводов.
Высокий показатель теплопроводности меди позволяет использовать ее в различных теплообменниках и теплоотводных приборах. Именно из меди создают кулера для системных блоков, радиаторы отопления, трубы, кондиционеры и другие механизмы.
Несмотря на довольно высокую стоимость медных труб, их достоинства неоспоримы:
- не боятся ультрафиолетового излучения
- устойчивы к образованию коррозии
- не реагируют на температурные перепады. Поэтому монтаж можно проводить даже в условиях низких температур воздуха.
Вследствие высокого показателя механической прочности, а также возможности механической обработки специалисты создают бесшовные медные трубы, имеющие круглое сечение. Они предназначены для транспортировки жидких веществ или газов в системах газо- и водоснабжения, кондиционирования и отопления.
Пожалуй, самым первым материалом, из которого сделали кровельное покрытие, была медь. Такой вариант кровли характеризуется долгим периодом эксплуатации — около 200 лет. Через определенное время кровля из меди окисляется, вследствие чего формируется пленка патины. Она защищает
поверхность меди от неблагоприятного действия ультрафиолета, низкой температуры, влажности и других погодных явлений.
Сплавы меди и их применение
Медь и ее сплавы широко используются в процессе возведения линий электропередач и устройств разного типа связи. Сплавы применяют в электромашиностроительной отрасти, в создании разных приборов, при изготовлении холодильников, вакуум-аппаратов.
Примерно половина всей меди используется на нужды электропромышленности. На базе меди получено огромное количество сплавов с разными металлами, например, Zn, Sn, Al, Be, Ni, Mn, Pb, Ti, Ag, Au. Существуют сплавы и с неметаллами, например, с фосфором, серой, кислородом и другими. Сфера использования таких сплавов довольно обширна. Большая часть их них отличается высокими антифрикционными качествами. Сплавы используют в литой и кованой форме, а также в порошковой форме. К примеру, широко используются сплавы:
Сфера использования таких сплавов довольно обширна. Большая часть их них отличается высокими антифрикционными качествами. Сплавы используют в литой и кованой форме, а также в порошковой форме. К примеру, широко используются сплавы:
- оловянные. Содержат от 4 до 33 % Sn
- свинцовые. В них содержится примерно 30 % Pb
- алюминиевые. Содержат от 5 до 11 % Al
- кремниевые. В таких сплавах присутствует 4-5 % Si
- сурьмяные бронзы, которые востребованы в производстве подшипников, теплообменников и прочих материалов в виде листа, прутков и труб для химической, бумажной и пищевой промышленности.
Разные сплавы меди с хромом, а также вольфрамовый порошковый сплав применяются для изготовления электродов и электроконтактов.
Сложно представить себе химическую промышленность и машиностроение без латуни — сплава меди с цинком (до 50 % Zn). Чаще всего в небольших количествах тут присутствуют и другие элементы, например, Al, Si, Ni, Mn. Сплавы меди с фосфором (6-8 %) применяют как припои.
Использование меди в медицине
Применение меди в медицинской отрасли можно встретить довольно часто. Согласно нормам традиционной медицины — медь это крайне важный элемент жизнедеятельности человека. В нашем организме медь присутствует в объеме 2*10-4 % от общего веса человека. Каждый день вместе с пищей мы употребляем примерно 60 мг меди, однако усваивается лишь 2 мг, но именно это количество и является суточной нормой для взрослого человека.
Медь крайне важна в процессе биосинтеза гемоглобина, а также в поддержании уровня сахара, холестерина и мочевой кислоты. Чтобы сердечно-сосудистая система, головной мозг, пищеварительный тракт работали как положено, необходима медь. При хроническом недостатке меди в организме человека развиваются следующие болезни:
- анемия
- остеопороз
- глаукома
- псориаз
- атрофируется сердечная мышца
- человек быстро устает, теряет вес
- в организме накапливается холестерин.
Самыми богатыми продуктами, содержащими медь, являются:
- шампиньоны
- картофель
- печень трески
- цельное зерно
- устрицы и каракатицы.
Применение и маркировка меди
Чтобы выяснить конкретный состав, по классификации ГОСТ 859-2001, имеется особая таблица с характеристиками и маркировками.
Наиболее востребованной является катодная медь или медные полуфабрикаты, другими словами катанка, прокат, слитки и предметы из медных сплавов. Особенности и сфера использования металла, по данным таблицы ГОСТ 859-2001, определяются согласно процентному содержанию разных примесей. Разные марки меди содержат от 10 до 50 разных примесей. Чаще всего наблюдается разделение на две группы:
- сплав, в котором содержится минимальное количество кислорода (до 0,011 %). Этот сплав имеет высокую чистоту. Обозначение по ГОСТ 859-2001 – М00, М01, медь М3. Применяются главным образом для создания токопроводников или сплавов высокой степени чистоты
- рафинированный металл, в котором содержится примесь фосфора для общего применения. Обозначения по ГОСТ 859-2001 – М1ф, М2р, М3р. Из такого металла создают трубы, горячекатаные и холоднокатаные листы, фольга.
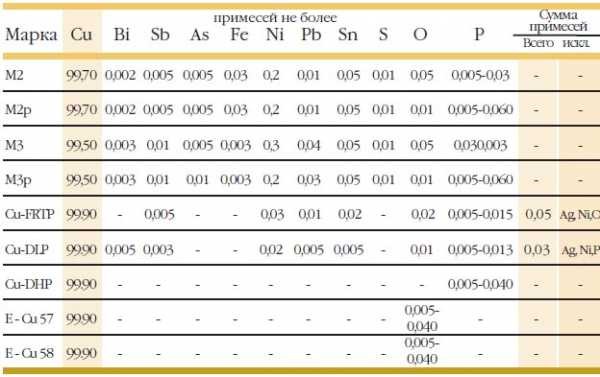 Стоит отметить, что данные классификации по ГОСТ 859-2001 соответствуют иностранным данным классификации по DIN. В иностранной классификации обязательно должны быть обозначены химические элементы и примеси. К примеру, марка М00 – это CuOFE, M1 – CuOF.
Стоит отметить, что данные классификации по ГОСТ 859-2001 соответствуют иностранным данным классификации по DIN. В иностранной классификации обязательно должны быть обозначены химические элементы и примеси. К примеру, марка М00 – это CuOFE, M1 – CuOF.
Для криогенной промышленности применяется исключительно наиболее чистые металлы, бескислородные марки. Для всех остальных нужд самыми популярными являются такие виды горячего и холодного проката, которые используются в разнообразных отраслях строительства и производства:
- М0, М00 – применяется для создания электропроводников и изделий высокой частоты. Они делаются только под заказ и отличаются более высокой стоимостью
- М001б, М001бф – из них делают медную проволоку небольшого сечения, электрические шины, проводку
- медь М1 (М1р, М1ре, М1ф) – это отличные проводники тока, прокатные материалы и высококачественные бронзы, имеющие максимально низкое количество олова. Из такой меди создают прутья и электроды для электрической сварки чугуна и прочих плохо свариваемых металлов
- медь М2 (М2к, М2р). Она подходит для создания изделий для криогенной техники, литого проката для обработки давлением.
- медь М3 (М3р, М3к) применяется в процессе создания прессованных полуфабрикатов и плоского проката. Кроме этого, из нее делают проволоку для электромеханической сварки медных и чугунных предметов.
Соединения меди
Далее рассмотрим наиболее востребованные соединения меди и их применение. Начнем с фунгицидов. Свыше сотни лет они применяются для борьбы с ложномучнисторосяными и несовершенными грибами, которые являются причиной пятнистости вегетативных органов растений. Фунгициды на основе меди и сегодня являются основными в системе антирезистентной программы к системным фунгицидам.
Пестициды, изготовленные на основе меди, очень востребованы в целях защиты садов и виноградников от вредителей и болезней.
Очень популярен сульфат меди. Применение это вещества происходит повсеместно и в различных областях. Сульфат меди(II) является наиболее важной солью меди. Он является исходным материалом для синтеза многих веществ. Безводный сульфат меди используют в качестве индикатора влажности. В лабораторных условиях он отвечает за осушку этанола и ряда других соединений.
Однако, наибольший объем медного купороса CuSO4 расходуется для борьбы с вредителями в сельскохозяйственной отрасли.
Гидроксид меди применение
Гидроксид меди, также ка и сульфат является отличным фунгицидом. Он защищается растения от различных болезней, как грибковых, так и бактериальных.
Плюсы использования гидроксида меди:
- широкий перечень инфекций, на которые действует соединение
- можно использовать практически для всех видов растений
- питательные вещества меди обеспечивают долгий срок хранения овощей и фруктов
- низкое содержание меди вследствие насыщения препаратов ионами Cu++
- устойчив к осадкам
- не оказывает негативного действия на природу
- невысокая стоимость.
Оксид меди применение
Оксид меди — CuO очень востребован в процессе изготовления стекла и эмалей. Он придает готовым изделиям зелёный и синий оттенок. Также оксид меди незаменим в производстве медно-рубинового стекла.
В лабораторных условиях он используется для выявления восстановительных качеств различных соединений. Вещество способно восстановить оксид до металлической меди. При этом наблюдается переход чёрного цвета оксида меди в розовый оттенок меди.
mining-prom.ru
Медь и ее основные и популярные сплавы. Маркировка по ГОСТ.
Медь и ее сплавы — отличное вещество, которое применяется во всех отраслях промышленности. Сейчас сложно представить жизнь без этого металла.

Медь — металл, который необходимый во всех отраслях промышленности
Основные факты
Медь является очень важным материалом для человека. Первыми орудиями труда у людей были именно медные изделия. Раньше обработка металла производилась холодным методом, что подтверждают различные археологические находки на территории Северной Америки. Еще до приезда Колумба индейцы сохранили такие традиции. Установлено, что еще 7 000 лет назад человек добывал и использовал медную руду. Именно благодаря его податливости он стал очень популярным.
Медь имеет красноватый оттенок за счет небольшого количества кислорода в составе. Если полностью исключить этот элемент, то оттенок будет желтоватым. Если начистить медь, то она будет иметь яркий блеск. Чем больше будет валентность, тем слабее оттенок. К примеру, медные карбонаты обычно имеют зеленый либо синий цвет.
После серебра медь является вторым металлом, который обладает хорошей электропроводностью. Из-за этого он активно применяется в электронике. Медь плохо реагирует на кислород. Она покрывается пленкой из-за окисления на свежем воздухе.
Медный оксид можно получить, если прокалить медь, гидрокарбонат или нитрат на воздухе. Это соединение способно окисляюще воздействовать на соединения органического характера.
Если растворить медь в серной кислоте, то выходит медный купорос. Его применяют в химической промышленности, а также использует в качестве профилактики вредителей урожая.
В зависимости от влияния примесей на характер общего медного сплава можно выделить 3 основные группы.
- К первой относятся те соединения, которые вместе с медью создают твердые вещества. Это касается мышьяка и сурьмы. Сюда же относятся железо, цинк, никель, олово, алюминий, фосфор и прочие.
- Вторую группу составляют соединения, которые практически не растворяются в меди. Примером является висмут, свинец и прочие. Из-за них обработка посредством давления затруднена. На способность к электропроводности это практически не влияет.
- Третья группа — это сера и кислород. Вместе с медью они создают химические соединения, которые отличаются своей хрупкостью.
Маркировка по ГОСТ

Существуют различные маркировки меди
В зависимости от добавок, примесей и их доли в общем объеме, сплав имеет разные свойства. Это может быть устойчивость к коррозии, прочность, антифрикционный эффект и прочее. Самыми распространенными являются смеси меди с алюминием, цинком, марганцем, магнием. Но в промышленности применяются варианты и с другими химическими веществами.
Разработано специальная таблица с маркировкой меди и ее характеристиками. Она применяется, когда нужно определить состав по классификации ГОСТ.
- К примеру, в Марке М00 содержание меди должно быть не менее 99,99%.
- В марке М0 содержится примерно 99,95% меди. В марке М0б присутствует примерно 99,97% основного компонента.
- Если медь обозначается как М1, это значит, что ее доля во всем составе около 99,9%.
- Если имеется пометка М1р, то это означает, что в веществе содержится 99,9 меди.
- Если имеется обозначение М2, то меди будет 99,7%, а вот в марке М2р тоже такая же концентрация основного компонента.
- Если пишется марка М3 иМ3р, то количество меди составляет 99,5%. Если марка М4, то количество основного вещества равняется 99%.
- Несмотря на то что количество меди в марках М1 и М1р, М2 и М2р, М3 и М3р одинаковое, при этом в продуктах с буквой «р» содержание кислорода меньше и составляет только не более 0,01%, а вот в других — примерно 0,05-0,08%. Кроме того, в состав включен фосфор, но его доля не более 0,04%.
А вот в продукте с маркой М0б совсем отсутствует кислород, в отличие от продукта с пометкой М0, где содержание кислорода составляет примерно 0,02%.
В большинстве случаев применяется катодная медь либо полуфабрикаты из меди (это касается проката, катанок и прочих изделий). Особенности и область применения зависят от процентного содержания примесей в общем продукте. В различных марках может быть 10–50 примесей. Чаще всего медь разделяют на 2 группы:
- Сплавы, которые содержат минимальное количество кислорода — не более 0,011%. По ГОСТу они обозначаются как М00, М01 и М3. Обычно применяются они для токопроводников либо создания сплавов, которые отличаются высокой чистотой.
- Металл рафинированного типа, которые имеет примеси фосфора в общем объеме. Предназначен для общего применения. По ГОСТу обозначается как М1ф, М2р, М3р. Обычно применяется для создания фольги, труб и листов горячего и холоднокатаного типа.
Для создания чистых и высокоточных металлов применяется только медь той марки, где отсутствует кислород. Это очень важно для криогенной промышленности. В остальных же случаях используются другие виды меди. Например, применение бывает следующим в зависимости от марки:
- М0 и М00 используется в производстве электропроводниковых деталей и деталей с высокой частотой. Обычно такие элементы получаются дороже, и делают их на заказ.
- М001б и М001бф применяется для медной проволоки с небольшим диаметром сечения. Также подходит для другой проводки и электрических шин.
- М1 (в том числе М1р, М1ре и М1ф) применяются как проводники для электрического тока. Они задействованы для создания бронзы высокого качества, где минимальное количество олова. Обычно делают электроды и прутья для сварки чугуна и прочих металлов, которые трудно сваривать.
- М2 (в том числе М2к, М2р) используется обычно для деталей, которые применяются в криогенной промышленности. Еще подходит для литого проката, который будет подвергаться обработки под давлением.
- М3 (в том числе М3р и М3к) подходит для производства полуфабрикатов прессованного типа либо проката плоского характера. Еще используется для проволоки, которая задействуется для сварки электромеханического характера чугунных и медных деталей.
Популярные сплавы меди
В качестве легирующего компонента в сплавах меди обычно применяется фосфор, золото, цинк и марганец. Их концентрация обычно составляет меньше 10%. Исключением является только латунь. Такая доля зависит от того, какие свойства сплавов требуются, а также учитывается его назначение.
Вот основные разновидности сплавов меди:
- Смесь с оловом. Она считается одной из самых первых, которые были открыты. Еще в Древней Греции активно применялась для создания шедевров, которые на данный момент являются ценностью для людей. Сегодня процесс создания такого сплава значительно улучшен. Используются электрически печи дугового типа. Для защиты от окисления задействован вакуум. Сплав закаливают, чтобы увеличить его прочность и пластичность.
- Алюминиевая бронза. Этот сплав меди и алюминия может деформироваться. Практически не подвержен коррозии. Его применяют обычно для создания деталей, которые будут подвергаться высокотемпературному воздействию.
- Смесь меди со свинцом. Этот материал отличается антифрикционными свойствами. За счет добавления свинца значительно увеличен показатель прочности.
- Латунь. Это сплав из 2 либо 3 компонентов.
- Нейзильбер — сплав на основе меди, причем добавлен никель — примерно от 6 до 34%. Еще в состав включен цинк. Стоимость такого материала меньше, чем у мельхиора, однако по внешним данным, характеристикам и свойствам они идентичные.
- Смесь меди и железа. Это возможно благодаря тому, что оба материала обладают схожими химическими показателями, но при этом температура плавления у них разная, так что выходит пористый сплав.

Сплавы с медью используют во многих отраслях промышленности
Сплавы на основе меди применяются в промышленности. Трудно найти хотя бы одну отрасль, где бы ни задействовали медь для производства различных деталей. В чистом виде металл используется в коммуникациях электротехнического типа. Камеры теплообмена, трубопровод, вакуумные механизмы на 1/3 состоят из этого металла.
Сплавы активно применяются в производстве автомобилей и сельскохозяйственного оборудования. Благодаря высокой резистентности к коррозии сплавы меди применяют для производства аппаратуры в химической отрасли. Смесь свинца и меди используется в создании техники сверхпроводникового типа.
Когда нужно сделать детали со сложным узором, то требуется сплав, обладающий пластичностью и вязкостью. Этим критериям соответствует мягкая медь. Из нее можно сделать любые шнуры и детали. Проволока хорошо гнется. К тому же ее можно соединять (паять) с серебряными и золотыми поверхностями. Сплавы меди отлично взаимодействуют с эмалью. Такая поверхность долго будет сохраняться, она не отслоится, не растрескается.
Бронза как сплав меди

Бронза как сплав меди активно используется в жизни человека
Медь и сплавы на ее основе очень разнообразны. Одним из ярких примером является бронза. Это смесь из меди, кремния, алюминия, бериллия и прочих элементов (исключением является только цинк). Марка заключается в символе Бр и других буквах, которые указывают на легирующее вещество. Затем пишется цифра, которая указывает на их пропорции. К примеру, марка БрОЦС4-4-2,5. Такой набор символов означает, что бронза содержит 4% олова, столько же цинка и 2,5% свинца. Всем остальным является уже медь.
Существует классификация по содержанию дополнительных веществ в общем сплаве. Выделяют бронзу оловянного и безоловянного типа. Последняя имеет подвиды. Характеристики бронзы:
- Оловянная. Эта смесь с оловом имеет высокий показатель резистентности к коррозии, имеется еще и антифрикционный эффект. Благодаря этому материал часто используется в химической отрасли. Это обычно смесь с никелем. Еще могут добавлять фосфор и цинк. Последнего материала добавляют не более 10%. Благодаря этому сплав по цене недорогой, но его характеристики не изменяются. Благодаря последним двум элементам улучшается антифрикционное действие. БрОц4–5 задействуют в производстве пружин. Это касается деформируемых бронз. Относительно литейных бронз, то обычно их применяют для арматуры, антифрикционных изделий. К примеру, это БрО4Ц4С17, БрО5ЦНС5, БрО3Ц12С5.
- Алюминиевая. Обладает хорошей сопротивляемостью коррозии в соленой воде и климатических условиях тропиков. Если бронза 1-фазная, то она отличается хорошей гибкостью и применяется для штамповки глубокого типа. Если бронза 2-фазная, то ее подвергают деформации горячего типа либо используют для фасонного литья. По литейным характеристикам алюминиевая бронза уступает оловянной, но благодаря ей получаются более плотные изделия. Примерами алюминиевой бронзы является БрАЖН10-4-4, БрА10Ж3Мц2.
- Кремнистые. За счет добавления кремния (не более 3,5%) материал становится прочнее и эластичнее. За счет никеля и марганца улучшаются коррозионные и механические показатели. Такую бронзу легко обрабатывать с помощью резания, давления и сварки. За счет упругости, механических характеристик и устойчивости к коррозии кремнистые бронзы применяются для создания пружинящих изделий различных приборов, в том числе и радиооборудования. Причем детали устанавливают в аппаратуру, которая будет работать в агрессивных условиях — морская вода, температура до 2 500°С. Примером кремнистой бронзы является БрКМц3–1.
- Бериллиевые. Эти сплавы отличаются тем, что они упрочнены за счет температурной обработки. Обладают высокой характеристикой к временному сопротивлению, хорошими пределами текучести, упругостью. Имеет устойчивость к коррозии. Подвергаются резанию и сварке. Активно используются для создания пружин, мембран и прочих деталей, которые будут работать на износ. Элементы обычно используются для приборов электронной техники. Примером бериллиевой бронзы является БрБ2.
- Свинцовые. В жидкой меди свинец почти не растворяется. После того как сплав затвердеет, он будет состоять их отдельных кристаллов меди и свинца. Благодаря такой необычной структуре имеются антифрикционные свойства. Из-за этого такие сплавы применяются для создания подшипников и вкладышей, которые будут работать с высокими показателями скорости и давления. Теплопроводность бронзы БрС30 в 4 раза больше, чем у оловянных сплавов. Благодаря этому она хорошо убирает нагревание, которое возникает из-за сильного трения. Довольно часто в свинцовые сплавы добавляют олово и никель, чтобы улучшить коррозионные и механические характеристики.
Все эти разновидности бронзы активно применяются в промышленности и других отраслях.
Внимание: латунь
Под латунью понимают смесь из меди и цинка, причем последнего компонента может быть от 5 до 44%. Если в состав включен еще и цинк (от 5 до 20%), то такая латунь называется красной либо томпаком. Если содержание цинка от 20 до 35%, то латунь называется желтой. Латунь, где концентрация цинка более 45%, редко применяется на практике.
Классификация латуни следующая:
- Двухкомпонентная. Еще ее называется простой. Входит только медь, цинк и небольшое количество примесей.
- Многокомпонентная — специальная. Кроме цинка и меди в состав включены другие легирующие компоненты.
Марка латуни обозначается как буква Л и двузначное число, которое указывает на долю меди. К примеру, если марка латуни Л80, то содержание меди составляет 80%, а цинка — 20%.
Томпак может обозначаться как Л96. Тогда содержание меди составляет примерно 95-96%. Еще томпак может обозначаться как Л90. В это случае мед содержится примерно 88–91%. В обоих случаях допускается не более 0,2% примесей.
Полутомпак обозначается как Л85. Это означает, что меди в нем будет от 84 до 86%. Если полутомпак записан как Л80, то содержание меди составит от 79 до 81%. В обоих случаях допускается содержание примесей не более 0,3%.
Латунь обозначается еще как Л70. В этом случае меди будет примерно 69–72%, примесей разрешено не более 0,2%. Если марка Л68, то концентрация основного вещества — от 67 до 70%, а примесей допускается не более 0,3%. Марка Л63 предполагает, что содержание меди составит от 62 до 65%, а примесей может быть до 0,5%. Если записана марка Л69, то основного компонента будет от 59 до 62%, причем примесей — не более 1%.
Латунь 2-компонентного типа довольно просто подвергается давлению. Обычно из нее делают изделия в виде труб, листов и прочего. Латунные детали могут растрескиваться из-за большого внутреннего напряжения. Когда они долго хранятся на открытом воздухе, то появляются трещины, которые могут располагаться как по ширине, так и по длине. Чтобы предотвратить это, нужно воспользоваться низкотемпературным воздействием (температура 200–300°С).
А вот марок латуни поликомпонентного типа намного больше, чем 2-компонентного. В обозначения сначала пишется Л. Потом записаны буквы, указывающие на легирующие компоненты, которые включены в состав вещества помимо цинка. После этого идет дефис и записываются числа. Первая цифра указывает на концентрацию основного вещества (в процентах). Все остальные — это доли легирующих веществ. Их последовательность будет такой же, как и в части с буквенными обозначениями. Сначала записываются те элементы, доля которых больше. К примеру, если марка записана как ЛАЖМц66-6-3-2, то это означает, что меди содержится 66%, алюминия — 6%, железа — 3% и марганца — 2%.
Для информации
Основные легирующие вещества в латуни многокомпонентного типа следующие:
- Марганец. Он применяется для улучшения прочности готового изделия. Повышается устойчивость к коррозии. Особенно это касается сочетания с железом. Еще это подходит для олова и алюминия.
- Олово. Тоже используется для улучшения прочности. Еще конечное вещество будет отличаться высокой устойчивостью к коррозии, особенно в соленой воде. Такие материалы, которые имеет включения олова, часто именуются еще морскими.
- Никель. Это вещество тоже улучшает прочность и добавляет устойчивость к коррозии, причем в различных условиях.
- Свинец. Из-за него ухудшаются механические характеристики, но при этом улучшается способность к обработке посредством резания. Обычно добавляют немного — содержание в латуни не более 1–2%. Это используется для деталей, которые будут подвергаться обработке на станках. Вот почему такую латунь еще именуют автоматной.
- Кремний. Из-за него твердость материала ухудшается, как и прочность. Но если добавлять сразу и кремний, и свинец, то антифрикционные свойства увеличиваются. Такой латунью можно будет заменить бронзу, которая применяется в подшипниках и считается более дорогой по цене.

Латунь — один из популярных металлов используемых в промышленности
Заключение
Медь, сплавы меди — это материалы, без которых сейчас трудно представить современный мир. Они обладают различными свойствами и используются в разных отраслях промышленности. Самыми известными сплавами являются бронза и латунь.
Похожие статьи
ometallah.com
Полезное о металлах: медь | Журнал Ярмарки Мастеров
В ходе многолетней практики создания украшений часто приходится сталкиваться с необходимостью рассказать покупателю или человеку, пришедшему на мастер-класс, о свойствах металлов и их славов.
Понятия — серебро, золото, железо — в целом являются общеизвестными и пояснений не требуют, а вот такие загадочные обозначения как «бижутерный сплав», томпак, бронза, нейзильбер и другие могут вызывать некоторые затруднения.
В связи с этим, возникла потребность написания цикла обзорных статей, которыми я бы хотела поделиться.
Первая статья цикла посвящена меди — первому освоенному человеком металлу.
Медь — элемент одиннадцатой группы IV периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 29. Обозначается символом Cu (лат. Cuprum).
В чистом виде медь — это пластичный, вязкий и легко прокатываемый в тонкие листы металл золотисто-розового цвета (розового цвета при отсутствии оксидной плёнки), обладающий высокой тепло- и электропроводностью.
Тонкие плёнки меди на просвет имеют зеленовато-голубой цвет.
Медь встречается в природе в самородном виде чаще, чем золото, серебро и железо.

Поэтому из-за сравнительной доступности для получения из руды и малой температуры плавления медь входит в семёрку металлов, известных человеку с очень древних времён и один из первых металлов, широко освоенных человеком .
Одни из самых древних изделий из меди, а также шлак — свидетельство выплавки её из руд — найдены на территории Турции, при раскопках поселения Чатал-Гююк, относящегося к периоду медного века.
Медный век, когда значительное распространение получили медные предметы, следует во всемирной истории за каменным веком и предшествует бронзовому. Медь как художественный материал использовался для изготовления украшений, скульптур, утвари и посуды.


В наши дни медь широко используется в промышленности разного рода из-за:
- высокой теплопроводимости;
- высокой электропроводимости;
- ковкости;
- хороших литейных качеств;
- большого сопротивления на разрыв;
- химической стойкости.


Около 40% меди идёт на изготовление различных электрических проводов и кабелей.
Кроме того, медь обладает высокой декоративной возможностью, что активно используется при изготовлении предметов декоративно-прикладного искусства и даже дизайне интерьеров.
На равне с прекрасной деформируемостью и устойчивостью к условиям окружающей среды, высокая декоративность меди обусловлена потрясающей цветовой палитрой патины, образующейся на ее поверхности.
Патина — пленка, образующаяся на поверхности металла в ходе окисления под влиянием окружающей среды.
Химический состав и цвет патины слегка отличается в зависимости от окружающей среды и формирует химически стабильный и прочный защитный слой, изолирующий металл от внешней среды. Патина предохраняет металл от дальнейшего разрушения. В случае механических повреждений эта поверхность восстанавливается сама.
Для соединений, образующихся на поверхности металлической меди характерны цвета: Cu2O — красный (в природе в виде минерала куприт), CuO — черный (в природе в виде минерала тенорит), CuCl2+h3O — голубой. Во влажном воздухе на поверхности меди образуются меднозакисные соли: в присутствии углекислого газа образуется зеленоватая пленка карбонатов состава Cu(OH)2·CuCO3; так как в воздухе всегда имеются следы сернистого газа и сероводорода, то в составе поверхностной пленки на металлической меди обычно имеются и сернистые соединения, в виде основного сульфата (II) — (CuOH)2 SO4.

В естественных условиях цвет меди изменяется несколько раз, начиная с момента рождения и до полного формирования патины на ее поверхности. Непосредственно после изготовления металла он покрывается оксидом Cu2O и поверхность меди становится нежно-розовая и блестящая. Под действием кислорода воздуха пленка из оксида меди Cu2O становится более толстой и цвет густеет; медь становится ярко-красной.

Затем на ней начинает образовываться оксид меди CuO черного цвета. Поэтому, по мере наращивания слоя CuO поверхность меди становится тусклой и матовой. Затем цвет темнеет и постепенно меняется на коричневый. Становясь все более непрозрачным, слой CuO меняет цвет меди с темно-коричневого в итоге на антрацитово-черный.

Затем эта поверхность развивается далее, под воздействием находящихся в воздухе углерода, серы, хлоридов и влаги на ней образуются различные меднозакисные соли, обладающие зеленым цветом, иногда с синеватыми или голубоватыми оттенками. С течением времени наступает последняя стадия процесса окисления и на поверхности образуется ярко-зеленый, иногда зеленый с голубовато-синим оттенком слой патины. В основной своей массе природная патина — это соединения родственные зеленоватому минералу меди — малахиту.


Многообразие и красоту этого металла можно отразить, приведя примеры предметов декоративно-прикладного искуссства, бижутерии и фотографий итерьеров, для создания которых использовалась медь.




















Широкое применение в ювелирной, инструментальной и машиностроительной промышленности и электротехнике нашли различные сплавы меди с другими веществами. Наиболее важными из них являются латуни, медноникеливые сплавы и бронзы.
Также необходимо отметить, что медь является важнейшим компонентом лигатур для изготовления драгоценных сплавов различных проб на основе серебра и золота.
Более подробно о сплавах меди, их свойствах и применении будет рассказано в следующих частях обзора 🙂
В завершении этой части приведу несколько советов по чистке медных украшений:

1. Для легкой чистки и удаления жирного налета медные украшения можно промыть в мыльной воде и/ или протереть бумагой или ветошью.
2. Для удаления пятен на медной поверхности и некрасивой патины:
- можно взять 9% уксус и мелкую пищевую соль. Из этих двух компонентов делают пасту, которой натирают медь, после чего пасту смывают, и ваше украшение блестит, как новое;
ВНИМАНИЕ: при этом методе счищается ВСЯ патина, т.е. если вы хотите сохранить состаренный вид изделия, данный метод не применять.
- ярко-зеленый налет на медном изделии можно удалить с помощью 10%-ного раствора лимонной кислоты — опустить изделие в нагретый раствор или протереть половинкой лимона. и промыть водой;
ВНИМАНИЕ: при этом методе счищается ВСЯ патина обработанная поверхность приобретает красновато-розовый оттенок, т.е. если вы хотите сохранить состаренный вид изделия, данный метод не применять.
3. Для удаления царапин и крохотных вмятин поверхность изделия можно потереть наждачной бумагой — нулевкой. Выбирать наждачку нужно внимательно, так как слишком грубая оставит полосы и может испортить внешний вид изделия. Самая подходящая — имеющая зернистость 2500 и выше.
ВНИМАНИЕ: не применять, если изделие имеет декоративную патину и вставки — камни, стекло, эмаль (есть риск их поцарапать даже нулевкой).
Хранить медные украшения надо подальше от прямого солнечного света, парфюмерии и воды.
Большое спасибо за внимание! 🙂
www.livemaster.ru
