Олово Sn химический элемент
Олово — один из немногих металлов, известных человеку еще с доисторических времен. Олово и медь были открыты раньше железа, а сплав их, бронза, — это, по-видимому, самый первый «искусственный» материал, первый материал, приготовленный человеком.
Результаты археологических раскопок позволяют считать, что еще за пять тысячелетий до нашей эры люди умели выплавлять и само олово. Известно, что древние египтяне олово для производства бронзы возили из Персии.
Под названием «трапу» этот металл описан в древнеиндийской литературе. Латинское название олова stannum происходит от санскритского «ста», что означает «твердый».
Упоминание об олове встречается и у Гомера. Почти за десять веков до новой эры финикияне доставляли оловянную руду с Британских островов, называвшихся тогда Касситеридами. Отсюда название касситерита — важнейшего из минералов олова; состав его Sn02. Другой важный минерал — станнин, или оловянный колчедан, Cu2FeSnS
Между прочим, наши предки располагали более богатыми оловянными рудами, чем мы. Можно было выплавлять металл непосредственно из руд, находящихся на поверхности Земли и обогащенных в ходе естественных процессов выветривания и вымывания. В наше время таких руд уже нет. В современных условиях процесс получения олова многоступенчатый и трудоемкий. Руды, из которых выплавляют олово теперь, сложны по составу: кроме элемента № 50 (в виде окисла или сульфида) в них обычно присутствуют кремний, железо, свинец, медь, цинк, мышьяк, алюминий, кальций, вольфрам и другие элементы. Нынешние оловянные руды редко содержат больше 1 % Sn, а россыпи — и того меньше: 0,01—0,02% Sn. Это значит, что для получения килограмма олова необходимо добыть и переработать по меньшей мере центнер руды.
Как получают олово из руд
Производство элемента № 50 из руд и россыпей всегда начинается с обогащения. Методы обогащения оловянных руд довольно разнообразны. Применяют, в частности, гравитационный метод, основанный на различии плотности основного и сопутствующих минералов. При этом нельзя забывать, что сопутствующие далеко не всегда бывают пустой породой. Часто они содержат ценные металлы, например вольфрам, титан, лантаноиды. В таких случаях из оловянной руды пытаются извлечь все ценные компоненты.
Состав полученного оловянного концентрата зависит от сырья, и еще от того, каким способом этот концентрат получали. Содержание олова в нем колеблется от 40 до 70%. Концентрат направляют в печи для обжига (при 600—700° С), где из него удаляются относительно летучие примеси мышьяка и серы. А большую часть железа, сурьмы, висмута и некоторых других металлов уже после обжига выщелачивают соляной кислотой. После того как это сделано, остается отделить олово от кислорода и кремния. Поэтому последняя стадия производства чернового олова — плавка с углем и флюсами в отражательных или электрических печах. С физико-химической точки зрения этот процесс аналогичен доменному: углерод «отнимает» у олова кислород, а флюсы превращают двуокись кремния в легкий по сравнению с металлом шлак.
Еще один источник
Для того чтобы получить килограмм олова, не обязательно перерабатывать центнер руды. Можно поступить иначе: «ободрать» 2000 старых консервных банок.
Всего лишь полграмма олова приходится на каждую банку. Но помноженные на масштабы производства эти полуграммы превращаются в десятки тонн… Доля «вторичного» олова в промышленности капиталистических стран составляет примерно треть общего производства. В нашей стране работают около ста промышленных установок по регенерации олова.
Олово в сплавах
На консервные банки идет примерно половина мирового производства олова. Другая половина — в металлургию, для получения различных сплавов. Мы не будем подробно рассказывать о самом известном из сплавов олова — бронзе, адресуя читателей к статье о меди — другом важнейшем компоненте бронз. Это тем более оправдано, что есть безоловянные бронзы, но нет «безмедных». Одна из главных причин создания безоловянных бронз — дефицитность элемента № 50. Тем не менее бронза, содержащая олово, по-прежнему остается важным материалом и для машиностроения, и для искусства.
Чаще всего оловянные сплавы применяют в качестве антифрикционных материалов или припоев. Первые позволяют сохранять машины и механизмы, уменьшая потери на трение; вторые соединяют металлические детали.
Из всех антифрикционных сплавов наилучшнми свойствами обладают оловянные баббиты, в составе которых до 90% олова. Мягкие и легкоплавкие свинцовооловянные припои хорошо смачивают поверхность большинства металлов, обладают высокой пластичностью и сопротивлением усталости. Однако область их применения ограничивается из-за недостаточной механической прочности самих припоев.
Между прочим, многие сплавы олова — истинные химические соединения элемента № 50 с другими металлами. Сплавляясь, олово взаимодействует с кальцием, магнием, цирконием, титаном, многими редкоземельными элементами. Образующиеся при этом соединения отличаются довольно большой тугоплавкостью. Так, станнид циркония Zr
Тот факт, что элемент № 50 образует довольно много-численные сплавы такого рода, заставляет критически отнестись к утверждению, что лишь 7% производимого в мире олова расходуется в виде химических соединений. Видимо, речь здесь идет только о соединениях с неметаллами.
Соединения с неметаллами
Из этих веществ наибольшее значение имеют хлориды. В тетрахлориде олова SnCl4 растворяются иод, фосфор, сера, многие органические вещества. Поэтому и используют его главным образом как весьма специфический растворитель. Дихлорид олова SnCl2 применяют как про-траву при крашении и как восстановитель при синтезе органических красителей. Те же функции в текстильном производстве еще у одного соединения элемента № 50 — станната натрия Na2
Промышленность ограниченно использует и окислы олова. SnO применяют для получения рубинового стекла, a Sn02 — белой глазури. Золотисто-Желтые кристаллы дисульфида олйва SnS2 нередко называют сусальным золотом, которым «золотят» дерево, гипс. Это, если можно так выразиться, самое «антисовременное» применение соединений олова. А самое современное?
Если иметь в виду только соединения олова, то это применение станната бария BaSn03 в радиотехнике в качестве превосходного диэлектрика. А один из изотопов олова, il9Sn, сыграл заметную роль при изучении эффекта Месс- бауэра — явления, благодаря которому был создан новый метод исследования — гамма-резонансная спектроскопия. И это не единственный случай, когда древний металл сослужил службу современной науке.
Об оловоорганике
Элементоорганических соединений, в состав которых входит олово, известно великое множество. Первое из них получено еще в 1852 г.
Сначала вещества этого класса получали лишь одним способом — в обменной реакции между неорганическими соединениями олова и реактивами Гриньяра. Вот пример такой реакции:
Соединения состава SnR4 широкого практического при-менения не нашли. Но именно из них получены другие оловоорганические вещества, польза которых несомненна.
Впервые интерес к оловоорганнке возник в годы первой мировой войны. Почти все органические соединения олова, полученные к тому времени, были токсичны. В качестве отравляющих веществ эти соединения не были использованы, их токсичностью для насекомых, плесневых грибков, вредных микробов воспользовались позже. На основе ацетата трифенилолова (C6H5)3SnOOCCH3 был создан эффективный препарат для борьбы с грибковыми заболеваниями картофеля и сахарной свеклы. У этого препарата оказалось еще одно полезное свойство: он стимулировал рост и развитие растений.
Для борьбы с грибками, развивающимися в аппаратах целлюлозно-бумажной промышленности, применяют другое вещество — гидроокись трибутилолова (С4Н9)зSnОН. Это намного повышает производительность аппаратуры.
Много «профессий» у дилаурината дибутилолова (C4H9)2Sn(OCOC11H23)2. Его используют в ветеринарной практике как средство против гельминтов (глистов). Это же вещество широко применяют в химической промышленности как стабилизатор поливинилхлорида и других полимерных материалов и как катализатор. Скорость
реакции образования уретанов (мономеры полиуретановых каучуков) в присутствии такого катализатора возрастает в 37 тыс. раз.
На основе оловоорганических соединений созданы эффективные инсектициды; оловоорганические стекла надежно защищают от рентгеновского облучения, полимерными свинец- и оловоорганическими красками покрывают подводные части кораблей, чтобы на них не нарастали моллюски.
Все это соединения четырехвалентного олова. Ограниченные рамки статьи не позволяют рассказать о многих других полезных веществах этого класса.
Органические соединения двухвалентного олова, напротив, немногочисленны и практического применения пока почти не находят.
О сером олове
Морозной зимой 1916 г. партия олова была отправлена по железной дороге с Дальнего Востока в европейскую часть России. Но на место прибыли не серебристобелые слитки, а преимущественно мелкий серый порошок.
За четыре года до этого произошла катастрофа с экспедицией полярного исследователя Роберта Скотта. Экспедиция, направлявшаяся к Южному полюсу, осталась без топлива: оно вытекло из железных сосудов сквозь швы, пропаянные оловом.
Примерно в те же годы к известному русскому химику В. В. Марковникову обратились из интендантства с просьбой объяснить, что происходит с лужеными чайниками, которыми снабжали русскую армию. Чайник, который принесли в лабораторию в качестве наглядного примера, был покрыт серыми пятнами и наростами, которые осыпались даже при легком постукивании рукой. Анализ показал, что и пыль, и наросты состояли только из олова, без каких бы то ни было примесей.
Что же происходило с металлом во всех этих случаях?
Как и многие другие элементы, олово имеет несколько аллотропических модификаций, несколько состояний. (Слово «аллотропия» переводится с греческого как «другое свойство», «другой поворот».) При нормальной плюсовой температуре олово выглядит так, что никто не может усомниться в принадлежности его к классу металлов.
Белый металл, пластичный, ковкий. Кристаллы белого олова (его называют еще бета-оловом) тетрагональные. Длина ребер элементарной кристаллической решетки — 5,82 и 3,18 А. Но при температуре ниже 13,2° С «нормальное» состояние олова иное. Едва достигнут этот температурный порог, в кристаллической структуре оловянного слитка начинается перестройка. Белое олово превращается в порошкообразное серое, или альфа-олово, и чем ниже температура, тем больше скорость этого превращения. Максимума она достигает при минус 39° С.
Кристаллы серого олова кубической конфигурации; размеры их элементарных ячеек больше — длина ребра 6,49 А. Поэтому плотность серого олова заметно меньше, чем белого: 5,76 и 7,3 г/см3 соответственно.
Результат превращения белого олова в серое иногда называют «оловянной чумой». Пятна и наросты на армейских чайниках, вагоны с оловянной пылью, швы, ставшие проницаемыми для жидкости,— следствия этой «болезни».
Почему сейчас не случаются подобные истории? Только по одной причине: оловянную чуму научились «лечить». Выяснена ее физико-химическая природа, установлено, как влияют на восприимчивость металла к «чуме» те или иные добавки. Оказалось, что алюминий и цинк способствуют этому процессу, а висмут, свинец и сурьма, напротив, противодействуют ему.
Кроме белого и серого олова, обнаружена еще одна аллотропическая модификация элемента № 50 — гамма-олово, устойчивое при температуре выше 161° С. Отличительная черта такого олова — хрупкость. Как и все металлы, с ростом температуры олово становится пластичнее, но только при температуре ниже 161° С. Затем оно полностью утрачивает пластичность, превращаясь в гамма- олово, и становится настолько хрупким, что его можно истолочь в порошок. Стаканы из олова
Еще раз о дефиците метела
Часто статьи об элементах заканчиваются рассуждениями автора о будущем своего «героя». Как правило, рисуется оно в розовом свете. Автор статьи об олове лишен этой возможности: будущее олова — металла, несомненно, Полезнейшего — неясно. Неясно только по одной причине.
Несколько лет пазад американское Горное бюро опубликовало расчеты, из которых следовало, что разведанных запасов элемента № 50 хватит миру самое большее на 35 лет. Правда, уже после этого было найдено несколько новых месторождений, в том числе крупнейшее в Европе, расположенное на территории Польской Народной Республики. И тем не менее дефицит олова продолжает тревожить специалистов.
Поэтому, заканчивая рассказ об элементе № 50, мы хотим еще раз напомнить о необходимости экономить и беречь олово.
Нехватка этого металла волновала даже классиков литературы. Помните у Андерсена? «Двадцать четыре солдатика были совершенно одинаковые, а двадцать пятый солдатик был одноногий. Его отливали последним, и олова немного не хватило». Теперь олова не хватает не немного. Недаром даже двуногие оловянные солдатики стали редкостью — чаще встречаются пластмассовые. Но при всем уважении к полимерам заменить олово они могут далеко не всегда.
ИЗОТОПЫ. Олово — один из самых «многоизотопных» элементов: природное олово состоит из десяти изотопов с массовыми числами 112, 114—120, 122 п 124. Самый распространенный из них i20Sn, на его долю приходится около 33% всего земного олова. Почти в 100 раз меньше олова-115— самого редкого изотопа элемента № 50.
Еще 15 изотопов олова с массовыми числами 108—111, 113, 121, 123, 125—132 получены искусственно. Время жизни этих изотопов далеко не одинаково. Так, олово-123 имеет период полураспада 136 дней, а олово-132 всего 2,2 минуты.
ПОЧЕМУ БРОНЗУ НАЗВАЛИ БРОНЗОЙ? Слово «бронза» почти одинаково звучит на многих европейских языках. Его происхождение связывают с названием небольшого итальянского порта на берегу Адриатического моря — Бриндизи. Именно через этот порт доставляли бронзу в Европу в старину, и в древнем Риме этот сплав называли «эс бриндиси»— медь из Бриндизи.
В ЧЕСТЬ ИЗОБРЕТАТЕЛЯ. Латинское слово frictio означает «трение». Отсюда название антифрикционных материалов, то есть материалов «против трепия». Они мало истираются, отличаются мягкостью и тягучестью. Главное их применение — изготовление подшипниковых вкладышей. Первый антифрикционный сплав на основе олова и свинца предложил в 1839 г. инженер Баббит. Отсюда название большой и очень важной группы антифрикционных сплавов — баббитов.
jKECTb ДЛЯ КОНСЕРВИРОВАНИЯ. Способ длительного сохранения пищевых продуктов консервированием в банках из белой жести, покрытой оловом, первым предложил французский повар ф. Аппер в 1809 г.
СО ДНА ОКЕАНА. В 1976 г. начало работать необычное предприятие, которое сокращенно называют РЭП. Расшифровывается это так: разведочно-эксплуатационное предприятие. Оно размещается в основном на кораблях. За Полярным кругом, в море Лаптевых, в районе Ванькиной губы РЭП добывает с морского дна оловоносный песок. Здесь же, на борту одного из судов, работает обогатительная фабрика.
МИРОВОЕ ПРОИЗВОДСТВО. По американским данным, мировое производство олова в конце прошлого века составляло 174—180 тыс. т.
natural-museum.ru
олово — это… Что такое олово?
О́ЛОВО -а; ср. Химический элемент (Sn), мягкий ковкий серебристо-белый металл (применяется для пайки, лужения, приготовления сплавов и т.п.).
О́ЛОВО (лат. Stannum), Sn, химический элемент с атомным номером 50, атомная масса 118,710). Латинское «stannum» первоначально означало сплав серебра и свинца. «Оловом» в ряде славянских языков называли свинец. Химический символ олова Sn читается «станнум». Природное олово состоит из девяти стабильных нуклидов (см. НУКЛИД) с массовыми числами 112 (в смеси 0,96% по массе), 114 (0,66%), 115 (0,35%), 116 (14,30%), 117 (7,61%), 118 (24,03%), 119 (8,58%), 120 (32,85%), 122 (4,72%), и одного слабо радиоактивного олова-124 (5,94%). 124Sn — бета-излучатель, его период полураспада очень велик и составляет T1/2 = 1016–1017 лет. Олово расположено в пятом периоде в IVА группе периодической системы элементов Д. И. Менделеева. Конфигурация внешнего электронного слоя 5s25p2. В своих соединениях олово проявляет степени окисления +2 и +4 (соответственно валентности II и IV).Металлический радиус нейтрального атома олова 0,158 нм, радиусы иона Sn2+ 0,118 нм и иона Sn4+ 0,069 нм (координационное число 6). Энергии последовательной ионизации нейтрального атома олова равны 7,344 эВ, 14,632, 30,502, 40,73 и 721,3 эВ. По шкале Полинга электроотрицательность олова 1,96, то есть олово находится на условной границе между металлами и неметаллами.
История открытия
Когда человек впервые познакомился с оловом точно сказать нельзя. Олово и его сплавы известны человечеству с древнейших времен. Упоминание об олове есть в ранних книгах Ветхого Завета. Сплавы олова с медью, так называемые оловянные бронзы (см. БРОНЗА), по-видимому, стали использоваться более чем за 4000 лет до нашей эры. А с самим металлическим оловом человек познакомился значительно позже, примерно около 800 года до нашей эры. Из чистого олова в древности изготовляли посуду и украшения, очень широко применяли изделия из бронзы.
Нахождение в природе
Олово — редкий рассеянный элемент, по распространенности в земной коре олово занимает 47-е место. Содержание олова в земной коре составляет, по разным данным, от 2·10-4 до 8·10–3% по массе. Основной минерал олова — касситерит (см. КАССИТЕРИТ) (оловянный камень) SnO2, содержащий до 78,8 % олова. Гораздо реже в природе встречается станнин (см. СТАННИН) (оловянный колчедан) — Cu2FeSnS4 (27,5 % Sn).
Получение
Для добычи олова в настоящее время используют руды, в которых его содержание равно или немного выше 0,1%. На первом этапе руду обогащают (методом гравитационной флотации или магнитной сепарации). Таким образом удается повысить содержание олова в руде до 40—70%. Далее проводят обжиг концентрата в кислороде для удаления примесей серы и мышьяка. Затем полученный таким образом оксид SnO2 восстанавливают углем или алюминием (цинком) в электропечах:
SnO2 + C = Sn + CO2. Особо чистое олово полупроводниковой чистоты готовят электрохимическим рафинированием или методом зонной плавки.
Физические и химические свойства
Простое вещество олово полиморфно. В обычных условиях оно существует в виде бета-модификации (белое олово), устойчивой выше 13,2°C. Белое олово — это серебристо-белый, мягкий, пластичный металл, обладающий тетрагональной элементарной ячейкой, параметры a=0.5831, c=0.3181 нм. Координационное окружение каждого атома олова в нем — октаэдр. Плотность бета-Sn 7,29 г/см3 . Температура плавления 231,9°C, температура кипения 2270°C.
При охлаждении, например, при морозе на улице, белое олово переходит в альфа-модификацию (серое олово). Серое олово имеет структуру алмаза (кубическая кристаллическая решетка с параметром а = 0,6491 нм). В сером олове координационный полиэдр каждого атома — тетраэдр, координационное число 4. Фазовый переход бета-Sn ® альфа-Sn сопровождается увеличением удельного объема на 25,6%, что приводит к рассыпанию олова в порошок. В старые времена наблюдавшееся во время сильных холодов рассыпание оловянных изделий называли «оловянной чумой». В результате этой «чумы» пуговицы на обмундировании солдат, их пряжки, кружки, ложки рассыпались, и армия могла потерять боеспособность.
Из-за сильного различия структур двух модификаций олова разнятся и их электрофизические свойства. Так, бета-Sn — металл, а альфа-Sn относится к числу полупроводников (см. ПОЛУПРОВОДНИКИ). Ниже 3,72 К альфа-Sn переходит в сверхпроводящее состояние. Стандартный электродный потенциал E°Sn2+/Sn равен –0.136 В, а E пары °Sn4+/Sn2+ 0.151 В. При комнатной температуре олово, подобно соседу по группе германию, (см. ГЕРМАНИЙ) устойчиво к воздействию воздуха или воды. Такая инертность объясняется образованием поверхностной пленки оксидов. Заметное окисление олова на воздухе начинается при температурах выше 150°C:
Sn + O2 = SnO2.
При нагревании олово реагирует с большинством неметаллов. При этом образуются соединения в степени окисления +4, которая более характерна для олова, чем +2. Например:
Sn + 2Cl2 = SnCl4
С концентрированной соляной кислотой олово медленно реагирует:
Sn + 4HCl = SnCl4 + H2
Возможно также образование хлороловянных кислот составов HSnCl3, H2SnCl4 и других, например:
Sn + 3HCl = HSnCl3 + 2H2
В разбавленной серной кислоте олово не растворяется, а с концентрированной реагирует очень медленно. Состав продукта реакции олова с азотной кислотой зависит от концентрации кислоты. В концентрированной азотной кислоте образуется оловянная кислота b-SnO2·nH2O (иногда ее формулу записывают как H2SnO3). При этом олово ведет себя как неметалл:
Sn + 4HNO3конц. = b-SnO2·H2OЇ + 4NO2 + H2O
При взаимодействии с разбавленной азотной кислотой олово проявляет свойства металла. В результате реакции образуется соль нитрат олова(II):
3Sn + 8HNO3 разб. = 3Sn(NO3)2 + 2NO + 4H2O.
При нагревании олово, подобно свинцу, может реагировать с водными растворами щелочей. При этом выделяется водород и образуется гидроксокомплекс Sn(II), например:
Sn + 2KOH +2H2O = K2[Sn(OH)4] + H2
Гидрид олова — станнан SnH4 — можно получить по реакции:
SnCl4 + Li[AlH4] = SnH4 + LiCl + AlCl3.
Этот гидрид весьма нестоек и медленно разлагается уже при температуре 0°C. Олову отвечают два оксида SnO2 (образующийся при обезвоживании оловянных кислот) и SnO. Последний можно получить при слабом нагревании гидроксида олова(II) Sn(OH)2 в вакууме:
Sn(OH)2 = SnO + H2O
При сильном нагреве оксид олова(II) диспропорционирует:
2SnO = Sn + SnO2
При хранении на воздухе монооксид SnO постепенно окисляется:
2SnO + O2 = 2SnO2.
При гидролизе растворов солей олова(IV) образуется белый осадок — так называемая альфа-оловянная кислота:
SnCl4 + 4NH3 + 6H2O = H2[Sn(OH)6] + 4NH4Cl.
H2[Sn(OH)6] = -SnO2·nH2OЇ + 3H2O.
Свежеполученная альфа-оловянная кислота растворяется в кислотах и щелочах:
a-SnO2·nH2O + KOH = K2[Sn(OH)6],
a-SnO2·nH2O + HNO3 = Sn(NO3)4 + H2O.
При хранении альфа-оловянная кислота стареет, теряет воду и переходит в бета-оловянную кислоту, которая отличается большей химической инертностью. Данное изменение свойств связывают с уменьшением числа активных HO–Sn группировок при стоянии и замене их на более инертные мостиковые –Sn–O–Sn– связи. При действии на раствор соли Sn(II) растворами сульфидов выпадает осадок сульфида олова(II):
Sn2+ + S2– = SnS
Этот сульфид может быть легко окислен до SnS2 раствором полисульфида аммония:
SnS + (NH4)2S2 = SnS2 + (NH4)2S
Образующийся дисульфид SnS2 растворяется в растворе сульфида аммония (NH4)2S:
SnS2 + (NH4)2S = (NH4)2SnS3. Четырехвалентное олово образует обширный класс оловоорганических соединений, используемых в органическом синтезе, в качестве пестицидов и других.
Применение
Важное применение олова — лужение железа и получение белой жести, которая используется в консервной промышленности. Для этих целей расходуется около 33% всего добываемого олова. До 60% производимого олова используется в виде сплавов с медью, медью и цинком, медью и сурьмой (подшипниковый сплав, или баббит (см. БАББИТЫ)), с цинком (упаковочная фольга) и в виде оловянно-свинцовых и оловянно-цинковых припоев (см. ПРИПОЙ). Олово способно прокатываться в тонкую фольгу — станиоль (см. СТАНИОЛЬ), такая фольга находит применение при производстве конденсаторов, органных труб, посуды, художественных изделий. Олово применяют для нанесения защитных покрытий на железо и другие металлы, а также на металлические изделия (лужение). Дисульфид олова SnS2 применяют в составе красок, имитирующих позолоту («сусальное золото»). Искусственный радионуклид олова 119Sn — источник гамма-излучения в мессбауэровской спектроскопии.
Физиологическое действие
О роли олова в живых организмах практически ничего не известно. В теле человека содержится примерно (1—2)· 10–4% олова, а его ежедневное поступление с пищей составляет 0,2—3,5 мг. Олово представляет опасность для человека в виде паров и различных аэрозольных частиц, пыли. При воздействии паров или пыли олова может развиться станноз — поражение легких. Очень токсичны некоторые оловоорганические соединения. Временно допустимая концентрация соединений олова в атмосферном воздухе 0,05 мг/м3, ПДК олова в пищевых продуктах 200 мг/кг, в молочных продуктах и соках — 100 мг/кг. Токсическая доза олова для человека — 2 г.
dic.academic.ru
Олово — Мегаэнциклопедия Кирилла и Мефодия — статья
О́лово (лат. Stannum), Sn, химический элемент с атомным номером 50, атомная масса 118, 710). Латинское «stannum» первоначально означало сплав серебра и свинца. «Оловом» в ряде славянских языков называли свинец. Химический символ олова Sn читается «станнум». Природное олово состоит из девяти стабильных нуклидов с массовыми числами 112 (в смеси 0, 96% по массе), 114 (0, 66%), 115 (0, 35%), 116 (14, 30%), 117 (7, 61%), 118 (24, 03%), 119 (8, 58%), 120 (32, 85%), 122 (4, 72%), и одного слабо радиоактивного олова-124 (5, 94%). 124Sn— бета-излучатель, его период полураспада очень велик и составляет T1/2 = 1016–1017 лет. Олово расположено в пятом периоде в IVА группе периодической системы элементов Д. И. Менделеева. Конфигурация внешнего электронного слоя 5s25p2. В своих соединениях олово проявляет степени окисления +2 и +4 (соответственно валентности II и IV).Металлический радиус нейтрального атома олова 0, 158 нм, радиусы иона Sn2+ 0, 118 нм и иона Sn4+ 0, 069 нм (координационное число 6). Энергии последовательной ионизации нейтрального атома олова равны 7, 344 эВ, 14, 632, 30, 502, 40, 73 и 721, 3 эВ. По шкале Полинга электроотрицательность олова 1, 96, то есть олово находится на условной границе между металлами и неметаллами.
Когда человек впервые познакомился с оловом точно сказать нельзя. Олово и его сплавы известны человечеству с древнейших времен. Упоминание об олове есть в ранних книгах Ветхого Завета. Сплавы олова с медью, так называемые оловянные бронзы, по-видимому, стали использоваться более чем за 4000 лет до нашей эры. А с самим металлическим оловом человек познакомился значительно позже, примерно около 800 года до нашей эры. Из чистого олова в древности изготовляли посуду и украшения, очень широко применяли изделия из бронзы.Олово — редкий рассеянный элемент, по распространенности в земной коре олово занимает 47-е место. Содержание олова в земной коре составляет, по разным данным, от 2·10-4 до 8·10–3% по массе. Основной минерал олова — касситерит (оловянный камень) SnO2, содержащий до 78, 8 % олова. Гораздо реже в природе встречается станнин (оловянный колчедан) — Cu2FeSnS4 (27, 5 % Sn).Для добычи олова в настоящее время используют руды, в которых его содержание равно или немного выше 0, 1%. На первом этапе руду обогащают (методом гравитационной флотации или магнитной сепарации). Таким образом удается повысить содержание олова в руде до 40-70%. Далее проводят обжиг концентрата в кислороде для удаления примесей серы и мышьяка. Затем полученный таким образом оксид SnO2 восстанавливают углем или алюминием (цинком) в электропечах:
SnO2 + C = Sn + CO2. Особо чистое олово полупроводниковой чистоты готовят электрохимическим рафинированием или методом зонной плавки.
Простое вещество олово полиморфно. В обычных условиях оно существует в виде бета-модификации (белое олово), устойчивой выше 13, 2°C. Белое олово — это серебристо-белый, мягкий, пластичный металл, обладающий тетрагональной элементарной ячейкой, параметры a=0.5831, c=0.3181 нм. Координационное окружение каждого атома олова в нем — октаэдр. Плотность бета-Sn 7, 29 г/см3 . Температура плавления 231, 9°C, температура кипения 2270°C.
При охлаждении, например, при морозе на улице, белое олово переходит в альфа-модификацию (серое олово). Серое олово имеет структуру алмаза (кубическая кристаллическая решетка с параметром а = 0, 6491 нм). В сером олове координационный полиэдр каждого атома — тетраэдр, координационное число 4. Фазовый переход бета-Sn → альфа-Sn сопровождается увеличением удельного объема на 25, 6%, что приводит к рассыпанию олова в порошок. В старые времена наблюдавшееся во время сильных холодов рассыпание оловянных изделий называли «оловянной чумой». В результате этой «чумы» пуговицы на обмундировании солдат, их пряжки, кружки, ложки рассыпались, и армия могла потерять боеспособность.
Из-за сильного различия структур двух модификаций олова разнятся и их электрофизические свойства. Так, бета-Sn — металл, а альфа-Sn относится к числу полупроводников. Ниже 3, 72 К альфа-Sn переходит в сверхпроводящее состояние. Стандартный электродный потенциал E°Sn2+/Sn равен –0.136 В, а E пары °Sn4+/Sn2+ 0.151 В. При комнатной температуре олово, подобно соседу по группе германию, устойчиво к воздействию воздуха или воды. Такая инертность объясняется образованием поверхностной пленки оксидов. Заметное окисление олова на воздухе начинается при температурах выше 150°C:Sn + O2 = SnO2.
При нагревании олово реагирует с большинством неметаллов. При этом образуются соединения в степени окисления +4, которая более характерна для олова, чем +2. Например:
Sn + 2Cl2 = SnCl4
С концентрированной соляной кислотой олово медленно реагирует:
Sn + 4HCl = SnCl4 + H2
Возможно также образование хлороловянных кислот составов HSnCl3, H2SnCl4 и других, например:
Sn + 3HCl = HSnCl3 + 2H2
В разбавленной серной кислоте олово не растворяется, а с концентрированной реагирует очень медленно. Состав продукта реакции олова с азотной кислотой зависит от концентрации кислоты. В концентрированной азотной кислоте образуется оловянная кислота β-SnO2·nH2O (иногда ее формулу записывают как H2SnO3). При этом олово ведет себя как неметалл:
Sn + 4HNO3конц. = β-SnO2·H2O↓ + 4NO2 + H2O
При взаимодействии с разбавленной азотной кислотой олово проявляет свойства металла. В результате реакции образуется соль нитрат олова(II):
3Sn + 8HNO3 разб. = 3Sn(NO3)2 + 2NO + 4H2O.
При нагревании олово, подобно свинцу, может реагировать с водными растворами щелочей. При этом выделяется водород и образуется гидроксокомплекс Sn(II), например:
Sn + 2KOH +2H2O = K2[Sn(OH)4] + H2
Гидрид олова — станнан SnH4 — можно получить по реакции:
SnCl4 + Li[AlH4] = SnH4 + LiCl + AlCl3.
Этот гидрид весьма нестоек и медленно разлагается уже при температуре 0°C. Олову отвечают два оксида SnO2 (образующийся при обезвоживании оловянных кислот) и SnO. Последний можно получить при слабом нагревании гидроксида олова(II) Sn(OH)2 в вакууме:
Sn(OH)2 = SnO + H2O
При сильном нагреве оксид олова(II) диспропорционирует:
2SnO = Sn + SnO2
При хранении на воздухе монооксид SnO постепенно окисляется:
2SnO + O2 = 2SnO2.
При гидролизе растворов солей олова(IV) образуется белый осадок — так называемая альфа-оловянная кислота:
SnCl4 + 4NH3 + 6H2O = H2[Sn(OH)6] + 4NH4Cl.
H2[Sn(OH)6] = -SnO2·nH2OЇ + 3H2O.
Свежеполученная альфа-оловянная кислота растворяется в кислотах и щелочах:
α-SnO2·nH2O + KOH = K2[Sn(OH)6],
α-SnO2·nH2O + HNO3 = Sn(NO3)4 + H2O.
При хранении альфа-оловянная кислота стареет, теряет воду и переходит в бета-оловянную кислоту, которая отличается большей химической инертностью. Данное изменение свойств связывают с уменьшением числа активных HO–Sn группировок при стоянии и замене их на более инертные мостиковые –Sn–O–Sn– связи. При действии на раствор соли Sn(II) растворами сульфидов выпадает осадок сульфида олова(II):
Sn2+ + S2– = SnS
Этот сульфид может быть легко окислен до SnS2 раствором полисульфида аммония:
SnS + (NH4)2S2 = SnS2 + (NH4)2S
Образующийся дисульфид SnS2 растворяется в растворе сульфида аммония (NH4)2S:
SnS2 + (NH4)2S = (NH4)2SnS3. Четырехвалентное олово образует обширный класс оловоорганических соединений, используемых в органическом синтезе, в качестве пестицидов и других.
Важное применение олова — лужение железа и получение белой жести, которая используется в консервной промышленности. Для этих целей расходуется около 33% всего добываемого олова. До 60% производимого олова используется в виде сплавов с медью, медью и цинком, медью и сурьмой (подшипниковый сплав, или баббит), с цинком (упаковочная фольга) и в виде оловянно-свинцовых и оловянно-цинковых припоев. Олово способно прокатываться в тонкую фольгу — станиоль, такая фольга находит применение при производстве конденсаторов, органных труб, посуды, художественных изделий. Олово применяют для нанесения защитных покрытий на железо и другие металлы, а также на металлические изделия (лужение). Дисульфид олова SnS2 применяют в составе красок, имитирующих позолоту («сусальное золото»). Искусственный радионуклид олова 119Sn — источник гамма-излучения в мессбауэровской спектроскопии.О роли олова в живых организмах практически ничего не известно. В теле человека содержится примерно (1-2)· 10–4% олова, а его ежедневное поступление с пищей составляет 0, 2-3, 5 мг. Олово представляет опасность для человека в виде паров и различных аэрозольных частиц, пыли. При воздействии паров или пыли олова может развиться станноз — поражение легких. Очень токсичны некоторые оловоорганические соединения. Временно допустимая концентрация соединений олова в атмосферном воздухе 0, 05 мг/м3, ПДК олова в пищевых продуктах 200 мг/кг, в молочных продуктах и соках — 100 мг/кг. Токсическая доза олова для человека — 2 г.
- Спиваковский В. Б. Аналитическая химия олова. М., 1975.
- Большаков К. А., Федоров П. И. Химия и технология малых металлов. М., 1984.
megabook.ru
Популярная библиотека химических элементов. Раритетные издания. Наука и техника
Олово
| 50 | |
Sn |
4 18 18 8 2 |
| ОЛОВО | |
| 118,69 | |
| 5s25p2 | |
Олово – один из немногих металлов, известных человеку еще с доисторических времен. Олово и медь были открыты раньше железа, а сплав их, бронза, – это, по-видимому, самый первый «искусственный» материал, первый материал, приготовленный человеком.
Результаты археологических раскопок позволяют считать, что еще за пять тысячелетий до нашей эры люди умели выплавлять и само олово. Известно, что древние египтяне олово для производства бронзы возили из Персии.
Под названием «трапу» этот металл описан в древнеиндийской литературе. Латинское название олова stannum происходит от санскритского «ста», что означает «твердый».
Упоминание об олове встречается и у Гомера. Почти за десять веков до новой эры финикияне доставляли оловянную руду с Британских островов, называвшихся тогда Касситеридами. Отсюда название касситерита – важнейшего из минералов олова; состав его SnO2. Другой важный минерал – станнин, или оловянный колчедан, Cu2FeSnS4. Остальные 14 минералов элемента №50 встречаются намного реже и промышленного значения не имеют. Между прочим, наши предки располагали более богатыми оловянными рудами, чем мы. Можно было выплавлять металл непосредственно из руд, находящихся на поверхности Земли и обогащенных в ходе естественных процессов выветривания и вымывания. В наше время таких руд уже нет. В современных условиях процесс получения олова многоступенчатый и трудоемкий. Руды, из которых выплавляют олово теперь, сложны по составу: кроме элемента №50 (в виде окисла или сульфида) в них обычно присутствуют кремний, железо, свинец, медь, цинк, мышьяк, алюминий, кальций, вольфрам и другие элементы. Нынешние оловянные руды редко содержат больше 1% Sn, а россыпи – и того меньше: 0,01…0,02% Sn. Это значит, что для получения килограмма олова необходимо добыть и переработать по меньшей мере центнер руды.
Как получают олово из руд
Производство элемента №50 из руд и россыпей всегда начинается с обогащения. Методы обогащения оловянных руд довольно разнообразны. Применяют, в частности, гравитационный метод, основанный на различии плотности основного и сопутствующих минералов. При этом нельзя забывать, что сопутствующие далеко не всегда бывают пустой породой. Часто они содержат ценные металлы, например вольфрам, титан, лантаноиды. В таких случаях из оловянной руды пытаются извлечь все ценные компоненты.
Состав полученного оловянного концентрата зависит от сырья, и еще от того, каким способом этот концентрат получали. Содержание олова в нем колеблется от 40 до 70%. Концентрат направляют в печи для обжига (при 600…700°C), где из него удаляются относительно летучие примеси мышьяка и серы. А большую часть железа, сурьмы, висмута и некоторых других металлов уже после обжига выщелачивают соляной кислотой. После того как это сделано, остается отделить олово от кислорода и кремния. Поэтому последняя стадия производства чернового олова – плавка с углем и флюсами в отражательных или электрических печах. С физико-химической точки зрения этот процесс аналогичен доменному: углерод «отнимает» у олова кислород, а флюсы превращают двуокись кремния в легкий по сравнению с металлом шлак.
В черновом олове примесей еще довольно много: 5…8%. Чтобы получить металл сортовых марок (96,5…99,9% Sn), используют огневое или реже электролитическое рафинирование. А нужное полупроводниковой промышленности олово чистотой почти шесть девяток – 99,99985% Sn – получают преимущественно методом зонной плавки.
Еще один источник
Для того чтобы получить килограмм олова, не обязательно перерабатывать центнер руды. Можно поступить иначе: «ободрать» 2000 старых консервных банок.
Всего лишь полграмма олова приходится на каждую банку. Но помноженные на масштабы производства эти полуграммы превращаются в десятки тонн… Доля «вторичного» олова в промышленности капиталистических стран составляет примерно треть общего производства. В нашей стране работают около ста промышленных установок по регенерации олова.
Как же снимают олово с белой жести? Механическими способами сделать это почти невозможно, поэтому используют различие в химических свойствах железа и олова. Чаще всего жесть обрабатывают газообразным хлором. Железо в отсутствие влаги с ним не реагирует. Олово же соединяется с хлором очень легко. Образуется дымящаяся жидкость – хлорное олово SnCl4, которое применяют в химической и текстильной промышленности или отправляют в электролизер, чтобы получить там из него металлическое олово. И опять начнется «круговерть»: этим оловом покроют стальные листы, получат белую жесть. Из нее сделают банки, банки заполнят едой и запечатают. Потом их вскроют, консервы съедят, банки выбросят. А потом они (не все, к сожалению) вновь попадут на заводы «вторичного» олова.
Другие элементы совершают круговорот в природе с участием растений, микроорганизмов и т.д. Круговорот олова – дело рук человеческих.
Олово в сплавах
На консервные банки идет примерно половина мирового производства олова. Другая половина – в металлургию, для получения различных сплавов. Мы не будем подробно рассказывать о самом известном из сплавов олова – бронзе, адресуя читателей к статье о меди – другом важнейшем компоненте бронз. Это тем более оправдано, что есть безоловянные бронзы, но нет «безмедных». Одна из главных причин создания безоловянпьтх бронз – дефицитность элемента №50. Тем не менее бронза, содержащая олово, по-прежнему остается важным материалом и для машиностроения, и для искусства.
Техника нуждается и в других оловянных сплавах. Их, правда, почти не применяют в качестве конструкционных, материалов: они недостаточно прочны и слишком дороги. Зато у них есть другие свойства, позволяющие решать важные технические задачи при сравнительно небольших затратах материала.
Чаще всего оловянные сплавы применяют в качестве антифрикционных материалов или припоев. Первые позволяют сохранять машины и механизмы, уменьшая потери на трение; вторые соединяют металлические детали.
Из всех антифрикционных сплавов наилучшими свойствами обладают оловянные баббиты, в составе которых до 90% олова. Мягкие и легкоплавкие свинцовооловянные припои хорошо смачивают поверхность большинства металлов, обладают высокой пластичностью и сопротивлением усталости. Однако область их применения ограничивается из-за недостаточной механической прочности самих припоев.
Олово входит также в состав типографского сплава гарта. Наконец, сплавы на основе олова очень нужны электротехнике. Важнейший материал для электроконденсаторов – станиоль; это почти чистое олово, превращенное в тонкие листы (доля других металлов в станиоле не превышает 5%).
Между прочим, многие сплавы олова – истинные химические соединения элемента №50 с другими металлами. Сплавляясь, олово взаимодействует с кальцием, магнием, цирконием, титаном, многими редкоземельными элементами. Образующиеся при этом соединения отличаются довольно большой тугоплавкостью. Так, станнид циркония Zr3Sn2 плавится лишь при 1985°C. И «виновата» здесь не только тугоплавкость циркония, но и характер сплава, химическая связь между образующими его веществами. Или другой пример. Магний к числу тугоплавких металлов не отнесешь, 651°C – далеко не рекордная температура плавления. Олово плавится при еще более низкой температуре – 232°C. А их сплав – соединение Mg2Sn – имеет температуру плавления 778°C.
Тот факт, что элемент №50 образует довольно многочисленные сплавы такого рода, заставляет критически отнестись к утверждению, что лишь 7% производимого в мире олова расходуется в виде химических соединений («Краткая химическая энциклопедия», т. 3, с. 739). Видимо, речь здесь идет только о соединениях с неметаллами.
Соединения с неметаллами
Из этих веществ наибольшее значение имеют хлориды. В тетрахлориде олова SnCl4 растворяются иод, фосфор, сера, многие органические вещества. Поэтому и используют его главным образом как весьма специфический растворитель. Дихлорид олова SnCl2 применяют как протраву при крашении и как восстановитель при синтезе органических красителей. Те же функции в текстильном производстве еще у одного соединения элемента №50 – станната натрия Na2SnO3. Кроме того, с его помощью утяжеляют шелк.
Промышленность ограниченно использует и окислы олова. SnO применяют для получения рубинового стекла, a SnO2 – белой глазури. Золотисто-желтые кристаллы дисульфида олова SnS2 нередко называют сусальным золотом, которым «золотят» дерево, гипс. Это, если можно так выразиться, самое «антисовременное» применение соединений олова. А самое современное?
Если иметь в виду только соединения олова, то это применение станната бария BaSnO3 в радиотехнике в качестве превосходного диэлектрика. А один из изотопов олова, 119Sn, сыграл заметную роль при изучении эффекта Мессбауэра – явления, благодаря которому был создан новый метод исследования – гамма-резонансная спектроскопия. И это не единственный случай, когда древний металл сослужил службу современной науке.
На примере серого олова – одной из модификаций элемента №50 – была выявлена связь между свойствами и химической природой полупроводникового материала. И это, видимо, единственное, за что серое олово можно помянуть добрым словом: вреда оно принесло больше, тем пользы. Мы еще вернемся к этой разновидности элемента №50 после рассказа о еще одной большой и важной группе соединений олова.
Об оловоорганике
Элементоорганических соединений, в состав которых входит олово, известно великое множество. Первое из них получено еще в 1852 г.
Сначала вещества этого класса получали лишь одним способом – в обменной реакции между неорганическими соединениями олова и реактивами Гриньяра. Вот пример такой реакции:
SnCl4 + 4RMgX → SnR4 + 4MgXCl
(R здесь – углеводородный радикал, X – галоген).
Соединения состава SnR4 широкого практического применения не нашли. Но именно из них получены другие оловоорганические вещества, польза которых несомненна.
Впервые интерес к оловоорганике возник в годы первой мировой войны. Почти все органические соединения олова, полученные к тому времени, были токсичны. В качестве отравляющих веществ эти соединения не были использованы, их токсичностью для насекомых, плесневых грибков, вредных микробов воспользовались позже. На основе ацетата трифенилолова (C6H5)3SnOOCCH3 был создан эффективный препарат для борьбы с грибковыми заболеваниями картофеля и сахарной свеклы. У этого препарата оказалось еще одно полезное свойство: он стимулировал рост и развитие растений.
Для борьбы с грибками, развивающимися в аппаратах целлюлозно-бумажной промышленности, применяют другое вещество – гидроокись трибутилолова (С4Н9)3SnOH. Это намного повышает производительность аппаратуры.
Много «профессий» у дилаурината дибутилолова (C4H9)2Sn(OCOC11H23)2. Его используют в ветеринарной практике как средство против гельминтов (глистов). Это же вещество широко применяют в химической промышленности как стабилизатор поливинилхлорида и других полимерных материалов и как катализатор. Скорость реакции образования уретанов (мономеры полиуретановых каучуков) в присутствии такого катализатора возрастает в 37 тыс. раз.
На основе оловоорганических соединений созданы эффективные инсектициды; оловоорганические стекла надежно защищают от рентгеновского облучения, полимерными свинец- и оловоорганическими красками покрывают подводные части кораблей, чтобы на них не нарастали моллюски.
Все это соединения четырехвалентного олова. Ограниченные рамки статьи не позволяют рассказать о многих других полезных веществах этого класса.
Органические соединения двухвалентного олова, напротив, немногочисленны и практического применения пока почти не находят.
О сером олове
Морозной зимой 1916 г. партия олова была отправлена по железной дороге с Дальнего Востока в европейскую часть России. Но на место прибыли не серебристо-белые слитки, а преимущественно мелкий серый порошок.
За четыре года до этого произошла катастрофа с экспедицией полярного исследователя Роберта Скотта. Экспедиция, направлявшаяся к Южному полюсу, осталась без топлива: оно вытекло из железных сосудов сквозь швы, пропаянные оловом.
Примерно в те же годы к известному русскому химику В.В. Марковникову обратились из интендантства с просьбой объяснить, что происходит с лужеными чайниками, которыми снабжали русскую армию. Чайник, который принесли в лабораторию в качестве наглядного примера, был покрыт серыми пятнами и наростами, которые осыпались даже при легком постукивании рукой. Анализ показал, что и пыль, и наросты состояли только из олова, без каких бы то ни было примесей.
Что же происходило с металлом во всех этих случаях?
Как и многие другие элементы, олово имеет несколько аллотропических модификаций, несколько состояний. (Слово «аллотропия» переводится с греческого как «другое свойство», «другой поворот».) При нормальной плюсовой температуре олово выглядит так, что никто не может усомниться в принадлежности его к классу металлов.
Белый металл, пластичный, ковкий. Кристаллы белого олова (его называют еще бета-оловом) тетрагональные. Длина ребер элементарной кристаллической решетки – 5,82 и 3,18 Å. Но при температуре ниже 13,2°C «нормальное» состояние олова иное. Едва достигнут этот температурный порог, в кристаллической структуре оловянного слитка начинается перестройка. Белое олово превращается в порошкообразное серое, или альфа-олово, и чем ниже температура, тем больше скорость этого превращения. Максимума она достигает при минус 39°C.
Кристаллы серого олова кубической конфигурации; размеры их элементарных ячеек больше – длина ребра 6,49 Å. Поэтому плотность серого олова заметно меньше, чем белого: 5,76 и 7,3 г/см3 соответственно.
Результат превращения белого олова в серое иногда называют «оловянной чумой». Пятна и наросты на армейских чайниках, вагоны с оловянной пылью, швы, ставшие проницаемыми для жидкости, – следствия этой «болезни».
Почему сейчас не случаются подобные истории? Только по одной причине: оловянную чуму научились «лечить». Выяснена ее физико-химическая природа, установлено, как влияют на восприимчивость металла к «чуме» те или иные добавки. Оказалось, что алюминий и цинк способствуют этому процессу, а висмут, свинец и сурьма, напротив, противодействуют ему.
Кроме белого и серого олова, обнаружена еще одна аллотропическая модификация элемента №50 – гамма-олово, устойчивое при температуре выше 161°C. Отличительная черта такого олова – хрупкость. Как и все металлы, с ростом температуры олово становится пластичнее, но только при температуре ниже 161°C. Затем оно полностью утрачивает пластичность, превращаясь в гамма-олово, и становится настолько хрупким, что его можно истолочь в порошок.
Еще раз о дефиците
Часто статьи об элементах заканчиваются рассуждениями автора о будущем своего «героя». Как правило, рисуется оно в розовом свете. Автор статьи об олове лишен этой возможности: будущее олова – металла, несомненно, полезнейшего – неясно. Неясно только по одной причине.
Несколько лет назад американское Горное бюро опубликовало расчеты, из которых следовало, что разведанных запасов элемента №50 хватит миру самое большее на 35 лет. Правда, уже после этого было найдено несколько новых месторождений, в том числе крупнейшее в Европе, расположенное на территории Польской Народной Республики. И тем не менее дефицит олова продолжает тревожить специалистов.
Поэтому, заканчивая рассказ об элементе №50, мы хотим еще раз напомнить о необходимости экономить и беречь олово.
Нехватка этого металла волновала даже классиков литературы. Помните у Андерсена? «Двадцать четыре солдатика были совершенно одинаковые, а двадцать пятый солдатик был одноногий. Его отливали последним, и олова немного не хватило». Теперь олова не хватает не немного. Недаром даже двуногие оловянные солдатики стали редкостью – чаще встречаются пластмассовые. Но при всем уважении к полимерам заменить олово они могут далеко не всегда.
Изотопы
Олово – один из самых «многоизотопных» элементов: природное олово состоит из десяти изотопов с массовыми числами 112, 114…120, 122 и 124. Самый распространенный из них 120Sn, на его долю приходится около 33% всего земного олова. Почти в 100 раз меньше олова-115 – самого редкого изотопа элемента №50. Еще 15 изотопов олова с массовыми числами 108…111, 113, 121, 123, 125…132 получены искусственно. Время жизни этих изотопов далеко не одинаково. Так, олово-123 имеет период полураспада 136 дней, а олово-132 всего 2,2 минуты.
Почему бронзу назвали бронзой?
Слово «бронза» почти одинаково звучит на многих европейских языках. Его происхождение связывают с названием небольшого итальянского порта на берегу Адриатического моря – Бриндизи. Именно через этот порт доставляли бронзу в Европу в старину, и в древнем Риме этот сплав называли «эс бриндиси» – медь из Бриндизи.
В честь изобретателя
Латинское слово frictio означает «трение». Отсюда название антифрикционных материалов, то есть материалов «против трения». Они мало истираются, отличаются мягкостью и тягучестью. Главное их применение – изготовление подшипниковых вкладышей. Первый антифрикционный сплав на основе олова и свинца предложил в 1839 г. инженер Баббит. Отсюда название большой и очень важной группы антифрикционных сплавов – баббитов.
Жесть для консервирования
Способ длительного сохранения пищевых продуктов консервированием в банках из белой жести, покрытой оловом, первым предложил французский повар Ф. Аппер в 1809 г.
Со дна океана
В 1976 г. начало работать необычное предприятие, которое сокращенно называют РЭП. Расшифровывается это так: разведочно-эксплуатационное предприятие. Оно размещается в основном на кораблях. За Полярным кругом, в море Лаптевых, в районе Ванькиной губы РЭП добывает с морского дна оловоносный песок. Здесь же, на борту одного из судов, работает обогатительная фабрика.
Мировое производство
По американским данным, мировое производство олова в 1975 г. составляло 174…180 тыс. т.
• Сурьма
• Оглавление
Дата публикации:
4 августа 2003 года
n-t.ru
Что такое олово и для чего оно нужно?
Мягкий белый металл – олово – был одним из первых металлов, которые научился обрабатывать человек. Ученые считают, что добывать олово стали гораздо раньше, чем было впервые найдено железо.
Некоторые археологические находки подтверждают, что оловянные шахты на территории нынешнего Ирака работали уже четыре тысячи лет назад. Оловом торговали: купцы выменивали его на золото и драгоценные камни. В природе олово содержится в оксидной оловянной руде касситерите – минерале, залежи которого встречаются в Юго-Восточной Азии, Южной Америке, Австралии, Китае.
Из истории
По данным историков и археологов, впервые обнаружили олово, вероятнее всего, случайно, в наносных отложениях касситерита. Древние горны с отработанным шлаком удалось найти на юго-западе Великобритании. Среди обнаруженных предметов эпохи Древнего Рима и Греции оловянные изделия встречаются очень редко, что подтверждает предположение, что металл этот был дорогим.
Об олове упоминается в произведениях арабской литературы VIII-IX веков, а также в средневековых произведениях, описывающих путешествия и великие открытия. В Богемии и Саксонии олово стали добывать в XII веке.
Интересно, что задолго до того, как люди стали добывать чистое олово, изобрели бронзу – сплав олова с медью. По некоторым данным, бронза была известна человеку уже в 2500 году до нашей эры.
Дело в том, что олово существует в составе руд вместе с медью, поэтому при плавке получали не чистую медь, а ее сплав с оловом, то есть бронзу. Олово как случайную примесь можно обнаружить в медной посуде египетских фараонов, изготовленной в 2000 году до нашей эры.
Химические свойства олова
Олово инертно по отношению к воде и кислороду при комнатной температуре. Металл также имеет свойство покрываться тонкой оксидной пленкой на открытом воздухе. Именно химическая инертность олова в обычных условиях послужила популярности металла у изготовителей жестяной тары.
Серная и соляная кислота в разбавленном состоянии воздействуют на олово крайне медленно, а в концентрированном виде при нагревании растворяют его. При соединении с соляной кислотой получают хлорид олова, при реакции с серной – сульфат олова.
При вступлении в реакцию с разбавленной азотной кислотой получают нитрат олова, с концентрированной азотной кислотой – нерастворимую оловянную кислоту. Соединения олова имеют важное промышленное значение: их используют при производстве гальванических покрытий.
Применение олова
Этот серебристо-белый мягкий металл можно раскатать до состояния тонкой фольги. Олово не ржавеет, поэтому его широко используют в разных сферах. Чаще всего из этого металла изготавливают тару. Если олово нанести тонким слоем на другой металл, оно придаст поверхности особый блеск и гладкость.
Это свойство олова используют при изготовлении консервных банок. Олово часто используют в качестве антикоррозионного покрытия. Более третьей части всего олова, которое сегодня добывают в мире, используется при производстве пищевых емкостей для продуктов и напитков. Жестяные банки, хорошо всем знакомые, сделаны из стали, покрытой слоем олова толщиной не более 0,4 мкм.
Еще треть добываемого олова идет на изготовление припоев – сплавов со свинцом в разных пропорциях. Припои используются в электротехнике, для пайки трубопроводов. Такие сплавы могут содержать до 97% олова, медь и сурьму, увеличивающие твердость и прочность сплава.
Из олова, смешанного с сурьмой, делают посуду (в первую очередь фраже). В промышленности олово используют в различных химических соединениях.
www.vseznaika.org
ОЛОВО — это… Что такое ОЛОВО?
олово — олово, а … Русский орфографический словарь
ОЛОВО — (символ Sn), переходный элемент IV группы периодической таблицы, известный с древнейших времен. Основная руда КАССИТЕРИТ. Мягкое, пластичное, устойчивое к коррозии, олово используется в качестве защитного покрытия для железа, стали, меди и других … Научно-технический энциклопедический словарь
ОЛОВО — (лат. Stannum) Sn, химический элемент IV группы периодической системы, атомный номер 50, атомная масса 118,710. Серебристо белый металл, мягкий и пластичный; tпл 231,91 .С. Полиморфно; т. н. белое олово (или ? Sn) с плотностью 7,228 г/см³… … Большой Энциклопедический словарь
ОЛОВО — ср. крушец (металл) пепельно серебристый, белее свинца, весьма мягкий, легкоплавкий, легкий весом, более прочих удобный для паянья и для отливки простых мелких вешиц; | ·стар. свинец, откуда пословица: Слово олово, веско. Лить олово, святочное… … Толковый словарь Даля
ОЛОВО — хим. элемент, символ Sn (лат. Stannum), ат. и. 50, ат. м. 118,71; серебристо белый металл, мягкий и пластичный; существует в двух аллотропных модификациях белое олово ß Sn (плотность 7228 кг/м3), которое при температуре ниже +13,2°С переходит в… … Большая политехническая энциклопедия
ОЛОВО — (Stannum), Sn, химический элемент IV группы периодической системы, атомный номер 50, атомная масса 118,710; металл, tпл 231,9 шC. Олово компонент бронзы, латуни, баббита и других сплавов, материал защитных покрытий на металлах, из него… … Современная энциклопедия
олово — касситерит, пинкзальц Словарь русских синонимов. олово сущ., кол во синонимов: 6 • касситерит (3) • … Словарь синонимов
Олово — Олово, металл, добавляемый в медь для получения бронзы (Чис 31:22; Иез 22:18,20). Финикийцы ввозили О. через см. Фарсис, предположит. при этом подразумевается О., к рое доставлялось на Ближний Восток с Британских островов через финик. форпосты в… … Библейская энциклопедия Брокгауза
Олово — Sn (лат. Stannum * a. tin; н. Zinn; ф. etain; и. estaсo), хим. элемент IV группы периодич. системы Менделеева, ат.н. 50, ат. м. 118, 69. B природе встречаются 10 стабильных изотопов 112Sn (0,96%), 114Sn (0,66%), 115Sn (0,35%), 116Sn… … Геологическая энциклопедия
ОЛОВО — ОЛОВО, олова, мн. нет, ср. Мягкий, ковкий серебристо белый металл. Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова
ОЛОВО — ОЛОВО, а, ср. Химический элемент, мягкий ковкий серебристо белый металл. | прил. оловянный, ая, ое. О. солдатик (игрушечная фигурка солдата). Толковый словарь Ожегова. С.И. Ожегов, Н.Ю. Шведова. 1949 1992 … Толковый словарь Ожегова
dic.academic.ru
1.Химический элемент олово(Sn).
1.1. Электронная формула данного химического элемента:
1S22S22P63S23P63D104S24P64D104F05S25P2
Сокращенная электронная формула:4D105S25P2
В 5-м периоде электроны заполняют сначала 5S-подуровень, потом 4D-подуровень, затем 5P-подуровень. Начиная с 3-го периода, происходит несоответствие между количеством электронов на энергетическом уровне и количеством электронов в данном периоде, что можно объяснить принципом наименьшей энергии. В соответствии с данным принципом, при заполнении энергетических уровней наблюдается эффект запаздывания. Электроны в таком состоянии заполняют орбитали в порядке повышения уровня энергии орбиталей. В соответствии с правилом Клечковского увеличение энергии и соответственно заполнение орбиталей происходит в порядке возрастания суммы квантовых чисел (n+l), а при равной сумме (n+l) в порядке возрастания числа n.
4D(4+2)=6 5S(5+0)=5 5P(5+1)=6
4D- и 5P-подуровни имеют одинаковые значения (n+l), но энергетически более выгоден 4D-подуровень, т. к. у него меньшее значение n. Поэтому данные подуровни заполняются в следующем порядке: 5S, 4D, 5P. 5-й период заполняется аналогично 4-му.
1.2. I. Sn – олово. Порядковый номер 50, 5 период, IV группа, главная (А) подгруппа.
Порядковый номер олова – 50, а относительная атомная масса Аr=119 (округленное значение). Соответственно, заряд ядра его атома +50 (число протонов). Следовательно, число нейтронов в ядре равно N=Аr-Z=69. Так как атом электронейтрален, то число электронов, содержащихся в атоме олова, тоже равно 50.
Элемент олово находится в 5 периоде периодической таблицы Д. И. Менделеева, значит, все электроны атома располагаются на пяти энергетических уровнях. Так же по номеру периода устанавливается количество электронов, которые находятся в данном периоде. Их количество равно: Xe=2n2=2*52=50.
Номер группы (IV) показывает на то, что максимальная степень окисления металла равна +4.
Олово относится к IV группе главной (А) подгруппе, следовательно, олово – P-элемент.
I
5S 4D
I. Возможность “эффекта провала электронов”:50Sn
Так как 4D-подуровень заполнен электронами полностью, то “эффект провала электронов” не наблюдается.
1.3. Валентные подуровни в электронной формуле данного химического элемента – 5S и 5P: 5S25P2. Олово относится к P-элементам, т. к. у этого элемента в последнюю очередь заполняется пятый электронный слой, 5P-подуровень.
1.4. Наборы квантовых чисел для всех валентных электронов:
S
-1 0 1
1:n=5, l=0, ml=0, ms=+1/2;S2:n=5, l=0, ml=0, ms=-1/2;
P1:n=5, l=1, ml=-1, ms=+1/2; +50Sn
P2:n=5, l=1,ml=0,ms=+1/2.
1.5. Олово – металл, т.к. его атомы отдают электроны, превращаясь в положительные ионы. Т. к. олово расположено вблизи диагонали бор – астат, он обладает двойственными свойствами: в одних соединениях ведет себя как металл, в других – как неметалл (амфотерные оксиды и гидроксиды).
Так как атомы олово содержат на внешнем слое 4 электрона, они могут отдавать их, приобретая при этом степень окисления +4 (проявлять восстановительные свойства). Также олово может принимать степень окисления +2.
5S 5P 5S 5P
с.о.=+2 с.о.=+4
1
1)
2)
.6.В соответствии с правилом Гунда суммарное спиновое число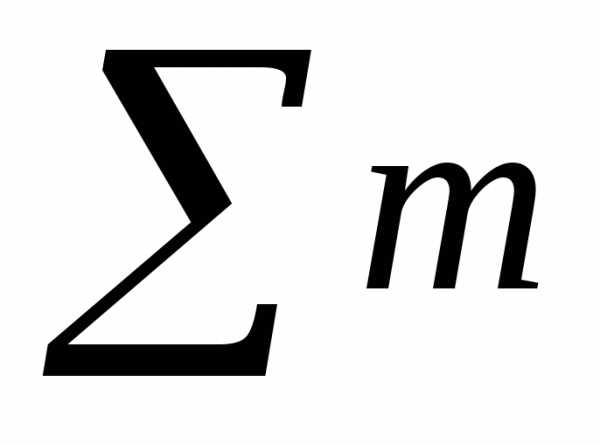 s должно быть максимальным. Расположим
2 электрона на P-атомной
орбитали
s должно быть максимальным. Расположим
2 электрона на P-атомной
орбитали
|
Так как во втором
варианте 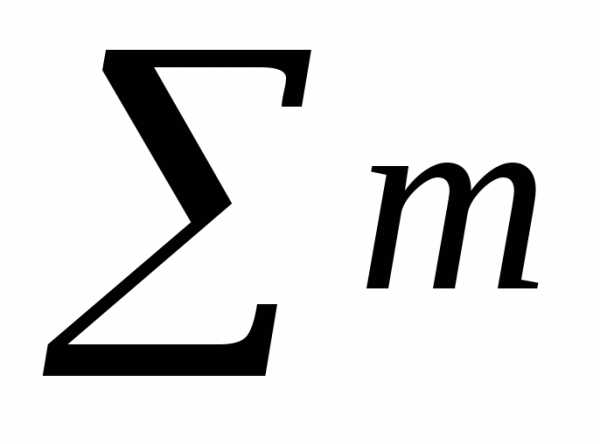 s=max,
то два электрона располагаются наP-атомной орбитали в таком
положении, как во втором варианте.
s=max,
то два электрона располагаются наP-атомной орбитали в таком
положении, как во втором варианте.
Согласно принципу наименьшей энергии электроны в основном состоянии заполняют орбитали в порядке повышения уровня энергии орбиталей. В одном и том же уровне энергия подуровней возрастает:Es<Ep. Поэтому сначала заполняется 5S-подуровень(2 электрона), а после этого заполняется 5P-подуровень по одному электрону в каждой ячейке.
1.7.
5S 5P 5S 5P
K=2K*=4SP3 q4-гиб.-я
q4-гиб.-я
Атом олова в возбужденном состоянии имеет ковалентность, равную 4.
С водородом олово
образует гидрид SnH4;с
галогенами соединения типаSnX2иSnX4. Соединения
типаSnX2обусловлены
наличием у олова неподеленной пары
электронов. Соединения типаSnX4иSnH4имеютSP3 q4-гибридизацию
и имеют форму тетраэдра.
q4-гибридизацию
и имеют форму тетраэдра.
studfiles.net