Silicium — это… Что такое Silicium?
| Кремний/Silicium (Si) | |
|---|---|
| Атомный номер | 14 |
| Внешний вид простого вещества | В аморфной форме — коричневый порошок, в кристаллической — тёмно-серый, слегка блестящий |
| Свойства атома | |
| Атомная масса (молярная масса) | 28,0855 а. е. м. (г/моль) |
| Радиус атома | 132 пм |
| Энергия ионизации (первый электрон) | 786,0(8,15) кДж/моль (эВ) |
| Электронная конфигурация | [Ne] 3s2 3p2 |
| Химические свойства | |
| Ковалентный радиус | 111 пм |
| Радиус иона | 42 (+4e) 271 (-4e) пм |
| Электроотрицательность (по Полингу) | 1,90 |
| Электродный потенциал | 0 |
| Степени окисления | +4, −4, +2 |
| Термодинамические свойства простого вещества | |
| Плотность | 2,33 г/см³ |
| Удельная теплоёмкость | 19,8 Дж/(K·моль) |
| Теплопроводность | 149 Вт/(м·K) |
| Температура плавления | 1688 K |
| Теплота плавления | 50,6 кДж/моль |
| Температура кипения | 2623 K |
| Теплота испарения | 383 кДж/моль |
| Молярный объём | 12,1 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | алмаз |
| Период решётки | 5,430 Å |
| Отношение c/a | n/a |
| Температура Дебая | 625,00 K |
| Si | 14 |
| 28,0855 | |
| 3s²3p² | |
| Кремний | |
История
Схема атома кремния
В чистом виде кре́мний был выделен в 1811 году французскими учеными Жозефом Луи Гей-Люссаком и Луи Жаком Тенаром.
Происхождение названия
В 1825 году шведский химик Йёнс Якоб Берцелиус действием металлического калия на фтористый кремний SiF4 получил чистый элементарный кремний. Новому элементу было дано название «силиций» (от лат. silex — кремень). Русское название «кремний» введено в 1834 году российский химиком Германом Ивановичем Гессом. В переводе c греческого kremnos — «утес, гора».
Нахождение в природе
По распространённости в земной коре кремний среди всех элементов занимает второе место (после кислорода). Масса земной коры на 27,6—29,5 % состоит из кремния. Кремний входит в состав нескольких сотен различных природных силикатов и алюмосиликатов. Больше всего распространен кремнезём — многочисленные формы диоксида кремния (IV) SiO
Получение
В промышленности кремний получают, восстанавливая расплав SiO2коксом при температуре около 1800 °C в дуговых печах. Чистота полученного таким образом кремния составляет около 99,9 %. Так как для практического использования нужен кремний более высокой чистоты, полученный кремний хлорируют. Образуются соединения состава SiCl4 и SiCl3H. Эти хлориды далее очищают различными способами от примесей и на заключительном этапе восстанавливают чистым водородом. Возможна также очистка кремния за счет предварительного получения силицида магния Mg
Способ получения кремния в чистом виде разработан Николаем Николаевичем Бекетовым. Крупнейшим производителем кремния в России является ОК Русал[1] — кремний производится на заводах в г. Каменск-Уральский (Свердловская область) и г. Шелехов (Иркутская область).
Физические свойства
Кристаллическая структура кремния.
Кристаллическая решетка кремния кубическая гранецентрированная типа алмаза, параметр а = 0,54307 нм (при высоких давлениях получены и другие полиморфные модификации кремния), но из-за большей длины связи между атомами Si—Si по сравнению с длиной связи С—С твердость кремния значительно меньше, чем алмаза. Кремний хрупок, только при нагревании выше 800 °C он становится пластичным веществом. Интересно, что кремний прозрачен к инфракрасному излучению, начиная с длины волны 1.1 микрометр.
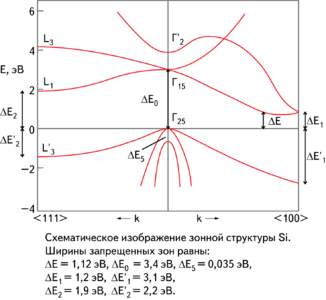 Схематическое изображение зонной структуры кремния [1]
Схематическое изображение зонной структуры кремния [1]Электрофизические свойства
Элементарный кремний — типичный непрямозонный полупроводник. Ширина запрещенной зоны при комнатной температуре 1,12 эВ, а при Т = 0 К составляет 1,21 эВ [2]. Концентрация носителей заряда в кремнии с собственной проводимостью при комнатной температуре 1,5·1016м-3. На электрофизические свойства кристаллического кремния большое влияние оказывают содержащиеся в нем микропримеси. Для получения монокристаллов кремния с дырочной проводимостью в кремний вводят добавки элементов III-й группы — бора, алюминия, галлия и индия, с электронной проводимостью — добавки элементов V-й группы — фосфора, мышьяка или сурьмы. Электрические свойства кремния можно варьировать, изменяя условия обработки монокристаллов, в частности, обрабатывая поверхность кремния различными химическими агентами.
Подвижность электронов 1400 см²/(в*c).
Химические свойства
В соединениях кремний склонен проявлять степень окисления +4 или −4, так как для атома кремния более характерно состояние sp³-гибридизации орбиталей. Поэтому во всех соединениях, кроме оксида кремния (II) SiO, кремний четырёхвалентен.
Химически кремний малоактивен. При комнатной температуре реагирует только с газообразным фтором, при этом образуется летучий тетрафторид кремния SiF4. При нагревании до температуры 400—500°C кремний реагирует с кислородом с образованием диоксида SiO2, с хлором, бромом и иодом — с образованием соответствующих легко летучих тетрагалогенидов SiHal4.
С водородом кремний непосредственно не реагирует, соединения кремния с водородом — силаны с общей формулой SinH2n+2 — получают косвенным путем. Моносилан SiH4 (его часто называют просто силаном) выделяется при взаимодействии силицидов металлов с растворами кислот, например:
Ca2Si + 4HCl → 2CaCl2 + SiH4↑.
Образующийся в этой реакции силан SiH4 содержит примесь и других силанов, в частности, дисилана Si2H6 и трисилана Si3H8, в которых имеется цепочка из атомов кремния, связанных между собой одинарными связями (—Si—Si—Si—).
С азотом кремний при температуре около 1000 °C образует нитрид Si3N4, с бором — термически и химически стойкие бориды SiB3, SiB6 и SiB12. Соединение кремния и его ближайшего аналога по таблице Менделеева — углерода — карбид кремния SiC (карборунд) характеризуется высокой твердостью и низкой химической активностью. Карборунд широко используется как абразивный материал.
При нагревании кремния с металлами возникают силициды. Силициды можно подразделить на две группы: ионно-ковалентные (силициды щелочных, щелочноземельных металлов и магния типа Ca2Si, Mg2Si и др.) и металлоподобные (силициды переходных металлов). Силициды активных металлов разлагаются под действием кислот, силициды переходных металлов химически стойки и под действием кислот не разлагаются. Металлоподобные силициды имеют высокие температуры плавления (до 2000 °C). Наиболее часто образуются металлоподобные силициды составов MeSi, Me3Si2, Me2Si3, Me5Si3 и MeSi2. Металлоподобные силициды химически инертны, устойчивы к действию кислорода даже при высоких температурах.
При восстановлении SiO2 кремнием при высоких температурах образуется оксид кремния (II) SiO.
Для кремния характерно образование кремнийорганических соединений, в которых атомы кремния соединены в длинные цепочки за счет мостиковых атомов кислорода —О—, а к каждому атому кремния, кроме двух атомов О, присоединены еще два органических радикала R1 и R2 = CH3, C2H5, C6H5, CH2CH2CF3 и др.
Применение

В настоящее время кремний — основной материал для электроники и солнечной энергетики.
Монокристаллический кремний — материал для зеркал газовых лазеров.
Иногда кремний (технической чистоты) и его сплав с железом (ферросилиций) используется для производства водорода в полевых условиях.
Соединения металлов с кремнием — силициды, являются широкоупотребляемыми в промышленности (например электронной и атомной) материалами с широким спектром полезных химических, электрических и ядерных свойств (устойчивость к окислению, нейтронам и др.), а также силициды ряда элементов являются важными термоэлектрическими материалами.
Кремний применяется в металлургии при выплавке чугуна, сталей, бронз, силумина и др. (как раскислитель и модификатор, а также как легирующий компонент).
Соединения кремния служат основой для производства стекла и цемента. Производством стекла и цемента занимается силикатная промышленность. Она также выпускает силикатную керамику — кирпич, фарфор, фаянс и изделия из них.
Широко известен силикатный клей, преимущественно применяемый для склеивания бумаги.
Последнее время очень широко применяются полимеры на основе кремния — силиконы.
Биологическая роль
Для некоторых организмов кремний является важным биогеным элементом. Он входит в состав опорных образований у растений и скелетных — у животных. В больших количествах кремний концентрируют морские организмы — диатомовые водоросли, радиолярии, губки. Большие количества кремния концентрируют хвощи и злаки, в первую очередь — подсемейства Бамбуков и Рисовидных, в том числе — рис посевной. Мышечная ткань человека содержит (1-2)·10-2% кремния, костная ткань — 17·10-4%, кровь — 3,9 мг/л. С пищей в организм человека ежедневно поступает до 1 г кремния.
Соединения кремния относительно нетоксичны. Но очень опасно вдыхание высокодисперсных частиц как силикатов, так и диоксида кремния, образующихся, например, при взрывных работах, при долблении пород в шахтах, при работе пескоструйных аппаратов и т. д. Микрочастицы SiO2, попавшие в лёгкие, кристаллизуются в них, а возникающие кристаллики разрушают лёгочную ткань и вызывают тяжёлую болезнь — силикоз. Чтобы не допустить попадания в лёгкие опасной пыли, следует использовать для защиты органов дыхания респиратор.
См. также
Ссылки
Литература
- Самсонов. Г. В. Силициды и их использование в технике. Киев, Изд-во АН УССР, 1959. 204 стр. с илл.
- Алёшин Е. П., Алёшин Н. Е. Рис. Москва, 1993. 504 стр. 100 рис.
Примечания
- ↑ Р Смит., Полупроводники: Пер. с англ. — М.: Мир, 1982. — 560 с, ил.
- ↑ Зи С., Физика полупроводниковых приборов: В 2-х книгах. Кн. 1. Пер. с англ. — М.: Мир, 1984. — 456 с, ил.
Wikimedia Foundation. 2010.
- Silly Really
- Silly really
Смотреть что такое «Silicium» в других словарях:
Silicium — Aluminium ← Silicium → Phosphore C … Wikipédia en Français
SILICIUM — Le silicium (symbole Si, numéro atomique 14) ne se trouve pas à l’état natif, mais constitue, sous forme de silice et de silicates, l’élément le plus abondant (environ 28 p. 100), après l’oxygène, à la surface du globe (cf. SILICATES, SILICE).… … Encyclopédie Universelle
Silicium [1] — Silicium, Atomgew. 28,4, wie Kohlenstoff vierwertig, kommt in der Natur nicht in freiem Zustande vor, dagegen weit verbreitet als Kieselsäure (SiO2), besonders in den Silikaten (s.d.). Man unterscheidet amorphes und kristallisiertes Silicium.… … Lexikon der gesamten Technik
Silicium — Si*lic i*um, n. See {Silicon}. [1913 Webster] … The Collaborative International Dictionary of English
Silicĭum — Silicĭum, so v.w. Kiesel 2). Siliciumfluorid, so v.w. Kieselfluorid, s.u. Kiesel 2) E), vgl. Kieselfluormetalle. Siliciumoxyd, so v.w. Kieseloxyd, s.u. Kiesel 2) A) a). Silieniumwasserstoff, so v.w. Kieselwasserstoff, s.u. Kiesel 2) B) … Pierer’s Universal-Lexikon
Silicĭum — (lat.), Kiesel … Meyers Großes Konversations-Lexikon
Silicium [2] — Silicium, Si, Atomgew. 28,3, spez. Gew. des kristallisierten 2,34, des amorphen braunen 2,35, des graphitartigen 2,00. Man gewinnt es neuestens aus Quarzsand und Kohle im elektrischen Ofen als Nebenerzeugnis der Herstellung von Siliciumkarbid… … Lexikon der gesamten Technik
Silicium — Silicium, lat., s. Kieselerde; Silicat, kieselsaures Salz … Herders Conversations-Lexikon
silicium — [sə lish′ē əm, səlis′ē əm] n. [ModL: so named (1808) by DAVY Sir Humphry < L silex, flint (see SILEX) + IUM] former name for SILICON … English World dictionary
Silicium — Eigenschaften … Deutsch Wikipedia
Silicium — Si|li|ci|um 〈n.; s; unz.; chem. ; fachsprachl.〉 = Silizium [zu lat. silex „Kieselstein“] * * * Si|li|ci|um [↑ Silic u. ↑ ium (1)], das; s; Symbol: Si; S: Silizium: chem. Element aus Gruppe 14 des Periodensystems ( … Universal-Lexikon
dic.academic.ru
Кремний (Silicium)
Кремний (Silicium)
|
Свойство |
Кремний |
|
Атомный номер |
14 |
|
Атомная масса |
28,0855 |
|
Группа |
IV |
|
Период |
3 |
|
Электронное строение |
3s2 3p2 |
|
Электроотрицательность |
1,9 |
|
Плотность при 20°С, г/cм3 |
2,33 |
|
Температура плавления, °С |
1410 |
|
Температура кипения, °С |
3265 |
|
Характерные степени окисления |
-4 +4 |
|
Цвет элемента |
Темно-серы |
Кремний — Si, химический элемент IV группы периодической системы Менделеева; атомный номер 14, атомная масса 28,086. В природе элемент представлен тремя стабильными изотопами: 28Si (92,27%), 29Si (4,68%) и 30Si (3,05%).
Историческая справка.
Соединения кремния, широко распространённые на земле, были известны человеку с каменного века. Использование каменных орудий для труда и охоты продолжалось несколько тысячелетий. Применение соединений кремния, связанное с их переработкой, — изготовление стекла — началось около 3000 лет до н. э. в Древнем Египте. Раньше других стало известно соединение кремния — двуокись SiO2 (кремнезём). В 18 в. кремнезём считали простым телом и относили к «землям», что отражено в его названии. В свободном состоянии кремний был получен французскими учеными Гей-Люссаком и Тенаром в 1811 г., однако истинную природу кремния установил спустя 14 лет шведский химик Я. Берцелиус.
Сложность состава кремнезёма установил И. Я. Берцелиус и он же впервые, в 1825, получил элементарный кремний из фтористого кремния SiF4, восстанавливая последний металлическим калием. Новому элементу было дано название «силиций» (от лат. silex — кремень). Русское название ввёл Г. И. Гесс в 1834. Оригинальным путем (реакцией цинка с хлористым соединением кремния) свободный кремний был получен в 1865 г. русским ученым Н. Н. Бекетовым, сейчас это один из способов получения высокочистого полупроводникового кремния.
Чистая и прозрачная разновидность кварца, называемая горным хрусталем, была известна уже древним грекам. Они считали горный хрусталь льдом, так сильно замерзшим, что он навсегда утратил способность таять. Греки называли горный хрусталь кристаллом — «кристаллос», что значило лед. Впоследствии это слово вошло в минералогию и, получив широкое распространение, стало употребляться для обозначения твердых тел, имеющих форму правильных многогранников.
Кроме горного хрусталя, кристаллы которого достигают иной раз огромной величины (нескольких метров), кварц встречается в природе в виде окрашенных соединений. Среди них чистые и прозрачные разновидности, окрашенные в фиолетовый (аметисты) и в лимонно-желтый цвет (цитрины) относятся к числу драгоценных и полудрагоценных самоцветов. Общее число разновидностей кварца достигает двухсот, количество природных соединений, содержащих кварц, измеряется многими сотнями.
Сейчас невозможно точно сказать, кто и когда изобрел стекло, так же как невозможно сказать, кто и когда впервые обжег горшок из глины. Известно лишь, что стекло является одним из древнейших изобретений человечества. Так, ожерелье, найденное на шее мумии египетской царицы Хатшепсут, состоящее из зеленовато-черных стеклянных бусин, насчитывает 3400 лет. Еще старше возраст стеклянной бусины из могилы города Фив, насчитывающей 5500 лет.
Высокого совершенства в стеклоделии достигли мастера древнего Рима. О большом искусстве получения цветных стекол свидетельствует мозаичный пол с изображением цепной собаки, обнаруженная в одном из домов при раскопках Помпеи, а также мозаика в вилле римского императора Адриана, известная в искусстве под названием «Неподметенный пол». Римские стеклоделы были большими мастерами производства различных изделий из стекла. Они делали кувшины для воды, масла и вина; чаши и кубки, вазы и многое другое. Некоторые из таких предметов дошли до наших дней; они бережно хранятся в музеях крупнейших городов Западной Европы. Среди образцов подлинного искусства особого упоминания заслуживает ваза Аюджио из дома богача Мелегера в Помпее. Это красивейший сосуд из темно-синего стекла, украшенный венком из винограда и плюща, сделанным из мелочно-белого стекла. Подобным шедевром является и ваза, найденная в гробнице римского императора Александра Севера, из темно-голубого стекла, украшенная резными рисунками, изображающими греческий миф о Язоне и волшебнице Медее.
Изучение состава древнерусских стекол домонгольского времени показывает замечательную самобытность русских мастеров, сумевших создать совершенно оригинальную рецептуру. Наиболее типичными для древнерусского стеклоделия являются свинцово-кремнеземные и калиево-свинцово-кремнеземные стекла. Из них древнерусские умельцы изготовляли бусы, браслеты, мозаику, посуду, оконные стекла. Свинцово-кремнеземные стекла были обнаружены также в Польше. В других странах стекла такого состава еще не найдены.
Одно из самых древних изобретений — стекло — приобрело в жизни человека огромное значение — в повседневности нашего быта, в промышленности, в технике, в науке, в произведениях искусств. Оконное, бутылочное, ламповое, зеркальное стекло; стекло домашней, хозяйственной, лабораторной посуды и аппаратов; стекло оптическое — от стекол очков до сложных анастигматов фотокамер; линзы бесчисленных оптических приборов — от микроскопов, открывающих огромный, но для простого глаза невидимый мир, до телескопов, уносящих нас в бесконечные просторы мироздания. Трудно перечислить все области применения стекла и невозможно сосчитать различные предметы, сделанные из него. Успехи химии в области изучения стекла сделали его материалом, из которого изготовляются несгораемые ткани, театральные занавеси, декорации, ковры, изоляционные ленты, вата, войлок и многие другие предметы техники и быта. Ценные свойства кварца (пропускает ультрафиолетовые лучи, малый коэффициент расширения, химическая инертность, тугоплавкость и др.) обеспечили ему широкое применение в различных областях науки и техники.
Тончайшие, исключительно прочные, нити, получаемые из кварца, расплавленного в пламени гремучего газа, применяются в точных электроизмерительных приборах и инструментах для подвешивания деталей (стрелок, указателей, рычагов и т. д.). Из тугоплавкого кварцевого стекла изготовляют термометры для измерения высоких температур. Малый коэффициент расширения позволяет употреблять кварц для изготовления сосудов, трубок, лабораторной посуды и разнообразной химической аппаратуры, применяемой в условиях резких колебаний температуры. Оптические свойства кварца обеспечивают его применение в производстве всевозможных оптических приборов, в изготовлении ламп «горного солнца», в устройстве закрытых соляриев и т. д.
Есть еще много других минералов, содержащих соединения кремния, которые также находят разнообразное применение в технике. Одни из них за прочность и красивый вид (гранит, порфир, лабрадор и др.) используются как строительный и отделочный материалы; другие, обладая исключительной твердостью, применяются в качестве так называемых точных камней в разнообразных измерительных приборах, от часовых механизмов до аналитических весов и аппаратов специального назначения; третьи — цементы, обладая способностью в смеси с другими веществами связывать воедино щебень, камни, кирпичи, широко применяются в строительстве; четвертые — за безукоризненную прозрачность, чистоту и блеск ценятся как самоцветы и, наконец, пятые, обладающие пестрой, яркой, необычной окраской (яшмы, нефрит, халцедоны), употребляются в художественных изделиях, которые украшают дворцы и музеи.
Важнейшее соединение кремния — кремнезем — необходим для жизни растений и животных. В растениях кремнезем накапливается в стеблях, что значительно повышает их механическую прочность. Кремнезем входит в состав не только крупных растений, но и мельчайших из них — диатомовых водорослей. Кремний нужен и животным. Птицы без кремнезема не создают прочной скорлупы яиц. Некоторые виды губок строят опорные образования своего тела также из кремнезема. Кремнезем есть и в организме человека. Больше всего содержится кремнезема в стекловидном теле глаза, где количество его достигает до 0,06% по весу. Однако биологическая роль кремнезема в человеческом организме до сих пор еще не изучена.
По распространённости в земной коре кремний — второй, после кислорода, элемент, его среднее содержание в литосфере 29,5% по массе. В земной коре кремний играет такую же первостепенную роль, как углерод в животном и растительном мире. Для геохимии кремния важна исключительно прочная связь его с кислородом. Около 12% литосферы составляет кремнезём SiO2 в форме минерала Кварца и его разновидностей, 75% литосферы слагают различные Силикаты и Алюмосиликаты (полевые шпаты, слюды, амфиболы и т. д.). Общее число минералов, содержащих кремнезём, превышает 400.
Использовалась информация из открытых Web источников.
Использовались материалы с сайта «Большая Советская Энциклопедия (БСЭ)»,
а также XuMuK.ru — сайт о химии.
si-c.ru
свойства, применение, получение, взаимодействия, характеристика
КРЕМНИЙ, Si (лат. Silicium * а. silicium, siliсоn; н. Silizium; ф. silicium; и. siliseo), — химический элемент IV группы периодической системы Менделеева, атомный номер 14, атомная масса 28,086. В природе встречаются 3 стабильных изотопа 28Si (92,27), 29Si (4,68%), 30Si (3,05%).
Физические свойства кремния
Соединения кремния известны человеку с древнейших времён как материал для изготовления орудий труда и охоты. Сведения о переработке его соединений (в Древнем Египте получали стекло) датируются около 3000 лет до н.э. Кремний впервые выделен в 1811 французскими учёными Ж. Л. Гей-Люссаком и Л. Ж. Тенаром, но идентифицирован лишь в 1823 шведским учёным Й. Я. Берцелиусом.
Кремний образует тёмно-серые со смолистым блеском хрупкие кристаллы, решётка гранецентрированная кубическая типа алмаза (а=0,5431 нм). Плотность 2328 кг/м3, t плавления 1415°С, t кипения около 3250°С. Удельная теплоёмкость (при 25°С) 19,79 Дж/(моль•К), коэффициент теплопроводности 84-126 Вт/(м•К), удельное электрическое сопротивление 2,3•103 Ом•м, температурный коэффициент электрического сопротивления 1,7•10-3 К-1 (273 К), температурный коэффициент линейного расширения 3,72•10-3 К-1 в интервале 291-1273 К. Твёрдость по Бринеллю 2,4 ГПа, по Moocy 7. Модуль упругости 109 ГПа.
Кремний — полупроводник, электрические свойства которого сильно зависят от примесей. Ширина запрещённой зоны 1,12 эВ при 0 К. Прозрачен для инфракрасных лучей (отражательная способность 0,3, показатель преломления 3,42).
Химические свойства кремния
В большинстве соединений кремний проявляет степени окисления -4, +2, +4. При низких температурах химически инертен. На воздухе покрывается тонкой плёнкой оксида, в атмосфере кислорода окисляется при нагревании свыше 400°С. С фтором взаимодействует в обычных условиях, с остальными галогенами, азотом, углеродом — при нагревании. В воде, кислотах (за исключением смеси HF+HNO3) не растворяется. Щёлочи переводят кремний в соли кремниевых кислот с выделением водорода. Растворим во многих расплавленных металлах, с некоторыми из них даёт соединения, называемые силицидами. С водородом образует весьма реакционноспособные соединения общей формулы SinH2n+2 (где n=1-8) — силаны. Известны многочисленные кремнийорганические соединения (силиконы, органосилоксаны и т.д.). Большое значение имеют кремниевые кислоты. В свободном состоянии выделены мета-(Н2SiO3), орто-(Н2SiO4) и двуметакремниевая (Н2Si2О5) кислоты. Соли кремниевых кислот широко распространены в природе: минералы класса силикатов природных. При изоморфном замещении в их структуре части кремния алюминием образуются алюмосиликаты.
Нахождение в природе
Кремний — второй элемент после кислорода по своей распространённости в земной коре, его кларк 29,5% (по массе). Известно свыше 400 минералов, содержащих кремний. Около 12% литосферы слагает кварц SiO2 и его скрытокристаллические разновидности (халцедон, опал и т.д.), а 75% составляют различные силикаты и алюмосиликаты (полевые шпаты, слюды, амфиболы и т.д.). В магматических процессах в результате кристаллизационной дифференциации происходит обогащение поздних порций расплава кремнезёмом. При повышенных температурах кремнезём растворяется в водяных парах и может мигрировать, поэтому для гидротермальных образований характерны большие концентрации кварца. При выветривании на месте магматогенных минералов класса силикатов и алюмосиликатов развиваются глинистые минералы и оксиды. Среднее содержания кремния (в массовых %): в каменных метеоритах 18, ультраосновных породах 19, основных 24, средних 26, кислых 32,3, глинах 7,3, песчаниках 36,8, карбонатных горных породах 2,4; в воде океанов 3-10%. В живом веществе кремний играет важную роль, участвуя в образовании твёрдых скелетных частей. Особенно много его накапливается в морских растениях (например, диатомовые водоросли) и животных (кремнероговые губки, радиолярии и др.), которые, отмирая, формируют на дне океанов и морей мощные отложения кремнезёма.
Суточное потребление кремния человеком до 1 г. При высоком содержании диоксида кремния в воздухе он попадает в лёгкие человека и вызывает заболевание — силикоз.
Получение и использование
Получают технический кремний восстановлением SiO2 коксом; полупроводниковый кремний — восстановлением водородом SiCl4 или SiHCl3, разложением SiH4. Монокристаллы выращивают методом бестигельной зонной плавки и по методу Чохральского (вытягиванием из расплава).
Кремний — основной материал полупроводниковой электроники.
Кремний используют для изготовления интегральных схем, диодов, транзисторов, солнечных батарей, фотоприёмников и др., а также линз в приборах инфракрасной техники. Кремний применяется в качестве легирующей добавки в производстве сталей и сплавов цветных металлов.
www.mining-enc.ru
Популярная библиотека химических элементов. Раритетные издания. Наука и техника
Кремний
| 14 | |
Si |
4 8 2 |
| КРЕМНИЙ | |
| 28,086 | |
| 3s23p2 | |
Чем знаменит кремний? Во-первых, этот элемент – второй по распространенности на Земле после кислорода. Масса земной коры более чем на четверть – 27,6% – состоит из кремния.
Во-вторых, этот элемент – ближайший аналог углерода со всеми, как говорится, вытекающими отсюда последствиями.
Очевидно, с этих двух точек зрения и стоит рассматривать кремний – достаточно обыкновенный и достаточно необыкновенный элемент.
Природные соединения
«Показывают мне, – писал в одной из своих популярных книг академик А.Е. Ферсман, – самые разнообразные предметы: прозрачный шар, сверкающий на солнце чистотой холодной ключевой воды, красивый, пестрого рисунка агат, яркой игры многоцветный опал, чистый песок на берегу моря, тонкую, как шелковинка, нитку из плавленого кварца или жароупорную посуду из него, красиво ограненные груды горного хрусталя, таинственный рисунок фантастической яшмы, окаменелое дерево, превращенное в камень, грубо обработанный наконечник стрелы древнего человека… все это одно и то же химическое соединение элементов кремния и кислорода».
Как ни разнообразен этот перечень, он, конечно, не исчерпывает многообразия природных соединений кремния. Начнем, однако, с упомянутых. «Грубо обработанный наконечник стрелы древнего человека» был сработан из кремня. А что такое кремень? Современный человек видел эти наконечники, равно, как и кремневые ружья, разве только в историческом музее. «Кремни», вставляемые в зажигалки курильщиков, ни внешне, ни по составу нимало не похожи на те кремни. Впрочем, многие из нас в детстве высекали искры, ударяя камешком о камешек, и скорее всего, тогда в наших руках были настоящие кремни.
Так что такое кремень? Химик на этот вопрос ответит буквально по Ферсману: двуокись кремния, кремнезем. Возможно, при этом добавит, что кремнезем кремня – аморфный, в отличие от кристаллического кремнезема кварцевого песка и горного хрусталя, и что часть химиков считает кремень кристаллогидратом mSiO2 · nH2O.
Геолог на тот же вопрос ответит иначе, но тоже в общем-то буднично: минеральное образование, распространенное и мало интересное, пласты и «желваки» кремня обычно залегают среди известняков и меловых отложений…
И лишь гуманитарий-историк отзовется, должен отозваться, о кремне восторженно, ибо именно кремень – невзрачный и не очень прочный камень – помог в свое время человеку стать Человеком. Каменный век – век кремневых орудий труда. Причиной тому не только и не столько распространенность и доступность кремня, сколько способность его при сколе образовывать острые режущие кромки.
Обратимся теперь к кристаллическим аналогам кремня: «красиво ограненные груды горного хрусталя», «чистый песок на берегу моря»… Разница между ними небольшая, по существу лишь в размерах и примесях. Чистый песок – чистая кристаллическая двуокись кремния. Чистой воды горный хрусталь – то же самое. И что еще очень важно, оба эти вещества – полимеры, неорганические полимеры.
Одним из первых предположение о полимерном строении двуокиси кремния высказал Дмитрий Иванович Менделеев. Именно этим обстоятельством объяснял он нелетучесть и тугоплавкость веществ состава SiO2 или, правильнее, (SiO2)n. Рентгеноструктурные исследования наших дней подтвердили правильность этой догадки. Установлено, что кристаллический кремнезем представляет собой трехмерный сетчатый полимер. Цепочка кремнекислородных тетраэдров очень прочна, связь кремния с кислородом намного прочнее, чем, например, связь между атомами углерода в цепях органических полимеров. Кремнекислородным цепям хватает и гибкости, но в мире минералов они образуют жесткие сплетения в виде пространственных решеток и сеток, которые хрупки, неподатливы при механической обработке. Чтобы кремнекислородные цепочки остались гибкими, эластичными, их нужно изолировать одну от другой, окружить другими атомами или группами атомов. Это сделали химики, синтезировавшие многочисленные ныне кремнийорганические полимеры, речь о которых ниже. Впрочем, и природа дала великолепный образец волокнистого по структуре полимерного соединения кислорода и кремния – это асбест.
Сегодня очень непросто ответить на детский вопрос, какая из разновидностей кристаллической двуокиси кремния – песок или горный хрусталь – важнее для современного человека. Если брать в расчет только природный горный хрусталь, запасы которого практически исчерпаны, то ответ однозначен: конечно, песок. Из кварцевого песка делают кварцевое стекло, а из него – превосходную лабораторную посуду, баллоны ламп специального назначения и многое другое. Горный же хрусталь – не только поделочный материал, он и пьезоэлектрик. Он нужен радиотехнике в все возрастающих количествах, и вряд ли возможно было бы быстрое развитие этой отрасли, если бы люди не научились выращивать крупнокристаллический искусственный кварц в виде монокристаллов. В 30-х годах Александр Евгеньевич Ферсман писал: «Через несколько десятков лет геологи не будут больше с опасностью для жизни взбираться на вершины Альп, Урала или Кавказа в погоне за кристаллами, не будут добывать их в безводных пустынях Южной Бразилии или в наносах Мадагаскара. Я уверен, что мы будем по телефону заказывать нужные куски кварца на государственном кварцевом заводе». Кварцевые заводы появились даже раньше, чем предсказывал ученый. Они выпускают кристаллы кварца, ничем не уступающие природному горному хрусталю, в количествах, достаточных не только для радиоэлектронной промышленности, не только для оптики, но и для украшений. Сомневающимся в этом утверждении рекомендуем обратиться в ближайший от их дома ювелирный магазин.
Кремний – элементарный
Мы умышленно ограничили рассказ о природных соединениях кремния тремя веществами и одним, по существу, соединением. Обо всем в коротком очерке все равно не расскажешь, а соединения с кислородом – самые важные. Вернемся, однако, собственно к кремнию.
Несмотря на распространенность в природе, этот элемент открыли сравнительно поздно. В 1825 г. выдающийся шведский химик и минералог Йенс Якоб Берцелиус сумел в двух реакциях выделить не очень чистый аморфный кремний в виде коричневого порошка. Для этого он восстановил металлическим калием газообразное вещество, известное ныне как тетрафторид кремния SiF4, и кроме того, провел такую реакцию: K2SiF6 + 4К → 6KF + Si.
Новый элемент был назван силицием (от латинского silex – кремень). Русское название этого элемента появилось спустя девять лет, в 1834 г., и благополучно дожило, в отличие, скажем, от «буротвора», до наших дней.
Кремний, как и углерод, образует различные аллотропические модификации. Кристаллический кремний так же мало похож на аморфный, как алмаз на графит. Это твердое вещество серо-стального цвета с металлическим блеском и гранецентрированной кристаллической решеткой того же типа, что у алмаза. Впрочем, аморфный кремний, как выяснилось, тоже не аморфный, а мелкокристаллический.
Первый промышленный способ производства кремния, изобретенный во второй половине XIX в. известным русским химиком Н.Н. Бекетовым, основан на восстановлении четыреххлористого кремния SiCl4 парообразным цинком. Технически чистый кремний (95…98% Si) сейчас получают главным образом восстановлением кремнезема в электрической дуге между графитовыми электродами. Используется до сих пор изобретенный еще в прошлом веке способ восстановления кремнезема коксом в электрических печах. Этот способ также дает технический кремний, нужный металлургии как раскислитель, связывающий и удаляющий из металла кислород, и как легирующая добавка, повышающая прочность и коррозионную стойкость сталей и многих сплавов на основе цветных металлов. Впрочем, здесь важно, «не переборщить»: избыток кремния может привести к хрупкости.
Не отошел в прошлое и бекетовский способ получения кремния (в реакции между парами цинка и тетрахлоридом кремния – летучей бесцветной жидкостью с температурой кипения всего 57,6°C). Это один из способов получения высокочистого полупроводникового кремния, о котором определенно наслышаны читатели этой книги.
Полагают, что при абсолютном нуле идеально чистый и идеально правильный монокристаллический кремний должен быть идеальным электроизолятором. Но идеальная чистота так же недостижима, как и абсолютный нуль. В нашем случае это, что называется, к добру. Не идеальный, а просто высокочистый и сверхчистый кремний стал важнейшим полупроводниковым материалом. При температуре, отличной от абсолютного нуля, в нем возникает собственная проводимость, причем носителями электрического тока являются не только свободные электроны, но и так называемые дырки – места, покинутые электронами.
Вводя в сверхчистый кремний те или иные легирующие добавки (в микроколичествах; обычно это делается с помощью ионно-лучевых установок), в нем создают проводимость того или иного типа. Добавки элементов третьей группы менделеевской таблицы ведут к созданию дырочной проводимости, а пятой – электронной. Что значат для нас сегодня полупроводники, объяснять, вероятно, излишне. Расскажем лучше вкратце о способах получения полупроводникового кремния.
Один из этих способов упомянут выше. Заметим только, что реакцию высокочистых паров цинка с очень чистым четыреххлористым кремнием проводят при температуре 950°C в трубчатом реакторе, изготовленном из плавленого кварца. Элементарный кремний образуется в виде игольчатых кристаллов, которые потом измельчают и промывают соляной кислотой, разумеется тоже весьма чистой. Затем следует еще одна ступень очистки – зонная плавка, и лишь после нее поликристаллическую кремниевую массу превращают в монокристаллы.
Есть и другие реакции, в которых получают высокочистый полупроводниковый кремний. Это восстановление водородом трихлорсилана SiHCl или четыреххлористого кремния SiCl4 и термическое разложение моносилана, гидрида кремния SiH4 или тетраиодида SiJ4. В последнем случае разложение соединения происходит на разогретой до 1000°C танталовой ленте. Дополнительная очистка зонной плавкой следует после каждой из этих реакций.
В полупроводниковом кремнии содержание примесей крайне мало – 10–5…10–6% и даже меньше.
Кремнийорганика
Первое органическое соединение, содержащее кремний, было получено еще в 1845 г. в реакции этилового спирта с четыреххлористым кремнием: SiCl4 + 4С2Н5OН → Si(OC2Н5)4 + 4HCl. Но это не был первый синтез кремнийорганического соединения в том смысле, какой вкладывает в это понятие современная химическая номенклатура. Кремнийорганическими сейчас признают лишь те соединения, в которых есть связь углерод – кремний. Так что первое кремнийорганическое соединение – тетраэтил-силиций Si(C2H5)4 – было получено лишь в 1863 г.
Конечно, в то время никто не предполагал, что спустя 100 лет кремнийорганика разовьется в самостоятельную и важную ветвь химической науки, что кремнийорганические соединения, особенно полимерные, станут первостепенно важны для многих видов промышленности, для транспорта и строительства, даже для быта.
Опытная хозяйка перед стиркой смажет руки силиконовым кремом, который предохранит их не только от воды, но и от разъедающего действия соды или стирального порошка. Сдавая в чистку платье или костюм, мы охотно доплачиваем за несминаемую складку и за «пропитку», благодаря которой платье будет меньше грязниться. И в том и в другом случае нашу одежду на фабрике химической чистки обработают Кремнийорганическими жидкостями…
Этот же раздел химической науки подарил нам самые теплостойкие и в то же время самые морозостойкие синтетические каучуки. Температурный интервал работоспособности кремнийорганических каучуков от –80 до +260°C, и эти каучуки уже давно существуют не в виде экзотических лабораторных образцов, а в виде массовой промышленной продукции.
Для современной электротехники очень важны кремнийорганические лаки, представляющие собой растворы кремнийорганических полимеров. Они обладают отличными электроизоляционными свойствами, устойчивы к атмосферным воздействиям, перепадам температур, солнечной радиации. Вот лишь один пример эффективности подобных материалов в технике. До внедрения кремнийорганических лаков изоляция электродвигателя врубовой машины в условиях шахты служила в среднем 5 месяцев. Когда в качестве изоляции стали применять кремнийорганический лак, срок службы двигателя до первого ремонта вырос до 3 лет.
Подобных примеров можно привести десятки, и число их будет множиться с каждым годом: появляются новые вещества, в состав которых наряду с кремнием и традиционными элементами органического мира входят алюминий, титан и другие металлы. Каждый привносит в молекулу что-то свое, и на каком-то этапе количество переходит в качество.
Многие известные ученые работали и продолжают работать в этой области химии. Советскую школу кремний-органиков возглавляет академик К.А. Андрианов, который еще в 1937 г. получил первые в мире кремнийорганические полимеры – полиорганосилоксаны.
Кремний и жизнь
В обзорной статье о кремнии, написанной еще лет десять назад, такой раздел был бы необязателен. Слишком мало знала наука о роли кремния в жизни высших животных и человека. Известно было, что кремний (его двуокись) составляет основу скелетов у некоторых морских организмов – радиолярий, диатомей, некоторых губок, морских звезд. Известно также, что он нужен растениям: от злаков и осоки до пальм и бамбука. Чем жестче стебель растения, тем больше в его золе находят кремния. Растения, как и морские животные, берут кремний из воды. И в пресной, и в соленой воде растворено около 3 мг/л кремния (в виде кремниевых кислот и их солей). Роль же кремния в жизни высших животных и человека долгое время оставалась неясной. Было широко распространено мнение о биологической инертности и бесполезности соединений кремния.
Но, с другой стороны, давно известно серьезное заболевание – силикоз, вызываемое длительным вдыханием пыли, содержащей свободную двуокись кремния. Некоторые кремнийорганические соединения – арилсилатроны оказались токсичными для всех теплокровных животных.
И в то же время известно, что в человеческом организме кремний есть практически повсеместно, больше всего – в костях, коже, соединительной ткани, а также в некоторых железах. При переломах костей содержание кремния в месте перелома возрастает почти в 50 раз. Минеральные воды с высоким содержанием кремния (например, известная кавказская вода «Джермук») оказывают благотворное влияние на здоровье людей, особенно пожилых.
Нельзя сказать, что роль кремния в жизни выяснена уже окончательно – скорее, наоборот: появление новой информации все больше осложняет картину. Синтезом и исследованием биологически активных соединений кремния сейчас заняты во многих лабораториях мира. Очень активно работают над комплексом проблем, который кратко можно назвать так же, как названа эта глава, т.е. кремний и жизнь, сотрудники Иркутского института органической химии во главе с членом-корреспондентом Академии наук СССР М.Г. Воронковым. В одной из своих статей он писал: «Уже имеющиеся многочисленные наблюдения позволяют прийти к заключению о необходимости широких и тщательных исследований (в том числе на молекулярном уровне) роли кремния в живых организмах и изыскания возможностей использовать соединения этого элемента для лечения и профилактики различных заболеваний и травм, а также для борьбы со старением». Пояснения здесь, наверное, требует лишь последний тезис. Дело в том, что установлены возрастные особенности кремниевого обмена в организме: с возрастом содержание этого элемента в костной ткани, артериях, коже существенно уменьшается…
Этот раздел наших знаний об элементе №14 еще не стал сводом общепринятых, устоявшихся истин. Но, очевидно, именно здесь проходит в наши дни передний край борьбы за познание кремния – ближайшего аналога углерода, жизненно важного элемента.
Коротко об изотопах
Природный кремний состоит из трех изотопов с массовыми числами 28, 29 и 30. Преобладает (92,27%) легкий изотоп – кремний-28. Известны также несколько радиоактивных изотопов кремния; долгоживущий лишь один кремний-32 с периодом полураспада около 710 лет.
Больше всего – в силикатах
Во всех природных соединениях кремний связан с кислородом. На долю кремнезема (во всех его разновидностях) приходится около 12% массы земной коры. Намного больше доля силикатов и алюмосиликатов: 75% массы земной коры составлено из этих соединений кремния, кислорода и других элементов, в первую очередь алюминия.
Ферросилиций
Сплав кремния с железом – ферросилиций широко используются в черной металлургии и для изготовления кислотоупорных изделий. Этот сплав готовят, прокаливая смесь двуокиси кремния, угля и железной руды в доменных или электрических печах. На ферросилиций с 15% Si не действуют большинство кислот; правда, он подвержен разрушению соляной кислотой. Чтобы ферросилиций был устойчив к действию и этой кислоты, нужно, чтобы в нем было не меньше 50% Si.
Карборунд – соперник алмаза
Это соединение, как и многие карбиды, отличается прочностью, твердостью, жаропрочностью и химической стойкостью. По твердости кристаллы SiC уступают лишь алмазу и боразону, но поскольку карбид кремния значительно дешевле, его широко применяют для обработки твердых материалов. Получают карборунд в реакции кварцевого песка с углем, проходящей в электрической печи при температуре около 2000°C. Чистый карборунд бесцветен, ему, как и кремнию, свойственны качества полупроводника. А еще это единственное соединение, в котором есть связь кремний – углерод и которое тем не менее не относят к кремнийорганическим соединениям. Очевидно, потому, что вообще все карбиды считаются неорганическими соединениями.
Солнечные батареи
На спутниках, луноходах, космических кораблях и станциях установлены солнечные батареи, преобразующие в электричество лучистую энергию Солнца. В них работают кристаллы полупроводниковых материалов и в первую очередь кремния. При поглощении кванта света в таком кристалле освобождаются электроны. Если такие кристаллы составят довольно внушительных размеров панели, то нетрудно соединить проводником освещенный в неосвещенный участки. По проводнику потечет ток. Кремниевые преобразователи солнечной энергии в электрическую уже работают но только в космосе, но и на земле. А в павильоне «Космос» на ВДНХ их может увидеть каждый.
Стекла, стекла, стекла…
Перефразируя И.А. Крылова, можно сказать: «Что стекла разны, всякий знает». Что без стекла современному человеку пришлось бы худо, – тоже. Что в составе подавляющего большинства стекол есть двуокись кремния, тоже, пожалуй, знают почти все. А вот соотношение различных окислов в составе различных стекол известно лишь химикам. В «нормальном» стекле 75,3% SiO2, в бутылочном – 73, оконном – 72, электроламповом – всего 69,4%. Зато в высокопрочном стекле «пирекс», отличающемся также повышенной химической стойкостью, двуокиси кремния 80,9% – больше, чем в любом другом стекле, кроме, конечно, кварцевого…
И растворимое стекло
Самый распространенный клей – силикатный, он же растворимое стекло, метасиликат натрия Na2SiО3. Это знает каждый школьник, но это не совсем верно. В растворимом стекле наряду с Na2SiO3 содержатся и более сложные силикаты натрия. Помутнение силикатного клея – результат отщепления части молекул SiO2. Этот клей плохо пристает к резине, потому его лучше держать в сосуде с резиновой, а не корковой или тем более стеклянной пробкой.
Кремнии в газах
Некоторые соединения кремния газообразны при обычных условиях. Во-первых, это его тетрафторид – бесцветный газ с резким запахом, который переходит в жидкое состояние лишь при температуре –77°C под давлением 2 атм. Газообразны и два простейших кремневодорода – моносилан SiH4, аналог метана, и дисилан SiН6, аналог этана. Оба эти газа чрезвычайно легко окисляются и обладают малоприятными запахами.
Что такое аметист
Среди веществ состава SiO2 немало поделочных и полудрагоценных камней. Знаменитый лиловый аметист – это природный, окрашенный примесью марганца горный хрусталь. При нагревании до 300…350°C аметисты необратимо обесцвечиваются или даже желтеют. А аметисты, обесцвеченные рентгеновским излучением, способны восстановить свою изначальную окраску.
• Фосфор
• Оглавление
Дата публикации:
18 марта 2002 года
n-t.ru
