Свойства железа. Видеоурок. Химия 9 Класс
Тема: Химия металлов
Урок: Свойства железа
Железо — элемент побочной подгруппы восьмой группы четвёртого периода периодической системы химических элементов Д.И.Менделеева, с атомным номером 26. Обозначается символом Fe. На внешнем четвертом слое атома железа находится 2 электрона:
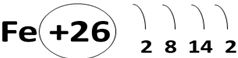
Основные степени окисления железа — +2 и +3, менее характерна для железа степень окисления +6.
Железо — один из самых распространённых в земной коре металлов (второе место после алюминия). В природе железо редко встречается в чистом виде, чаще всего оно встречается в составе железо-никелевых метеоритов. Распространённость железа в земной коре — 4,65 % (4-е место после O, Si, Al). Считается также, что железо составляет бо́льшую часть земного ядра.
Известно большое число руд и минералов, содержащих железо. Наибольшее практическое значение имеют красный железняк (гематит, Fe2O3), магнитный железняк (магнетит, Fe3O4), бурый железняк или лимонит.



а) б) в)
Рис. 1. Железные руды: а — магнетит, б- красный железняк, в – железный колчедан (пирит)
Простое вещество железо— ковкий металл серебристо-белого цвета с высокой химической реакционной способностью: железо быстро коррозирует при высоких температурах или при высокой влажности на воздухе. В чистом кислороде железо горит, а в мелкодисперсном состоянии самовозгорается и на воздухе.
При хранении на воздухе при температуре до 200 C железо постепенно покрывается плотной плёнкой оксида, препятствующего дальнейшему окислению металла. Во влажном воздухе железо покрывается рыхлым слоем ржавчины, который не препятствует доступу кислорода и влаги к металлу и его разрушению. Ржавчина не имеет постоянного химического состава, приближённо её химическую формулу можно записать как Fe
С кислородом железо реагирует при нагревании. При сгорании железа в кислороде образуется оксид Fe3O4 (железная окалина):
3Fe + 2O2 = Fe3O4

Рис. 2. Горение железной проволоки в атмосфере кислорода
При нагревании порошка серы и железа образуется сульфид, приближённую формулу которого можно записать как FeS.
При нагревании железо реагирует с галогенами, азотом, фосфором, кремнием, углеродом.

Рис. 3. Горение железной проволоки в атмосфере хлора
При высокой температуре (выше 700°С) железо реагирует с парами воды:
3Fe + 4H2O = Fe3O4 + 4H2.
Железо не растворяется в холодных концентрированных серной и азотной кислотах из-за пассивации поверхности металла прочной оксидной плёнкой. Горячая концентрированная серная кислота, являясь более сильным окислителем, взаимодействует с железом.
С соляной и разбавленной (приблизительно 20%-й) серной кислотами железо реагирует с образованием солей железа(II):
Fe + 2HCl → FeCl2 + H2↑;
Fe + H2SO4 → FeSO4 + H2↑.
При взаимодействии железа с приблизительно 70%-й серной кислотой реакция протекает с образованием сульфата железа(III):
2Fe + 6H2SO4 → Fe2(SO4)3 + 3SO2↑ + 6H2O.
Оксид железа(II) FeO обладает основными свойствами, ему отвечает основание Fe(OH)2. Оксид железа(III) Fe2O
2Fe(OH)3 + 3H2SO4 → Fe2(SO4)3 + 6H2O.
Гидроксид железа(III) Fe(OH)3 проявляет слабо амфотерные свойства, он способен реагировать только с концентрированными растворами щелочей:
Fe(OH)3 + 3КОН → K3[Fe(OH)6].
При хранении водных растворов солей железа(II) наблюдается окисление железа(II) до железа(III).
Список рекомендованной литературы
1. Оржековский П.А. Химия: 9-й класс: учеб. для общеобраз. учрежд. / П.А. Оржековский, Л.М. Мещерякова, Л.С. Понтак. – М.: АСТ: Астрель, 2007. (§29)
2. Оржековский П.А. Химия: 9-ый класс: учеб для общеобр. учрежд. / П.А. Оржековский, Л.М. Мещерякова, М.М. Шалашова. – М.: Астрель, 2013. (§34)
3. Рудзитис Г.Е. Химия: неорган. химия. Орган. химия: учеб. для 9 кл. / Г.Е. Рудзитис, Ф.Г. Фельдман. – М.: Просвещение, ОАО «Московские учебники», 2009.
4. Хомченко И.Д. Сборник задач и упражнений по химии для средней школы. – М.: РИА «Новая волна»: Издатель Умеренков, 2008.
5. Энциклопедия для детей. Том 17. Химия / Глав. ред. В.А. Володин, вед. науч. ред. И. Леенсон. – М.: Аванта+, 2003.
Дополнительные веб-ресурсы
1. Единая коллекция цифровых образовательных ресурсов (видеоопыты по теме) (Источник).
2. Электронная версия журнала «Химия и жизнь» (Источник).
Домашнее задание
с. 234 №№ 2-4 из учебника П.А. Оржековского «Химия: 9-ый класс» / П.А. Оржековский, Л.М. Мещерякова, М.М. Шалашова. – М.: Астрель, 2013.
Применение железа в промышленности, железо в физни людей
Железо
Чистое железо имеет довольно ограниченное применение. Его используют при изготовлении сердечников электромагнитов, как катализатор химических процессов, для некоторых других целей. Но сплавы железа — чугун и сталь — составляют основу современной техники. Находят широкое применение и многие соединения железа. Так, сульфат железа(III) используют при водоподготовке, оксиды и цианид железа служат пигментами при изготовлении красителей и так далее.
Железо и его сплавы, важнейшие конструкционные материалы в технике и промышленном производстве. Из сплавов железа с углеродом изготавливаются почти все конструкции в машиностроении и тяжелой промышленности. Легковые, грузовые автомобили, станки, железные дороги, корпуса и силовые установки судов – все это делается в основном из стали. Масштаб производства стали является одной из основных характеристик общего технико-экономического уровня развития государства. На долю стали приходится около 95% всей металлической продукции.
Железо может входить в состав сплавов на основе других металлов — например, никелевых. Магнитная окись железа — важный материал в производстве устройств долговременной компьютерной памяти: жёстких дисков, дискет и т. п. Также железо входит в большинство магнитных сплавов.
Железо находит широкое применение в виде солей. Хлорид железа III (хлорное железо) используется в радиолюбительской практике для травления печатных плат. Десятиводный сульфат железа (железный купорос) в смеси с медным купоросом используется для борьбы с вредными грибками в садоводстве и строительстве. Железо применяется в качестве анода в железо-никелевых аккумуляторах, железо-воздушных аккумуляторах.
Железо металлическое, определение — Справочник химика 21
Содержание трехвалентного железа определяется по разности между общим железом и суммой металлического и двухвалентного железа (второе определение). Общее железо определяют из отдельной навески обычным методом.В лаборатории имеется смесь металлического железа с закисью и окисью железа. Для определения количественного состава смеси 1 г ее обработали соляной кислотой и получили при этом 112 мл водорода. 1 г смеси восстановили водородом и получили 0,2115 г воды. Определить количество металлического железа, закиси и окиси железа в смеси. [c.445]
Железо металлическое при растворении в кислоте окисляется до двух- (или трех-) валентного (эквивалент ный вес 27,92 или 18,62) однако, так как определение его производится титрованием Fe + до Fe +, то эквивалентный вес равен атомному весу 55,85. Эквивалентные веса Fe + и Fe + также равны 55,85 и 55,85 (Fe + как в реакции с восстановителем, например, с KI, так и с окислителем после предварительного восстановления до Fe + присоединяет или отдает один электрон).
Для компонентов этой реакции табличные значения энтальпий образования равны соответственно для РвгОз —823 кДж/моль, для СО —110,6 кДж/моль и для СО2 —394 кДж/моль. Для металлического железа, по определению, энтальпия образования нз элементов равна нулю. Следовательно, [c.214]
При это.м условии таким образом можно рассмотреть и взаимодействие бинарных соединений с простыми веществами, приводящее к образованию ковалентных комплексов, например карбонилов. Так, металлическое железо при определенных условиях присоединяет СО [c.82]
ОПРЕДЕЛЕНИЕ ЖЕЛЕЗА МЕТАЛЛИЧЕСКОГО, ДВУХВАЛЕНТНОГО И ТРЕХВАЛЕНТНОГО [c.62]
Железо. Для определения металлического железа в рудах илп шлаках проводят обрабов-ку навески 10%-ным раствором сульфата меди при слабом кипячении под током СО2. На 1—3 г берут 15—20 мл раствора и разбавляют водой до 50—70 мл. [c.15]
Химический состав определяемого вещества очень часто не соответствует составу полученного осадка, хотя это вещество обязательно является составной частью осадка. Например, при определении содержания железа (металлическое железо Ре) весовой формой является РегОз. [c.203]
Например, при анализе металлических сплавов на основе железа (сталей и чугунов) в ряде случаев большое значение имеет не столько определение содержания железа, сколько определение содержания других элементов — С, Si, S, Р, Мп, Сг, Со, Ni, V, W, Мо, Си, А1, Ti, N, О и их соединений, например карбидов, обусловливающих физико-химические и механические свойства сплавов, жаропрочность, коррозионную стойкость в отношении сильно агрессивных сред и т. п. [c.12]
ОПРЕДЕЛЕНИЕ ПРИМЕСИ КОБАЛЬТА В ЖЕЛЕЗЕ МЕТАЛЛИЧЕСКОМ, ОКИСИ ЖЕЛЕЗА И ЖЕЛЕЗО-АММОНИЙНЫХ КВАСЦАХ [c.258]
Определение натертого железа. Для определения натертого железа, попадающего в пробу при измельчении карбида бора в металлической ступке, навеску карбида бора обрабатывают соляной кислотой при кипячении и в фильтрате определяют железо комплексонометрическим методом. [c.217]
Кроме железа, металлический алюминий восстанавливает до валентностей ниже четырех соединения ванадия, титана, а хром-до двухва-тентного, которые затем окисляются бихроматом калия что приводит к завышенным результатам определения железа. Применяемый металлический алюминий должен быть достаточ- [c.37]
В результате проведенной работы были сделаны выводы о том, что лишь в редких случаях можно разработать точный метод прямого определения металла в металлическом порошке или корольков сплава в шлаке из-за частичного растворения окислов металла, например закиси железа при определении металлического железа в железных порошках или закиси марганца при определении корольков металла в шлаках от плавки силикомарганца. [c.4]
В связи с необходимостью контроля железных порошков по ходу ряда технологических процессов в настоящее время большое значение приобретают экспрессные методы приближенного определения в железных порошках содержания железа металлического, закисного, окисного и истинной плотности порошков. [c.5]
Определение железа металлического [c.252]
Определение железа металлического и сульфидов [c.261]
Свинец в шлаках обычно определяется полярографическим методом на фоне соляной кислоты. Трехвалентное железо метает определению, поэтому его восстанавливают до двухвалентного, прибавляя к раствору металлическое железо в виде порошка. Потенциал полуволны восстановления свинца составляет —0,43—0,45 в по отношению к каломельному электроду- [c.82]
Для компонентов этой реакции табличные значения энтальпий образования равны соответственно для FejOa —822,16 для СО —110,53 для СО2 —393,51 кДж/моль. Для металлического железа, по определению, энтальпия образования равна нулю. Следовательно, при 298,15 К [c.247]
Подобный подход продуктивен тогда, когда при образовании с.пожного соединения из бинарных не происходит изменения степени окисления элементов. При этом условии таким образом можно рассмотреть и взаимодействие бинарных соединений с простыми веществами, приводящее к образованию ковалентных комплексов, например карбонилов. Так, металлическое железо при определенных условиях присоединяет СО Fe + 5С0 = [Fe( 0)5], причем в карбониле степень окисления железа остается равной нулю. Во всех остальных случаях взаимодействие бинарного соединения с простым веществом происходит с изменением степени окисления и полученные таким образом продукты не могут рассматриваться как комбинации бинарных соединений. Например, с этих позиций нельзя рассматривать SO2 I2, СаООЬ, h3S2O3 и т.п., поскольку при взаимодействии меняется степень окисления [c.282]
При отсутствии металлического железа и сульфидов, растворимых в разбавленных кислотах, определить содержание закиси и окиси железа особенно легко, когда шлак разлагается одной соляной или серной кислотой или же с добавкой фторида. Требуется только разложить шлак кислотой в атмосфере инертного газа без доступа воздуха и затем титриметрически или колориметрически определить железо(1П). В присутствии металличес
Ржавчина — Википедия
 Цвет ржавчины
Цвет ржавчиныРжа́вчина — является итогом окисления металла. А так же, общим термином для определения оксидов железа. В разговорной речи это слово применяется к красным оксидам, образующимся в ходе реакции железа с кислородом в присутствии воды или влажного воздуха. Есть и другие формы ржавчины, например, продукт, образующийся в ходе реакции железа с хлором при отсутствии кислорода. Такое вещество образуется, в частности, в арматуре, используемой в подводных бетонных столбах, и называют его зелёной ржавчиной. Несколько видов коррозии различимы зрительно или с помощью спектроскопии, они образуются при разных внешних условиях.[1] Ржавчина состоит из гидратированного оксида железа(III) Fe2O3·nH2O и метагидроксида железа (FeO(OH), Fe(OH)3). При наличии кислорода, воды и достаточного времени любая масса железа в конечном итоге преобразуется полностью в ржавчину и разрушается. Поверхность ржавчины не создаёт защиту для нижележащего железа, в отличие от образования патины на медной поверхности.
Ржавчиной, как правило, называют продукт коррозии только железа и его сплавов, таких как сталь. Многие другие металлы тоже подвергаются коррозии, но именно оксиды железа обычно называют ржавчиной.
 Толстый слой ржавчины на звеньях цепи возле моста Золотые Ворота в Сан-Франциско. Цепь постоянно подвергается воздействию сырости и солёных брызг, вызывающих разрушение поверхности, растрескивание и шелушение металла.
Толстый слой ржавчины на звеньях цепи возле моста Золотые Ворота в Сан-Франциско. Цепь постоянно подвергается воздействию сырости и солёных брызг, вызывающих разрушение поверхности, растрескивание и шелушение металла.Причины ржавления[править | править код]
Если железо, содержащее какие-либо добавки и примеси (например, углерод), находится в контакте с водой, кислородом или другим сильным окислителем и/или кислотой, то оно начинает ржаветь. Если при этом присутствует соль, например, имеется контакт с солёной водой, коррозия происходит быстрее в результате электрохимических реакций. Чистое железо относительно устойчиво к воздействию чистой воды и сухого кислорода. Как и у других металлов, например, у алюминия, плотно приставшее оксидное покрытие на железе (слой пассивации) защищает основную массу железа от дальнейшего окисления. Превращение же пассивирующего слоя оксида железа в ржавчину является результатом комбинированного действия двух реагентов, как правило, кислорода и воды. Другими разрушающими факторами являются диоксид серы и углекислый газ в воде. В этих агрессивных условиях образуются различные виды гидроксида железа. В отличие от оксидов железа, гидроксиды не защищают основную массу металла. Поскольку гидроксид формируется и отслаивается от поверхности, воздействию подвергается следующий слой железа, и процесс коррозии продолжается до тех пор, пока всё железо не будет уничтожено, или в системе закончится весь кислород, вода, диоксид углерода или диоксид серы.[2]
Происходящие реакции[править | править код]
 Покрытый ржавчиной и грязью болт. Заметна точечная коррозия и постепенная деформация поверхности, вызванная сильным окислением.
Покрытый ржавчиной и грязью болт. Заметна точечная коррозия и постепенная деформация поверхности, вызванная сильным окислением.Ржавление железа — это электрохимический процесс, который начинается с переноса электронов от железа к кислороду.[3] Скорость коррозии зависит от количества имеющейся воды, и ускоряется электролитами, о чём свидетельствуют последствия применения дорожной соли на коррозию автомобилей. Ключевой реакцией является восстановление кислорода:
- O2 + 4 e− + 2 H2O → 4 OH−
Поскольку при этом образуются гидроксид-анионы, этот процесс сильно зависит от присутствия кислоты. Действительно, коррозия большинства металлов кислородом ускоряется при понижении pH. Обеспечение электронов для вышеприведённой реакции происходит при окисления железа, которое может быть описано следующим образом:
- Fe → Fe2+ + 2 e−
Следующая окислительно-восстановительная реакция происходит в присутствии воды и имеет решающее значение для формирования ржавчины:
- 4 Fe2+ + O2 → 4 Fe3+ + 2 O2−
Кроме того, следующие многоступенчатые кислотно-щелочные реакции влияют на ход формирования ржавчины:
- Fe2+ + 2 H2O ⇌ Fe(OH)2 + 2 H+
- Fe3+ + 3 H2O ⇌ Fe(OH)3 + 3 H+
что приводит к следующим реакциям поддержания баланса дегидратации:
- Fe(OH)2 ⇌ FeO + H2O
- Fe(OH)3 ⇌ FeO(OH) + H2O
- 2 FeO(OH) ⇌ Fe2O3 + H2O
Из приведённых выше уравнений видно, что формирование продуктов коррозии обусловлено наличием воды и кислорода. С ограничением растворённого кислорода на передний план выдвигаются железо(II)-содержащие материалы, в том числе FeO и чёрный магнит (Fe3O4). Высокая концентрация кислорода благоприятна для материалов с трёхвалентным железом, с номинальной формулой Fe(OH)3-xOx/2. Характер коррозии меняется со временем, отражая медленные скорости реакций твёрдых тел.
Кроме того, эти сложные процессы зависят от присутствия других ионов, таких как Ca2+, которые служат в качестве электролита, и таким образом, ускоряют образование ржавчины, или в сочетании с гидроксидами и оксидами железа образуют различные осадки вида Ca-Fe-O-OH.
Более того, цвет ржавчины можно использовать для проверки наличия ионов Fe2+, которые меняют цвет ржавчины с жёлтого на синий.
 Отслаивающаяся краска обнажает участки ржавой поверхности листового металла.
Отслаивающаяся краска обнажает участки ржавой поверхности листового металла.Ржавчина является проницаемой для воздуха и воды, поэтому внутрилежащее железо продолжает разъедаться. Предотвращение ржавчины, следовательно, требует покрытия, которое исключает образование ржавчины. На поверхности нержавеющей стали образуется пассивирующий слой оксида хрома(III). Подобное проявление пассивации происходит с магнием, титаном, цинком, оксидом цинка, алюминием, полианилином и другими электропроводящими полимерами.
Гальванизация[править | править код]
Хорошим подходом к предотвращению ржавчины является метод гальванизации, который обычно заключается в нанесении на защищаемый объект слоя цинка либо методом горячего цинкования, либо методом гальванотехники. Цинк традиционно используется, потому что он достаточно дёшев, обладает хорошей адгезией к стали и обеспечивает катодную защиту на стальную поверхность в случае повреждения цинкового слоя. В более агрессивных средах (таких, как солёная вода), предпочтительнее кадмий. Гальванизация часто не попадает на швы, отверстия и стыки, через которые наносилось покрытие. В этих случаях покрытие обеспечивает катодную защиту металла, где оно выступает в роли гальванического анода, на который прежде всего и воздействует коррозия. В более современные покрытия добавляют алюминий, новый материал называется цинк-алюм. Алюминий в покрытии мигрирует, покрывая царапины и, таким образом, обеспечивая более длительную защиту. Этот метод основан на применении оксидов алюминия и цинка, защищающих царапины на поверхности, в отличие от процесса оксидизации, как в случае применения гальванического анода. В некоторых случаях при очень агрессивных средах или длительных сроках эксплуатации применяются одновременно и гальванизация цинком, и другие защитные покрытия, чтобы обеспечить надёжную защиту от коррозии.
Катодная защита[править | править код]
Катодная защита является методом, используемым для предотвращения коррозии в скрытых под землёй или под водой структурах путём подачи электрического заряда, который подавляет электрохимические реакции. Если её правильно применять, коррозия может быть остановлена полностью. В своей простейшей форме это достигается путём соединения защищаемого объекта с протекторным анодом, в результате чего на поверхности железа или стали происходит только катодный процесс. Протекторный анод должен быть сделан из металла с более отрицательным электродным потенциалом, чем железо или сталь, обычно это цинк, алюминий или магний.
Лакокрасочные и другие защитные покрытия[править | править код]
От ржавчины можно предохранять с помощью лакокрасочных и других защитных покрытий, которые изолируют железо из окружающей среды. Большие поверхности, поделённые на секции, как например, корпуса судов и современных автомобилей, часто покрывают продуктами на основе воска. Такие средства обработки содержат также ингибиторы коррозии. Покрытие стальной арматуры бетоном (железобетон) обеспечивает некоторую защиту стали в среде с высоким рН. Однако коррозия стали в бетоне всё ещё является проблемой.
Покрытие слоем металла[править | править код]
Ржавчина может полностью разрушить железо. Обратите внимание на гальванизацию незаржавевших участков.- Оцинковка (оцинкованное железо/сталь): железо или сталь покрываются слоем цинка. Может использоваться метод горячего цинкования или метод цинкового дутья.
- Лужение: мягкая листовая сталь покрывается слоем олова. В настоящее время практически не используется из-за высокой стоимости олова.
- Хромирование: тонкий слой хрома наносится электролитическим способом на сталь, обеспечивая как защиту от коррозии, так и яркий, полированный внешний вид. Часто используется в блестящих компонентах велосипедов, мотоциклов и автомобилей.
Воронение[править | править код]
Воронение — это способ, который может обеспечить ограниченную устойчивость к коррозии для мелких предметов из стали, таких как огнестрельное оружие и др. Способ состоит в получении на поверхности углеродистой или низколегированной стали или чугуна слоя окислов железа толщиной 1-10 мкм. Для придания блеска, а также для улучшения защитных свойств окисной плёнки, её пропитывают минеральным или растительным маслом.
Снижение влажности[править | править код]
Ржавчины можно избежать, снижая влажность окружающего железо воздуха. Этого можно добиться, например, с помощью силикагеля.
Ингибиторы[править | править код]
Ингибиторы коррозии, как, например, газообразные или летучие ингибиторы, можно использовать для предотвращения коррозии в закрытых системах. Некоторые ингибиторы коррозии чрезвычайно ядовиты. Одним из лучших ингибиторов выступают соли технециевой кислоты.
Ржавчина вызывает деградацию изделий и конструкций, изготовленных из материалов на основе железа. Поскольку ржавчина имеет гораздо больший объём, чем исходное железо, её нарост ведёт к быстрому разрушению конструкции, усиливая коррозию на прилегающих к нему участках — явление, называемое поеданием ржавчиной. Это явление стало причиной разрушения моста через реку Мианус (штат Коннектикут, США) в 1983 году, когда подшипники подъёмного механизма полностью проржавели изнутри. В результате этот механизм зацепил за угол одной из дорожных плит и сдвинул её с опор. Ржавчина была также главной причиной разрушения Серебряного моста в Западной Вирджинии в 1967 году, когда стальной висячий мост рухнул меньше, чем за минуту. Погибли 46 водителей и пассажиров, находившихся в то время на мосту.
 Мост Кинзу после разрушения.
Мост Кинзу после разрушения.Мост Кинзу в штате Пенсильвания был снесён смерчем в 2003 году в значительной степени потому, что центральные опорные болты, соединяющие сооружение с землёй, проржавели, из-за чего мост держался лишь под действием силы тяжести.
Кроме того, коррозия покрытых бетоном стали и железа может вызвать раскалывание бетона, что создает серьёзные конструкторские трудности. Это один из наиболее распространённых отказов железобетонных мостов.
- ↑ Interview, David Des Marais (неопр.) (недоступная ссылка). Архивировано 13 ноября 2007 года.
- ↑ Holleman, A. F.; Wiberg, E. «Inorganic Chemistry» Academic Press: San Diego, 2001. ISBN 0-12-352651-5.
- ↑ Hubert Gräfen, Elmar-Manfred Horn, Hartmut Schlecker, Helmut Schindler «Corrosion» Ullmann’s Encyclopedia of Industrial Chemistry, Wiley-VCH: Weinheim, 2002. DOI: 10.1002/14356007.b01_08
Какая разница между железом, металом и сталью ???
Металл — это вещество, обладающее высокой электрической проводимостью и характерным блеском, а также характерной для металлов зернистой структурой, и еще пластичностью, во.<br>Металлов много: железо, медь, никель, золото, серебро, натрий, литий, алюминий (см. таблицу Менделеева).<br>Железо — это химический элемент (Fe). Он является металлом, как и алюминий, и все остальные металлы.<br>Сталь — это сплав железа с углеродом. В природе нет чистого железа. Также нет ни одного изделия из чистого железа. Все трубы, ложки, вилки, конструкции. Если содержание углерода в сплаве не более 2.5 %(точно не помню) — такой сплав называется сталью. Больше — называется чугуном.
в содержании углерода
железо — этопрежде всего название химического элемента, металл — характеристика химического элемента, а сталь — это смесь железа с чем-то,кажется!
Ну какая-какая… Сталь — сплав, металл — общая характеристика группы элементов, а железо — конкретный представитель этой группы.
ну насколько помню химию, металлы это простое вещество, к ним относят и железо, а сталь это сложное, т.е. сплав железа с углеродом(до 17%)
Химия рулит… Нда… как бы так ответить, чтоб не травмировать твой мозг: железо -это Fe, Fe пренадлежит группе элементов-Металлов, а сталь это вообще-то сплав.
Железо -химический элемент…смотри таблицу Менделеева))…сплав-это соединение различных металлов и др. химических элементов…металл- это группа хим элементов обладающие определенными химическими свойствами…например способностью намагничиваться и окисляться…но опять же не все…ртуть вообще в твердое состояние перевести тяжело…ввиду оччень низкой температуры кристаллизации
Сталь это сплав железа с углеродом и еще какими то добавками-железо это химическии элемент-чистый без примесей.Чистое железо очень дорогое.Металлы -все химические элементы включенные в эту группу таблицей Менделеева.<br>
Все уже сказано<br><br>А чистое железо-не кричное а реликт..где то было обнаружено.Типа инопланетное.И не ржавеет вроде
Ответ прост:<br><br>1. Железо Fe — земельный элемент, входит в состав таблицы Менделеева.<br>2. Металл — сплав, в основе которого может лежать железо, медь, алюминий …Данный сплав как правило имеет различные добавки и компоненты: молибден, хром, ванадий, марганец, углерод …-задачи этих добавок — придать сплаву определенные физ. и хим. свойства. Сплав получается в процессе плавления при определенной температуре.<br>3. Сталь — ето сплав железа и углерода с содержанием последнего <2%<br> Чугун — ето сплав железа и углерода с содержанием последнего >2%<br>
Ну, научную сторону вопроса уже до меня вскрыли совершенно исчерпывающе, поэтому добавлю стишок, который много лет назад был опубликован в какой-то газете. У нас на работе его очень любят и часто поминают (память народная сохранила только две строки) : И мелодично пел весь рейс Стальной чугун железных рельс.
Как много еще осталось металлургов! Жуть!
Первое — частный случай второго (железо — один из металлов, есть и другие металлы, например, олово, медь) . Третье — частный случай первого (сталь — одна из технических форм железа, сплав, есть и другие, например, чугун).
«Металл» — группа химических элементов, в которую входит и «железо» «сталь» сплав железа с углеродом (содержание углерода не более 2%) В обиходе простым языком любое из этих слов может означать одно и то же.
«Металл» — группа химических элементов, в которую входит и «железо» «сталь» сплав железа с углеродом (содержание углерода не более 2%) В обиходе простым языком любое из этих слов может означать одно и то
Металлы это вещества, обладающие металлическим блеском, ковкостью и они проводят эл. ток. Примеры металлов: железо, медь, магний, алюминий, золото, калий… Железо — это чистый чёрный металл. Сталь — это сплав железа и углерода, один из чёрных металлов. Больше углерода: сталь твёрже и хрупче, меньше углерода: сталь более ковкая и пластичная.
как мы предпологаем что железо и металл одно и тоже ( ну тоесть одиноково)
Тяжёлые металлы — Википедия

Тяжёлые мета́ллы — химические элементы со свойствами металлов (в том числе и полуметаллы) и значительным атомным весом либо плотностью.
Понятие «тяжёлые металлы» было предложено немецким химиком Леопольдом Гмелиным в 1817 году[1].
Известно около сорока различных определений термина тяжёлые металлы, и невозможно указать на одно из них, как наиболее принятое. Соответственно, список тяжёлых металлов согласно разным определениям будет включать разные элементы. Используемым критерием может быть относительная атомная масса свыше 50, и тогда в список попадают все металлы, начиная с ванадия, независимо от плотности. Другим часто используемым критерием является плотность, примерно равная или большая плотности железа (8 г/см3), тогда в список попадают такие элементы как свинец, ртуть, медь, кадмий, кобальт, а, например, более легкое олово выпадает из списка. Существуют классификации, основанные и на других значениях пороговой плотности (например — плотность 5 г/см3[2][3]) или атомного веса. Некоторые классификации делают исключения для благородных и редких металлов, не относя их к тяжёлым, некоторые исключают нецветные металлы (железо, марганец).
Термин тяжёлые металлы чаще всего рассматривается не с химической, а с медицинской и природоохранной точек зрения[4].
Таким образом, при включении в эту категорию учитываются не только химические и физические свойства элемента, но и его биологическая активность и токсичность, а также объём использования в хозяйственной деятельности[5].
Многие тяжёлые металлы, такие как железо, медь, цинк, молибден, участвуют в биологических процессах и в определённых количествах являются необходимыми для функционирования растений, животных и человека микроэлементами. С другой стороны, тяжёлые металлы и их соединения могут оказывать вредное воздействие на организм человека, способны накапливаться в тканях, вызывая ряд заболеваний. Не имеющие полезной роли в биологических процессах металлы, такие как свинец и ртуть, определяются как токсичные металлы. Некоторые элементы, такие как ванадий или кадмий, обычно имеющие токсичное влияние на живые организмы, могут быть полезны для некоторых видов[6].
Механизмы действия[править | править код]
Катионы Pb2+, Hg2+, Cd2+ и другие, относимые к группе мягких кислот Льюиса, легко образуют прочные ковалентные связи с тиольными группами SH в молекуле аминокислоты цистеина. Ферменты, содержащие в своём активном центре тиольные группы, при действии даже малых концентраций ионов тяжёлых металлов подвергаются ингибированию, как правило, необратимому, что приводит к серьёзному нарушению обмена веществ. [7]
Среди разнообразных загрязняющих веществ тяжёлые металлы (в том числе ртуть, свинец, кадмий, цинк) и их соединения выделяются распространенностью, высокой токсичностью, многие из них — также способностью к накоплению в живых организмах. Они широко применяются в различных промышленных производствах, поэтому, несмотря на очистительные мероприятия, содержание соединений тяжёлых металлов в промышленных сточных водах довольно высокое. Они также поступают в окружающую среду с бытовыми стоками, с дымом и пылью промышленных предприятий. Многие металлы образуют стойкие органические соединения, хорошая растворимость этих комплексов способствует миграции тяжёлых металлов в природных водах. К тяжёлым металлам относят более 40 химических элементов, но при учёте токсичности, стойкости, способности накапливаться во внешней среде и масштабов распространения токсичных соединений, контроля требуют примерно в четыре раза меньшее число элементов.
Загрязнение океана[править | править код]
Помимо сточных вод, большие массы соединений тяжёлых металлов поступают в океан через атмосферу и с захоронением разнообразных отходов в Мировом океане. Для морских биоценозов наиболее опасны ртуть, свинец и кадмий.
Ртуть[править | править код]
Ртуть переносится в океан с материковым стоком (прежде всего — из стока промышленных вод) и через атмосферу. В составе атмосферной пыли содержится около 12 тыс. т ртути. До трети от этого количества образуется при выветривании пород, содержащих ртуть (киноварь). Ртуть антропогенного происхождения попадает в атмосферу в первую очередь при сжигании угля на электростанциях. Около половины годового промышленного производства этого металла (910 тыс. т) попадает в океан. Некоторые бактерии переводят токсичные хлориды ртути в ещё более токсичную метилртуть[8]. Соединения ртути накапливается многими морскими и пресноводными организмами в концентрациях, во много раз превышающих содержание её в воде.
Употребление в пищу рыбы и морепродуктов неоднократно приводило к ртутному отравлению населения. Так, к 1977 году насчитывалось 2800 жертв болезни Минамата, причиной которой послужило поступление в залив Минамата со сточными водами отходов предприятий, на которых в качестве катализатора использовалась хлористая ртуть. Соединения ртути высокотоксичны для человека.
Свинец[править | править код]
Свинец — рассеянный элемент, содержащийся во всех компонентах окружающей среды: в горных породах, почвах, природных водах, атмосфере, живых организмах. Помимо того, свинец поступает в окружающую среду в результате хозяйственной деятельности человека. До запрета на использование в топливе тетраэтилсвинца в начале XXI века, выхлопные газы транспорта были заметным источником свинца в атмосфере. С континентальной пылью в атмосфере океан получает 20—30 тысяч тонн свинца в год[8].
В организм человека свинец попадает как с пищей и водой, так и из воздуха. Свинец может выводиться из организма, однако малая скорость выведения может приводить к накоплению в костях, печени и почках.
Кадмий[править | править код]
Кадмий является относительно редким и рассеянным элементом, в природе концентрируется в минералах цинка. Поступает в природные воды в результате смыва почв, выветривания полиметаллических и медных руд, и со сточными водами рудообогатительных, металлургических и химических производств. Кадмий в норме присутствует в организме человека в микроскопических количествах. При накоплении организмом соединений кадмия поражается нервная система, нарушается фосфорно-кальциевый обмен. Хроническое отравление приводит к анемии и разрушению костей.
- ↑ Титов А. Ф., Казнина Н. М., Таланова В. В. Тяжелые металлы и растения.. — Петрозаводск: Карельский научный центр РАН, 2014. — С. 7. — 194 с. — ISBN 978-5-9274-0641-8.
- ↑ Металлы // Энциклопедический словарь юного химика. 2-е изд. / Сост. В. А. Крицман, В. В. Станцо. — М.: Педагогика, 1990. — с. 141—144. — 320 с. — ISBN 5-7155-0292-6
- ↑ А. Т. Пилипенко, В. Я. Починок, И. П. Середа, Ф. Д. Шевченко. Металлы. Общие свойства металлов // Справочник по элементарной химии / под ред. академика АН УССР А. Т. Пилипенко. — К.: Наукова думка, 1985. — С. 341—342. — 560 с.
- ↑ «Heavy metals» a meaningless term? — доклад ИЮПАК (англ.)
- ↑ Тяжёлые металлы Архивная копия от 23 марта 2010 на Wayback Machine // Справочник по гидрохимии
- ↑ A biological function for cadmium in marine diatoms. Lane TW, Morel FM.
- ↑ Е.С.Северин. Биохимия: учебник для вузов. — 5-е изд. — М.: ГЭОТАР-Медиа, 2008. — 768 с. с. — ISBN ISBN 978-5-9704-1195-7.
- ↑ 1 2 Ветошкин, 2004.
- Тяжёлые металлы — статья в Большом Энциклопедическом словаре
- Тяжёлые металлы — статья в Экологическом словаре
- Юркова Т. И. Тяжёлые металлы // Экономика цветной металлургии. — Красноярск, 2004.
- А. Г. Ветошкин. Источники загрязнения гидросфер // Процессы и аппараты защиты гидросфер. — Пенза, 2004.
- Н. К. Чертко и др. Биологическая функция химических элементов. — Справочное пособие. — Минск, 2012. — 172 с. — ISBN 978-985-7026-39-5.
- Присутствие макрофитов в водной системе ускоряет снижение концентраций меди, свинца и других тяжёлых металлов в воде. // Водное хозяйство России. 2009. No. 2. с. 58—67.
металлическое железо — это… Что такое металлическое железо?
- металлическое железо
металеве залізо
Словарь металлургической терминов. 2015.
- металлический сплав
- металлическое покрытие
Смотреть что такое «металлическое железо» в других словарях:
Железо — получить на Академике рабочий купон на скидку Ашан или выгодно железо купить с бесплатной доставкой на распродаже в Ашан
ЖЕЛЕЗО — ЖЕЛЕЗО, Ferrum (Fe), тяжелый металл, относящийся к VIII группе периодической системы Менделеева. Ат. в. 55,84(0=16), при чем известны два изотопа с ат. в. в 56 и 54. Чистое Ж. обладает серебристо белым цветом; уд. в. 7,88; оно мягче и более… … Большая медицинская энциклопедия
железо — а; ср. 1. Химический элемент (Fe), ковкий металл серебристого цвета, образующий в соединении с углеродом сталь и чугун. 2. Обиходное название малоуглеродистой стали, металла серебристого цвета. Ковать ж. Ветер стучит железом крыши. 3. О том, что… … Энциклопедический словарь
Железо — (Ferrum) Металл железо, свойства металла, получение и применение Информация о металле железо, физические и химические свойства металла, добыча и применение железа Содержание Содержание Определение термина Этимология История железа Происхождение… … Энциклопедия инвестора
Железо — 26 Марганец ← Железо → Кобальт … Википедия
ЖЕЛЕЗО — Fe (ferrum), химический элемент VIIIB подгруппы периодической системы элементов, металл, член триады железа (Fe, Co, Ni). Железо самородное редко встречается в природе, главным образом в минералах феррит, аваруит и метеоритах (т.н. метеоритное… … Энциклопедия Кольера
Железо — (техн.) Ж. есть наиболее распространенный и наиболее употребительный из металлов. Ж. было известно еще египтянам во время постройки пирамид; у греков упоминается о нем в Илиаде Гомера, причем о нем говорится, как о трудно обрабатываемом металле,… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Феррум металликум — Ferrum metallicum, Железо металлическое — Железо химический элемент VIII группы периодической системы Менделеева. Металл серебристо серого цвета. Изготовление на металлургических заводах. Приготовление растираний по §7. Употребляемые разведения: 3х, 3, 6 и выше.Гомеопатический… … Справочник по гомеопатии
МЕТАЛЛЫ ЧЕРНЫЕ — железо и его сплавы, важнейшие конструкционные материалы в технике и промышленном производстве. Из сплавов железа с углеродом, называемых сталями, изготавливаются почти все конструкции в машиностроении и тяжелой промышленности. Легковые, грузовые … Энциклопедия Кольера
Железные руды — Железо входит в большем или меньшем количестве в состав всех как изверженных, так и осадочных горных пород, но под названием Ж. руд понимают такие скопления железистых соединений, из которых в больших размерах и с выгодой в экономическом… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Желтая или кровещелочная соль — или синь кали, или железисто синеродистый (цианистый) калий (das gelbe Blatlaugensalz, eisenblausaures Kali, Kaliumeisencyanür; lessive de sang, ferrocyanure de potassium, prussiate jaune de potasse; yellow prussiate of potash, ferrocyanide of… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
(243) Ида — У этого термина существуют и другие значения, см. Ида. (243) Ида Открытие Первооткрыватель Иоганн Пализа … Википедия
